फ्रीडेल – क्राफ्ट्स विक्रिया : निर्जल ॲल्युमिनि यम क्लोराइड उत्प्रेरक ( विक्रियेमध्ये प्रत्यक्ष भाग न घेता तिची गती बदलणारा पदार्थ ) म्हणून वापरले असता , ॲरोमॅटिक हायड्रोकार्बनांतील [→ ॲरोमॅटिक संयुगे ] हायड्रोजन अणूच्या जागी अल्किल व ॲसिड गट [ → मू लके] प्रतिष्ठापित करून ( बसवून ) अनुक्रमे हायड्रोकार्बन व किटोन वर्गाची संयुगे बनविता येतात , हे १८७७ मध्ये शार्ल फ्रीडे ल व जेम्स मेसन क्रा फ्ट् स यांनी दाखविले व त्यावरून या विक्रियेला फ्री डेल – क्राफ्ट् स विक्रिया हे नाव देण्यात आले परंतु त्यानंतर झालेल्या संशोधनामुळे या विक्रिया क्षेत्राची व्याप्ती बरीच वाढली आहे . आधुनिक व्याख्येप्रमाणे ल्यूइस अम् ल प्रकारची ( जी . एन् . ल्यूइस या रसायनशास्त्रज्ञांच्या नावावरून ओळखण्यात येणाऱ्या अम्ल प्रकारची ) हॅलाइडे किंवा प्रोटॉन अम्ले [ → अम्ले व क्षारक अम्ल – हॅलाइडे] हे उत्प्रेरक वापरून घडविलेल्या प्रतिष्ठापन , ⇨ समघटकीकरण , निरास , ⇨ बहुवारि कीकरण व समावेशन अशा विविध विक्रियांचा [ → रा सायनिक विक्रिया] यात समावेश केला जातो . मूळच्या विक्रियेत कार्बन अणूंमध्येच परस्परात बंध निर्माण करता येत पण नंतरच्या प्रगतीमुळे कार्बन व ऑक्सिजन , कार्बन व नायट्रोजन , कार्बन व गंधक , कार्बन व हॅलोजने , कार्बन व फॉस्फरस या अणूंमध्येही बंध निर्माण करणे साध्य झाले आहे . तसेच मूळ विक्रिया ॲरोमॅटिक हायड्रोकार्बनांपुरतीच मर्यादित होती , तशी ती आता राहिलेली नाही . ॲलिफॅटिक व ॲलिसायक्लिक संयुगांवरही [⟶ ॲलिफॅटिक संयुगे ॲलिसायक्लिक संयुगे] ती घडविता येते , असे सिद्ध झाले आहे .
उत्प्रेरक : या विक्रियांमध्ये वापरले जाणारे उत्प्रेरक इलेक्ट्रॉन स्वीकारणारी संयुगे असतात . त्यांचे वर्गीकरण पुढे दिल्याप्रमाणे करतात .
(१) अम्ल – हॅलाइडे ( ल्यूइस अम्ले ) : ॲल्युमिनियम क्लोराइड व ब्रोमाइड आणि बोरॉन ट्रायल्युओराइड ही या वर्गाची संयुगे विशेष वापरली जातात . ॲल्युमिनियम क्लोराइड स्वस्त व सहज मिळणारे असल्यामुळे औद्योगिक उत्पादन विक्रियांमध्ये विशेष पसंत केले जाते . बेरियम क्लोराइड , कॅडमि य म क्लोराइड , झिंक क्लोराइडे ( ZnCl2 व ZnCl4 ) , फेरिक क्लोराइड व बोरॉन ट्रायक्लोराइड ही संयुगेही उत्प्रे रक म्हणून उपयोगी पडतात . [⟶ अम्ल – हॅलाइडे ] .
( २ ) धातु – अल्किल वर्गाची संयुगे व अल्कॉक्साइडे : ॲल्युमिनियम , बोरॉन व जस्त यांची अल्किल संयुगे आणि ॲल्युमिनियम फिनॉक्साइड ही या वर्गात येतात .
( ३ ) प्रोटॉन अम्ले ( ब्रॉन्स्टेड अम्ले जे . एन् . ब्रॉन्स्टेड या रसायनशास्त्रज्ञांच्या नावाने ओळखण्यात येणारी अम्ले ): सल्फ्यू रिक अम्ल , निर्जल हायड्रोजन फ्ल्यु ओराइड , फॉस्फोरि क व पॉलि फॉस्फोरि क अम्ले , तसेच परक्लोरिक , क्लोरोसल्फॉनिक , पॅराटोल्यूइन सल्फॉनिक व क्लोरोॲसिटिक अम्ले या वर्गात येतात .
( ४ ) अम्लीय ऑक्साइडे व सल्फाइडे : ॲल्युमिना व सिलि का किंवा त्यांची नैसर्गिक अथवा संश्लेषि त ( कृत्रिम री तीने तयार केलेली ) मिश्रणे उत्प्रेरक म्हणून वापरण्यात येतात . त्यांमध्ये क्रोमियम , मॅग्नेशियम , मॉलिब्डेनम , थोरियम , टंगस्टन व झिर्कोनियम यांची ऑक्साइडेही मिश्ररूपात असण्याची शक्यता असते . त्याचप्रमाणे मॉलिब्डेनमाची सल्फाइडे असू शकतात .
( ५ ) ॠनायन – विनियमक रेझिने : [⟶ रेझिने ] . उदा . , सल्फॉनीकरण केलेली पार्श्व संबद्ध स्टायरीन व डायव्हिनि ल बें झी न यांची बहुवारिके ( एक अथवा अधिक अणुसमुच्चय पुनः पुन्हा जोडले जाऊन बनलेली मोठा रेणु भार असलेली संयुगे ).
विद्रावक : ( विरघळविणारा पदार्थ ). या विक्रिया घडविण्यासाठी सामान्यतः ज्या हायड्रोकार्बनावर विक्रिया घडवावयाची ते द्रवरूप असेल , तर तेच अतिरिक्त प्रमाणात विद्रावक म्हणून वापरले जाते . ते शक्य नसेल , तर कार्बन डायसल्फाइड , पेट्रोलियम ईथर , एथिलीन क्लोराइड , मिथिलीन क्लोराइड , कार्बन टेट्राक्लोराइड , नायट्रोबें झी न , नायट्रोमिथेन , नायट्रोएथेन व नायट्रोप्रोपेन ही संयुगे विद्रावक म्हणून वापरतात . ही नायट्रोसंयुगे ॲल्युमिनियम क्लोराइड आणि इतर अम्ल धातू – हॅलाइडे यांच्याबरोबर जटि ल संयुगे बनवितात . त्यामुळे ती वापरली असता असमान विभा जन होणे , डांबरासारखे पदार्थ बन णे इ . अनिष्ट गोष्टी टळतात . ज्या ठिकाणी विक्रियाकारक सौम्य आणि ज्यावर विक्रिया व्हावयाची ते संयुग अतिविक्रियाशील असेल अशा ठिकाणी ऑ र्थोडायक्लोरोबें झी न , डाय- एथिल ई थर किंवा बें झी न हे विद्रावक म्हणून वापरतात पण अशा ठिकाणी विद्रावकावर रासायनिक विक्रिया होण्यास अवसर मिळणार नाही , इतक्या त्वरेने विक्रिया घडणे आवश्यक असते . काही विक्रियांमध्ये विद्रावकानुसार वेगवेगळी विक्रियाफले मिळतात , असे दिसून आले आहे . उदा . , कार्बन डाय सल्फाइड किंवा टेट्रानायट्रोमिथेन हे विद्रावक वापरले , तर नेप्थॅलिनात १ या स्थानी आणि नायट्रोबें झी न किंवा नायट्रोमेसिटीलीन वापरले , तर २ या स्थानी प्रतिष्ठापन घडते , असे दिसून आले आहे .
अल्किलीकरण : [ एखाद्या कार्बनी संयुगाच्या रेणूमध्ये प्रतिष्ठापन किंवा समावेशन विक्रियेने अल्किल गटाचा प्रवेश घडविण्याला अल्कि ली करण म्हणतात ⟶ अल्किलीकरण ] . ॲरोमॅटिक केंद्रकातील हायड्रोजन अणूंचे अल्किल गटांनी प्रतिष्ठापन झाले म्हणजे अल्किलीकृत हायड्रोकार्बने निर्माण होतात . यासाठी प्रारंभी अल्किल हॅलाइडे अल्किलीकारक म्हणून वापरली जात . ही विक्रिया सू त्र २ मध्ये दर्शविल्याप्रमाणे घडते .
|
Alcl3 |
||||||
|
ArH |
+ |
RX |
⟶ |
ArR |
+ |
HX |
|
ॲरोमॅटिक हायड्रोकार्बन |
अल्किल हॅलाइड |
अल्किल हायड्रोकार्बन |
हॅलोजन अम्ल |
|||
|
सूत्र २. ॲरोमॅटिक हायड्रोकार्बना चे अल्किलीकरण |
||||||
आधुनिक काळात अल्किलीकारके म्हणून अल्कोहॉले , अल्किने [ द्विबंध असलेली ॲलिफॅटिक हायड्रोकार्बने ⟶ अलिफॅटिक संयुगे ], अल्काइने ( त्रिबंध असलेली ॲलिफॅटिक हायड्रोकार्बने ) , कार्बॉक्सिलिक व खनिज अम्लांची एस्टरे , इथरे , आल्डिहाइडे , किटोने , पॅराफिने , सायक्लोपॅराफिने , थायॉले , सल्फाइडे , अमाइने व थायोसायनेटे अशी विविध संयुगे वापरली जातात .
विक्रियेसाठी वापरलेल्या उत्प्रेरकाची आणि अल्किलीकारकाची विक्रियाशी लता , प्रमाण , विक्रियेचे तापमान , कालावधी आणि विद्रावक यांवर संश्लेषणा ने मिळणाऱ्या संयुगात एक किंवा अधिक अल्किल गट प्रतिष्ठापनाने येतील हे व द्विप्रतिष्ठापि त संयुगे बनली असता ऑर्थो , मेटा व पॅरा यांपैकी कोणता समघटक जास्त प्रमाणात तयार होईल हे अवलंबून असते .
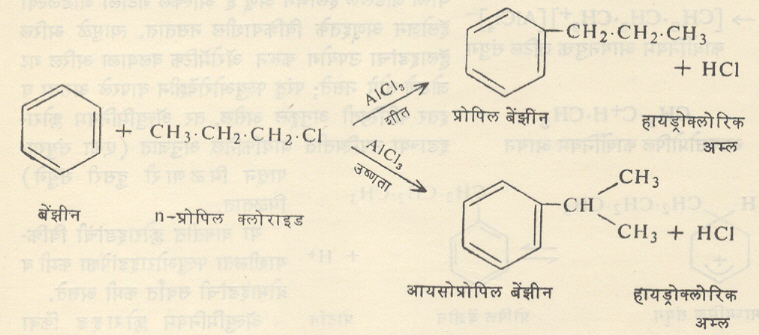
विक्रिया होतांना विक्रियाकारकाचा पुनर्विन्यास ( नवी निराळी मांडणी ) होण्याची शक्यताही असते त्यामुळे अपेक्षित संयुगाऐवजी वा त्याच्याबरोबर समघटकी संयुगे मिळण्याची शक्यता ही असते . उदा . , n– ब्युटिल क्लोराइड हा विक्रियाकारक ॲल्युमिनि यम क्लोराइड या उत्प्रेरकाबरोबर वापरला असता मुख्यतः द्वितीयक ब्युटिल बेंझीनच बनते पण हाच उ त्प्रे रक असताना n– प्रोपिल क्लोराइड वापरले , तर प्रोपिल बेंझिनाबरोबर विक्रियाकारकाचा पुनर्विन्यास झाल्यामुळे आयासोप्रोपिल बेंझिनही तयार होते ( सू त्र ३ ) . उत्प्रेरक , अल्किलीकारक , तापमान आणि विद्रावक यांवर हे फेरफार अवलंबून असतात .
एका रेणूमध्ये असलेले अल्किल गट तेथून निघून दुसऱ्या रेणूत प्रतिष्ठापनाने जाणेही या विक्रियांत शक्य असते . उदा . , बेंझीन व पॉलिएथिल बेंझिन यांमध्ये विक्रिया होऊन एथिल बेंझिन निर्माण होते . आयसोप्रोपिल व तृतीयक ब्युटिल गट अशा तऱ्हेने फार सुकरतेने स्थानांतरित होतात . एका गटाच्या जागी दुसरा गटही या विक्रियांत येऊ शकतो .
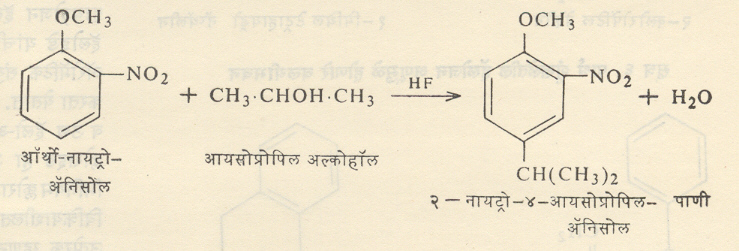
ॲरोमॅटिक वलयात मेटा स्थानी प्रतिष्ठापन होण्यास अनुकूल असे गट असतील , तर फ्रीडेल – क्राफ्ट् स विक्रिया घडून येत नाही उदा . , नायट्रोबेंझीन व ॲसिटोफेनोन यांचे अल्किलीकरण घडविता येत नाही परंतु अशा गटांच्या बरोबर ऑर्थो व पॅरा स्थानी प्रतिष्ठाप ना स अनुकूल असे प्रभावी गट असतील , तर मात्र विक्रिया घडून येते . उदा . , सूत्र ४ मधील विक्रिया , येथे OCH3 गटाच्या प्रभावामुळे पॅरा स्थानी प्रतिष्ठापन होते .
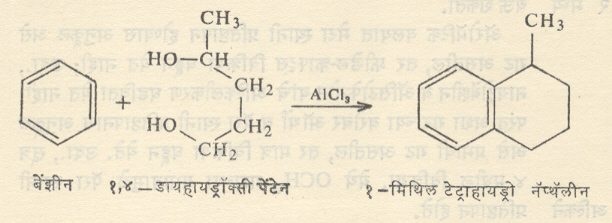
अल्किलीकारकामध्ये जर दोन कार्यकारी केंद्रे असतील ( उदा . , डायहॅलाइडे , अतृप्त – विक्रियेत इतर अणूंचा समावेश होऊ शकणारी – हॅलाइडे , डायॉले , अतृप्त अल्कोहॉले , डायओलेफिने इ . संयुगे ) , तर त्यांच्या विक्रियेने ॲरोमॅटीक हायड्रोकार्बनापासून विवृत ( टोके मोकळी असलेली ) शृंखलायुक्त संयुगे काही प्रमाणात तयार होतात पण वलयीभवनास अनुकूल परिस्थिती असेल , तर मुख्यतः वलयी अल्किल संयुगे बनतात . ती बनताना बहुधा एका केंद्राची विक्रिया होऊन प्रथम दुसरा कार्यकारी गट शिल्लक असलेले ॲरोमॅटीक संयुग प्रथम बनत असावे आणि त्यानंतर दुसऱ्या केंद्राची विक्रिया होऊन वलय बनत असावे ( सूत्र ५ ) .
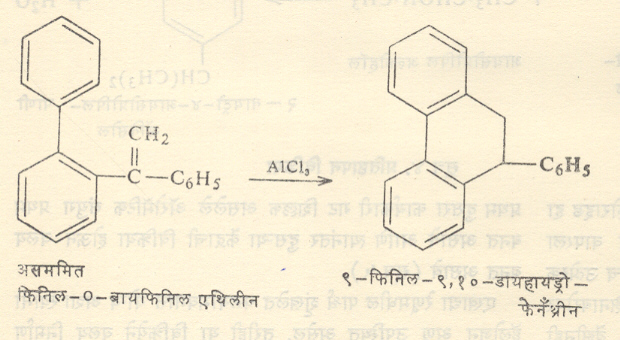
एखाद्या रेणूमधील पार्श्व शृंखलेत वलयीभवनास योग्य अशा स्थानी हॅलोजन उपस्थित असेल , तरीही या विक्रियेने वलय निर्माण होते . ( सूत्र ६ ). पार्श्व शृंखलेत द्वि बंध असेल , तरीही वलयीभवन घडून येते ( सूत्र ७ ). या पद्धतीने संघनित वलय समूह निर्माण करता येतात .
मूळ फ्रीडेल – क्राफ्ट् स विक्रियेत ॲरोमॅटीक हायड्रोकार्बनां च्या अल्किलीकरणाचाच अंतर्भाव आहे परंतू आधुनिक संशोधनामुळे मिथे न व एथेन वगळ्यास इतर पॅराफिनांचे अल्किलीकरण या विक्रियेने करणे साध्य झाले आहे . उदा . , ॲल्युमिनियम क्लोराइड हा उत्प्रेरक वापरला असता आयसोब्युटेनापासून एथिलिनाच्या विक्रियेने हेक्झेन , ऑक्टेन व डेकेन आणि त्यांची संघटक संयुगे बनविता येतात . त्याचप्रमाणे संहत ( ज्याचे विद्रावातील प्रमाण जास्त आहे असे ) सल्फ्यूरिक अम्ल (९६ – ९७ %) उत्प्रेरक म्हणून वापरून आयसोब्युटेन , आयसोपेंटेन व आ यसोहेक्झेन यांचे अल्किलीकरण ओलेफीन संयुगांच्या विक्रियेने घडवून आणता येते . या प्रकारे उच्च ऑक्टेन अंक असलेली [ ठोका – वि रोधक गुण दर्शविणारा निर्देशांक उच्च असलेली ⟶ अंतर्ज्वलन – एंजिन ] इंधने औद्योगिक प्रमाणावर बनविण्यात आली आहेत .
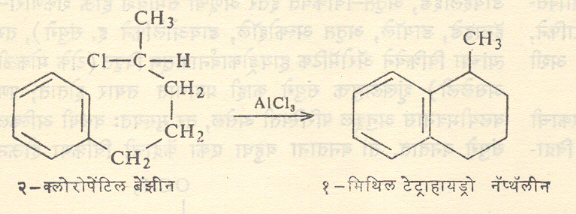

यंत्रणा : अल्किलीकरण विक्रियेत प्रथम ॲल्युमिनियम क् लोराइडासारख्या ल्यूइस अम्लाचा विक्रियाकारकावर परिणाम होतो व कार्बोनियम आयन ( कार्बनाचा समावेश असलेला सहसंयुजी बंध – ज्यात प्रत्येक बंधि त अणूने एकेक इलेक्ट्रॉन देऊन इलेक्ट्रॉनांची जोडी तयार होते असा बंध – तुटून बनणारा अल्पायुषी धन विद्युत् भारित खंड ) निर्माण होतो . उदा . , प्रोपिल क्लोराइडापासून प्रोपिल कार्बोनियम आयन सूत्र ८ मध्ये दाखविल्याप्रमाणे बनतो व ॲल्युमिनि यम क्लोराइडाबरोबर त्याचे जटि ल संयुग बनते . प्रोपिल कार्बोनियम आयनापासून आयसोप्रोपिल कार्बोनियम आयन ही बनतो . नंतर कार्बोनियम आयनांची ॲरोमॅटिक हायड्रोकार्बनाशी ( उदा . , बें झि नाशी ) विक्रिया होते आणि अखेरीस एक प्रोटॉन मुक्त होऊन अल्कि लीकृत संयुग निर्माण होते .
हॅलो – अल्कि लीकरण : हॅलो – अल्कि ल ई थरे व सल्फा इडे , डाय आणि पॉलि हॅलो हायड्रोकार्बने , हॅलो – अल्किने , हॅलो – अल्कोहॉले , हॅलो – अल्किल सल्फेटे आणि आ ल्डिहाइडे व हायड्रोजन हॅलाइडे यांची किंवा ॲसिटाले व हायड्रोजन हॅलो इडे यांची मिश्रणे विक्रियाकारक म्हणून वापरली असता ॲरोमॅटिक संयुगामध्ये हॅलोजनयुक्त अल्किल गट प्रतिष्ठापित करता येतात. या प्रकारे हॅलोमिथिलीकरण, हॅलोएथिलीकरण व उच्च हॅलो – अल्किलीकरणे घडवून आणली जातात . झिंक क्लोराइड हा उत्प्रेरक सामान्यतः वापरला जातो. ॲ ल्युमिनियम क्लोराइडाबरोबर वितळवून हा वापरला असता त्याची विक्रियाशीलता वाढते. कित्येक ठिकाणी खनिज अम्लेही उत्प्रेरक म्हणून वापरतात . ॲसिटिक अम्ल , डाय – एथिल ईथर , डायऑक्झेन , कार्बन टेट्राक्लोराइड , एथिलीन क्लोराइड , नायट्रोबेंझीन इ . पदार्थ विद्रावक म्हणून वापरले जातात .
हॅलो – अल्किलीकरणाने बनलेल्या संयुगाची पुन्हा मुळ हायड्रोकार्बनावर विक्रिया होऊन डाय – अरिल अल्केने किंवा अल्किलीकृत वलयी संयुगे सहविक्रिया फले म्हणून मिळतात ( सूत्र ९ ).
ॲरोमॅटिक संयुगांचे अरिलीकरण : ॲरोमॅटिक वलयाला जोडलेले हॅलोजन अणू हे अल्किल गटाला जोडलेल्या हॅलोजन अणूइतके विक्रियाशील नसतात . त्यामुळे अरिल हॅलाइडांचा उपयोग करून ॲरोमॅटिक वलयाला अरिल गट जोडणे सोपे नसते परंतु फ्ल्यु ओरोबेंझीन वापरले असता व इतर परिस्थिती अनुकूल असेल , तर ॲल्यु मिनी यम क्लोराइडाच्या उपस्थितीत बायफिनि ल अनुजात ( एका संयुगापासून मिळणारी दुसरी संयुगे ) मिळतात .
या बाबतीत क्लोराइडांची विक्रियाशीलता फ्ल्यु ओराइडांपेक्षा कमी व ब्रोमाइडांची सर्वांत कमी असते .
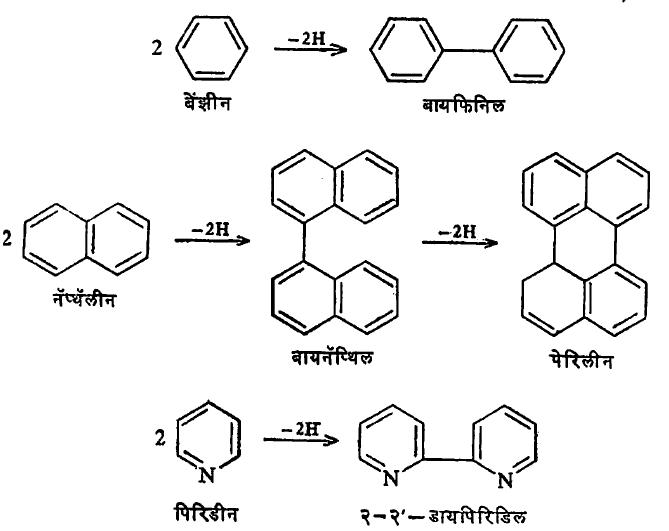
ॲल्युमिनियम क्लोराइड किंवा तत्सम उत्प्रेरकाच्या योगाने ॲरोमॅटिक वलयांतील हायड्रोजन अणूंचा निरास घडवून ॲरोमॅटिक वलयामध्ये बंध निर्माण करता येतात . ( सूत्र १० ).
ॲसिलीकरण : [⟶ ॲसिलीकरण ] . ॲरोमॅटिक संयुगात ॲल्युमिनियम क्लोराइड, बोरॉन
C 6 H 6 ⟶ C 6 H 5· CH 2 ·C I ⟶ C 6 H 5 ·CH 2 ·C 6 H 5
बेंझीन बें झिल क्लोराइड
सूत्र ९ . हॅलो – अल्किलीकरणाने बनलेल्या संयुगाची बेंझिनाशी विक्रीया होऊन मिळणारी सहविक्रिया फले .
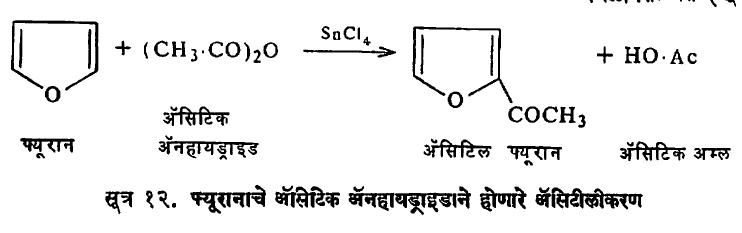
ट्राय फ्ल्यु ओराइड इ . उत्प्रेरकांच्या उपस्थितीत ॲसिल गट प्रतिष्ठापित करून कीटोने बनविता येतात ( सूत्र ११ ). त्यासाठी ॲसिल हॅलाइडे , अम्ल ॲनहायड्राइडे , एस्टरे , अम्ले , कीटोने , अमाइडे आणि नायट्राइले विक्रियाकारक म्हणून उपयोगी पडतात ( सूत्र १२ ).
|
Alcl3 |
||||||
|
ArH |
+ |
R·COX |
⟶ |
ArCOR |
+ |
HX |
|
ॲरोमॅटिक संयुग |
अल्किल हॅलाइड |
कीटोन |
हॅलोजन अम्ल |
|||
|
सूत्र ११.अरोमॅटिक संयुगाच्या असिलीकरणाने कीटोनाचे संश्लेषण. |
||||||
सामान्यतः एकापेक्षा जास्त ॲसिल गट ॲरोमॅटिक वलयास जोडता येत नाहीत . ऑर्थो व पॅरा स्थानी प्रतिष्ठापन करण्यास अनुकूल असे गट वलयात असतील , तर ॲसिल गट पॅरा स्थानी जोडला जातो .
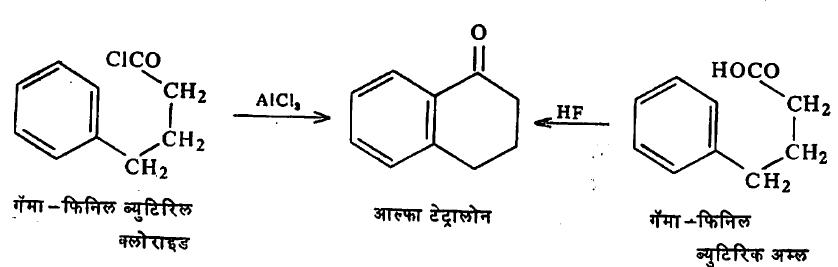
ॲरोमॅटिक संयुगाला पार्श्व शृंखला असून तीमध्ये COC I गट असेल , तर ॲल्यु मिनि यम क्लोराइड उत्प्रेरक वापरून वलयी की टोने बनविता येतात . पार्श्व शृंखलेत COOH गट असेल , तर हायड्रोजन फ्ल्यु ओराइड या उत्प्रेरकाने अशीच विक्रिया घडविता येते ( सूत्र १३ ).
ॲरोमॅटिक आल्डिहाइडांचे संश्लेषण : फॉर्मिल फ्ल्युओराइड हा विक्रियाकारक वापरला असता ॲरोमॅटिक संयुगातील हायड्रोजनाच्या जागी CHO गट प्रतिष्ठापित होऊन आल्डिहाइड बनते ( सूत्र १४ ).
|
ArH |
+ |
FCHO |
⟶ |
Ar COR |
+ |
HF |
|
ॲरोमॅटिक संयुग |
|
फॉर्मिल फ्ल्युओराइड |
|
अरोमॅटिक आल्डिहाइड |
|
हायड्रोजन फ्ल्युओराइड |
|
सूत्र १४.अरोमॅटिक आल्डिहाइडाचेसंश्लेषण. |
||||||
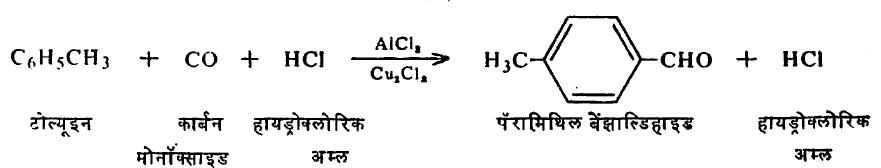
कार्बन मोनॉक्साइड व हायड्रोक्लोरिक अम्ल यांचे मिश्रण विक्रियाकारक म्हणून आणि ॲल्युमिनियम क्लोराइड व क्युप्रस क्लोराइड यांचे मिश्रण उत्प्रेरक म्हणून वापरले असताही आल्डिहाइडे निर्माण होतात ( सूत्र १५ ).
ॲरोमॅटिक कार्बॉक्सिलिक अम्लांचे संश्लेषण : ॲल्युमिनियम क्लोराइड हा उत्प्रेरक आणि कार्बन डायसल्फाइड हा विद्रावक म्हणून वापरला असता ॲरोमॅटिक संयुगावर कार्बोनिल क्लोराइडाची विक्रिया होऊन प्रथम अरिल क्लोराइड बनते . त्याच्या जलीय विच्छेदनाने ( पाण्याच्या विक्रियेने रेणूचे तुकडे करण्याने ) कार्बॉक्सिलिक अम्ल मिळविता येते ( सूत्र १६ ).
ॲलिफॅटिक व सायक्लोॲलिफॅटिक संयुगांचे ॲसिलीकरण : ॲसिल हॅलाइडांच्या विक्रियेने ओलेफिने व सायक्लोओलेफिने यांपासून अनुरूप अतृप्त कीटोने बनविता येतात ( सूत्र १७ ).
अम्ल ॲनहायड्राइडांनीही अशीच विक्रिया घडते . ॲसिटिलिनिक संयुगांपासून बीटा क्लोरोव्हिनील कीटोने मिळतात .
ॲलिफॅटिक कार्बॉक्सिलिक अम्लांचे संश्लेषण : स ल्फ्यू रिक अम्ल आणि बोरॉन ट्रायफ्ल्युओराइड हे उत्प्रेरक , ७५º– १००º से . तापमान आणि उच्च दाब ( वातावरणीय दाबाच्या ६००– ७०० पट दाब ) वापरून अल्किनावर कार्बन मोनॉक्साइडाची विक्रिया घडविली , तर ॲलिफॅटिक कार्बॉक्सिलिक अम्ले बनतात ( सूत्र १८ ).

कार्बन मोनाॅ क्साइडाऐवजी फॉर्मिक अम्ल वापरले , तर ही च विक्रिया ०० – ४०० से . तापमानास व कमी दाबास घडून येते .
सूत्र १८ . अलिफॅटिक कार् बॉक्सीलिक अम्लाचे संश्लेषण
सल्फॉनीकरण : [⟶ सल्फॉनीकरण ] . हायड्रोजन फ्ल्युओराइड किंवा बोरॉन ट्रायफ्ल्युओराइड हा उत्प्रेरक वापरला , तर ॲरोमॅटिक हायड्रोकार्बनां चे सल्फॉनीकरण होऊन सल्फानिक अम्ले बनतात ( सूत्र १९ ).
सूत्र १९ . अरोमॅटिक हायड्रोकार्बनाचे सल्फॉनीकरण
सल्फो निलीकरण : सल्फॉनिक हॅलाइडे किंवा सल्फानिक अम्ल ॲनहायड्राइडे यांची ॲरोमॅटिक हायड्रोकार्बनावर विक्रिया ॲल्युमिनियम क्लोराइड हा उत्प्रेरक वापरून घडविली म्हणजे सल्फो निलीकरण होऊन सल्फाॅ न वर्गाची संयु गे बनतात .
नायट्रीकरण : स ल्फ्यू रिक व परक्लोरिक ही प्रोटॉ न अम्ले आणि बोरॉन ट्रायफ्ल्युओराइड , ॲ ल्युमिनियम क्लोराइड , फेरिक क्लोराइड इ . ल्यू इस अम्ल हॅलाइ डे उत्प्रे रक म्हणून वापरून नायट्रिक अम्लाने , त्याचप्रमाणे नायट्रिल क्लोराइड आणि डाय नायट्रो जन पेंटाक्साइड या विक्रियाकारकांनी ॲरोमॅटिक हायड्रोकार्बनांचे नायट्री करण घडविता येते . [⟶ नायट्री करण ] .
हॅलोजनीकरण : क्लोरीन , ब्रोमीन व आयोडीन किंवा आयोडिन मोनोक्लोराइड , ब्रोमीन मोनोक्लोराइड या विक्रियाकारकांनी फेरिक क्लोराइड , ॲल्युमिनियम क्लोराइड इ. उत्प्रेरक वापरून ॲरोमॅटिक हायड्रोकार्बनांचे हॅलोजनीकरण करता येते . [⟶ हॅलोजनीकरण ] .
समघटकीकरण : n– ब्यूटेन व त्यासारख्या सरळ कार्बन शृंखला असलेल्या हायड्रोकार्बनाचे समघटकी क रण करून आयसोब्युटेन व तत्सम हायड्रोकार्बने मिळविता येतात . याकरिता ॲल्युमिनियम क्लोराइड , बोरान ट्रायफ्ल्युओराइड , स ल्फ्यू रिक अम्ल इ . उत्प्रे र क वापरण्यात येतात [⟶ समघट की करण ] .
बहुवारिकीकरण : ॲ ल्युमिनियम क्लोराइड , बोराॅ न ट्रायफ्ल्युओराइड इ . ल्यू इस अम्लांच्या उत्प्रेरण क्रियेने आयसो – ब्युटिली न , स्टायरीन , आल्फा मिथिल स्टायरीन , ब्युटाडा इ न आणि व्हिनिल आल्कि ल ईथरे यांचे बहुवारिकीकरण घडविता येते . गॅसोलिना सारखी इंधने , वंगणे व उच्च रेणुभाराची बहुवारिके बनविण्यासाठी या विक्रियेचा उपयोग होतो [⟶ बहुवारिकीकरण ] .
उपयोग : डीडीटी , फिनॉलप्थॅलीन , एथिल बेंझीन , क्युमीन , ॲसिटोफेनोन , प्रोपियोफेनोन इ . उपयुक्त संयुगे , तसेच गॅसोली न व प्रक्षालके ( वस्तू स्वच्छ करण्यासाठी वापरण्यात येणारे संश्लेषित पदार्थ डिटर्जंट्स ) बनविण्यासाठी आणि प्लॅस्टिके व कृ त्रि म रबरे इत्यादीं साठी उपयोगी पडणारी अनेक बहुवारिके तयार करण्याकरिता , त्याचप्रमाणे रासायनिक संशोधनात ही विक्रिया उपयोगी पडते .
संदर्भ : 1. Mark, H. F. MacKetta, J. J Othmer, D. F., Ed. Kirk-Othmer Encyclopedia of Chemical Technology, Vol. 10 , New York, 1966 .
2. Olah, G. A., Ed., Friedel-Crafts and Related Reactions, 4 Vols ., New York, 1963 – 65 .
केळकर , गो . रा . मिठारी , भू . चिं .
“