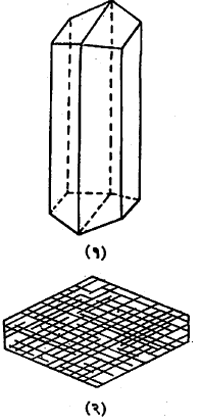
अँफिबोल गट : खनिजांच्या एका गटाचे नाव. स्फटिकांच्या संरचनेत व इतर भौतिक गुणधर्मांत व रासायनिक संघटनांत पुष्कळच साम्य असणाऱ्या अनेक खनिज जातींचा समावेश या गटात होतो. त्यांच्यापैकी काहींचे स्फटिक समचतुर्भुजी व काहींचे एकनताक्ष वर्गाचे असतात [→ स्फटिकविज्ञान]. या गटातील खनिजांच्या घटक आयनांपैकी (विद्युत् भारित अणू, रेणू वा अणुगट यांपैकी) एखाद्या आयनाच्या जागी त्याच्या एवढेच आकारमान असलेले इतर आयन येऊ शकत असल्यामुळे त्या खनिजांच्या समाकृतिक (जवळजवळ सारखे रा. सं. व सारखे आकार असणाऱ्या खनिजांच्या) माला असलेल्या आढळतात. असे प्रतिष्ठापन सहज होत असल्यामुळे कित्येक जातींचे रासायनिक संघटन अतिशय जटिल झालेले आहे.
अँफिबोल गटाच्या व ⇨पायरोक्सीन गटाच्या खनिजांच्या रासायनिक संघटनांत विशेषसा फरक नसल्यामुळे अँफिबोल गट हा पायरोक्सीन गटाचा बहुरूपक (रा. सं. तीच पण स्फटिकीय संरचना भिन्न असलेला) असा गट आहे, अशी कल्पना पूर्वी होती पण ती खरी नाही, असे अँफिबोलांचे क्ष-किरणांनी परीक्षण झाल्यावर कळून आले. अँफिबोलांच्या स्फटिकांच्या संरचनेत OH (हायड्रॉक्सिल) हा आवश्यक गट असतो व अँफिबोलांचे Si : O हे गुणोत्तर ४ : ११ असते. उलट पायरोक्सिनांचे तसेच गुणोत्तर १ : ३ असते. सिलिकॉन-ऑक्सिजन यांचे चतुष्फलक एकत्र जुळून तयार झालेल्या दोन एकेरी माला एकमेकींस जोडून तयार झालेली दुहेरी माला ही अँफिबोलांच्या स्फटिकांच्या संरचनेचे मौलिक एकक असते. चतुष्फलकांच्या दोन एकेरी मालांतील एक सोडून एक अशा चतुष्फलकांत ऑक्सिजनाचा एक अणू समाईक वाटला जाऊन ते जोडले गेल्यामुळे त्यांची दुहेरी माला तयार झालेली असते व त्यामुळेच Si : O गुणोत्तर १ : ३ होण्याऐवजी ४ : ११ झालेले असते. स्फटिकांच्या उभ्या अक्षाला समांतर असतील अशा रीतीने माला रचलेल्या असतात. दोन एकेरी माला धातूच्या आयनांनी बाजूच्या दिशेने जोडल्या गेलेल्या असतात व त्या दिशेची बंधक (बांधून ठेवणारी) प्रेरणा ही मालेच्या दिशेने असणाऱ्या Si–O चतुष्फलकांमधील बंधक प्रेरणेइतकी बलवान नसते. अँफिबोलांचे स्फटिक अक्षास समांतर वाढलेले, तंतूसारखे, काडीसारखे, किंवा प्रचिनासारखे असतात व प्रचिनाच्या फलकांस समांतर असे चांगले ⇨पाटन त्यांच्यात असते. हे गुणधर्म त्यांच्या वर उल्लेख केलेल्या आंतरिक संचरनेमुळे उद्भवलेले असतात. अँफिबोलांच्या संरचनेविषयी लक्षात घेण्यासारखी आणखी एक गोष्ट म्हणजे Si4O11 गटांच्या प्रत्येक जोडीच्या मध्ये सोडियमाचा एक अतिरिक्त अणू मावू शकेल अशा पोकळ जागा संरचनेत असतात.
रासायनिक संघटन : या गटातील सर्व जातींस लागू पडणारे सामान्य रासायनिक सूत्र (WXY)7-8(Z4O11)2 (O, OH, F)2 असे लिहिता येईल. या सूत्रातील W, X, Y, Z या सांकेतिक चिन्हांनी सारखीच किंवा जवळजवळ सारखीच आणवीय त्रिज्या असणारी मूलद्रव्ये दर्शविली जातात. W हे चिन्ह मोठे आयन असणाऱ्या Ca व Na व क्वचित अल्प प्रमाणात K या धातूंच्या आयनांसाठी, X हे अधिक लहान अशा Mg व Fe+2 व क्वचित Mn यांच्या आयनांसाठी, Y हे Fe+3, Ti व सहा सहसंयोजनाचे (जटिल संयुगातील केंद्रस्थानी असलेल्या अणुभोवतीच्या अणूंच्या वा गटांच्या संख्येचे) Al यांसाठी व Z हे Si व चार सहसंयोजनाच्या Al साठी वापरले जाते. वरील सामान्य सूत्रातील चिन्हांनी दर्शविलेल्या निरनिराळ्या अणूंचे प्रतिष्ठापन पुढे दिलेल्या मर्यादेत होऊ शकते.
(१) Si4O11 च्या साखळ्यांचे रासायनिक संघटन AlSi3O11 होईपर्यंत Si च्या जागी Al येऊ शकते. हे प्रतिष्ठापन खनिज निर्मितीच्या परिस्थितीवर अवलंबून असते. कमी तापमानात तयार होणाऱ्या अँफिबोलांपेक्षा उच्च तापमानात तयार होणाऱ्या अँफिबोलांत अधिक ॲल्युमिनियम असणे शक्य असते. (२) Fe+2 व Mg यांची अदलाबदल कोणत्याही प्रमाणात होऊ शकते. (३) एकूण (Ca, Na, K) शून्य किंवा जवळजवळ शून्याइतके किंवा २ ते ३ पर्यंत असतात. पण Ca दोनापेक्षा केव्हाही अधिक नसते व K हे अगदी अल्प असते. (४) OH व F यांची अदलाबदल कोणत्याही प्रमाणात होऊ शकते. (OH.F) जास्तीत जास्त २ असतात. O ने OH किंवा F यांची जागा घेतल्यामुळे ती दोनापेक्षा कमी होत असावीत.
वर वर्णन केल्याप्रमाणे प्रतिष्ठापन होण्याची शक्यता असल्यामुळे अँफिबोलांचे रासायनिक संघटन अतिशय जटिल असणे शक्य असते. रासायनिक संघटन व स्फटिकांच्या संरचना लक्षात घेऊन अँफिबोलांच्या पुढील पाच माला सामन्यतः केल्या जातात :
समचतुर्भुजी : अँथोफिलाइट माला (Mg,Fe)7(Si4O11)2(OH)2 : लोहापेक्षा मॅग्नेशियम अधिक.
एकनताक्ष : क्युमिंग्टनाइट माला (Fe, Mg)7(Si4O11)2(OH)2 : मॅग्नेशियमापेक्षा लोह अधिक.
ट्रेमोलाइट-ॲक्टिनोलाइट माला : Ca2(Mg,Fe)5 (Si4O11)(OH)2.
हॉर्नब्लेंड माला : Ca2Na0-1 (Mg, Fe, Al)5 [(Al, Si)4O11]2 (OH)2.
अल्कली-अँफिबोल माला : Na2(Mg,Fe, Al)5Si8 O22(OH)2.
अँथोफिलाइट माला : ही पायरोक्सीन गटातील एन्स्टॅटाइट हायपर्स्थीन या समचतुर्भुजी मालेशी समान अशी आहे. तिचे Mg : Fe हे गुणोत्तर ७ : ० ते १ : १ इतक्या मर्यादेत असते. कधीकधी त्यांच्या (Si4O11) या गटातील Si च्या जागी Al असू शकते. अँथोफिलाइटे फक्त रूपांतरित (बदललेल्या) खडकांत आढळतात.
क्युमिंग्टनाइट माला : पायरोक्सीन गटातल्या क्लिनोहायपर्स्थीनासारखी असलेली ही अँफिबोल गटातील माला आहे. या मालेतील खनिजांचे Mg : Fe हे गुणोत्तर ७ : ० ते १ : २ असे असते. काही मध्यम रासायनिक संघटना असणाऱ्या क्युमिंग्टनाइटांचे व तशाच अँथोफिलाइटांचे रासायनिक संघटन सारखेच असते. कधीकधी ती दोन्ही एकत्र आढळतात. क्युमिंग्टनाइटे ही फक्त रूपांतरित खडकांत आढळतात.
ट्रेमोलाइट-ॲक्टिनोलाइट माला : पायरोक्सीन गटात जशी डायोप्साइड-हेडेनबर्गाइट माला तशी ट्रेमोलाइट-ॲक्टिनोलाइट ही अँफिबोल गटातील माला आहे. ट्रेमोलाइट पांढरे असते व त्याच्यात लोह जवळजवळ नसते. Mg च्या जागी लोह येऊन लोहाचे प्रमाण वाढल्यावर खनिजाला हिरवा रंग येतो व त्याला
‘ॲक्टिनोलाइट’ म्हणतात. ही खनिजे रूपांतरित खडकांत आढळतात.
ट्रेमोलाइट-ॲक्टिनोलाइट मालेतील काही Mg च्या जागी फेरस (Fe+2) लोह व काही Mg च्या जागी Al व फेरिक (Fe+3) लोह ही येऊ शकतात. Si च्या काही अंशाच्या जागी Al येऊ शकते. खनिजात Ti व F हीसुद्धा असू शकतात. शिवाय Si4O11 गटाच्या प्रत्येक जोडीच्या मध्ये सोडियमाचा एक अतिरिक्त आयन येऊ शकतो. अशा सर्व प्रकारची प्रतिष्ठापने होऊन हॉर्नब्लेंड माला तयार होते. अँफिबोल गटातील हॉर्नब्लेंड हे पायरोक्सीन गटातील ऑजाइटासारखे आहे. परंतु ऑजाइटाच्या मानाने त्याचे रासायनिक संघटन अतिशय जटिल व परिवृत्तिशील (बदलणारे) असते व त्याचे निरनिराळे रासायनिक संघटन व भौतिक गुणधर्म असणारे अनेक प्रकार आढळतात. त्यांपैकी सर्वसामान्य अशा प्रकारांना ‘सामान्य’ किंवा ‘हिरवे हॉर्नब्लेंड’ म्हणतात. सामान्य हॉर्नब्लेंड हे हॉर्नब्लेंड सुभाजा (सहज भंग पावणारा खडक) व अँफिबोलाइट यांचे आवश्यक खनिज असून इतर रूपांतरित खडकांतही आढळते. डायोराइट व सायेनाइट यांसारख्या पातालिक (भूपृष्ठाच्या खूप खोल जागी असणाऱ्या) व अँडेसाइटासारख्या काही ज्वालामुखी खडकांतही ते आढळते. दाबाखाली स्फटिकीभवन होत असताना हॉर्नब्लेंडाला आवश्यक असलेला (OH) मिळण्यास परिस्थिती अधिक अनुकूल असते. म्हणून ज्वालामुखी खडकांच्या मानाने पातालिक खडकांत ते अधिक सामान्य असलेले आढळते. हॉर्नब्लेंडाचा गडद तपकिरी रंगाचा, ‘बेसाल्टी हॉर्नब्लेंड’ नावाचा एक प्रकारही आहे.
अल्कली-अँफिबोल माला : हॉर्नब्लेंडातील Ca चे Na ने अंशतः किंवा पूर्ण प्रतिष्ठापन होऊन या मालेची खनिजे तयार झालेली असतात, असे म्हणता येईल. त्यांच्यात Ca पेक्षा Na अधिक असते. या मालेतील प्रमुख खनिजे म्हणजे ग्लॉकोफेन Na2 Mg3 Al2 Si8 O22 (OH)2 व रीवेकाइट Na3Fe3+2Fe3+3Si8O22(OH)2 ही होत. त्या दोहोंचा रंग निळा असतो. ग्लॉकोफेन फक्त रूपांतरित खडकांत व रीवेकाइट हे रूपांतरित खडकांत व बराच सोडा असलेल्या ग्रॅनाइटात किंवा रायोलाइटात किंवा तशाच इतर अग्निज खडकांत आढळते.
संदर्भ : Berry, L. G. Manson, B. Mineralogy, Tokyo, 1961.
केळकर, क. वा.
