अल्कोहॉल : Kuhl, Koh’l अगर Kohol (म्हणजे ‘अतिसूक्ष्म चूर्ण’) या अर्थाच्या अरबी शब्दापासून ‘अल्कोहॉल’(Alkohol) हा शब्द तयार झाला, असे मानण्यात येते. अल्कोहॉल हा शब्द सौंदर्यप्रसाधनांत वापरल्या जाणाऱ्या अँटिमनी सल्फाइडाच्या अतिसूक्ष्म चूर्णासाठी पूर्वी वापरता तसेच तो शब्द इतर पदार्थांच्या अतिसूक्ष्म चूर्णांसाठी वापरत असत. तदनंतर त्याचा ‘अर्क’ या अर्थाने वापर करण्यात येऊ लागला. १६ व्या शतकानंतर ‘अल्कोहॉल’ हा शब्द वाइन ‘स्पिरिट’ साठी वापरण्यास सुरुवात झाली. नेहमी वापरात असलेले अल्कोहॉल हे सामान्यतः एथिल अल्कोहॉल असते. सर्व मद्यांमध्ये के कमीजास्त प्रमाणात असते.
रासायनिक दृष्ट्या अल्कोहॉलाची व्याख्या पुढीलप्रमाणे करतात : ज्यांच्यात एक किंवा अधिक हायड्रॉक्सिल(OH) गट आहेत अशा पॅराफिनी व ॲलिसायक्लिक [→ ॲलिसायक्लिक संयुगे] हायड्रोकार्बनांच्या अनुजातांना (एका संयुगापासून बनविलेले दुसरे संयुग) ‘अल्कोहॉल’ म्हणतात. ॲरोमॅटिक [→ ॲरोमॅटिक संयुगे] हायड्रो-कार्बनांच्या वलयातील कार्बनाला एक किंवा अधिक हायड्रॉक्सिल गट जोडलेले असले म्हणजे त्या संयुगांचे गुणधर्म अल्कोहॉलांहून बरेच वेगळे असतात व त्यांना ‘फिनॉले’ म्हणतात. पण ते हायड्रॉक्सिल गट जर वलयाच्या बाजूच्या शाखेला जोडलेले असले, तर त्यांचे गुणधर्म अल्कोहॉलांसारखे असून त्यांचा समावेश अल्कोहॉलात केला जातो. उदा., बेंझिल अल्कोहॉल C6H5-CH2OH. (अशा संयुगांना ॲलिफॅटिक अल्कोहॉलांचे अनुजात मानण्यात येते). एकच हायड्रॉक्सिल गट असणाऱ्या अल्कोहॉलांना मोनोहायड्रिक, दोन असणाऱ्यांना डायहायड्रिक, तीन असणाऱ्यांना ट्रायहायड्रिक व चार किंवा अधिक असणाऱ्यांना पॉलिहायड्रिक अल्कोहॉले म्हणतात. मोनोहायड्रिक अल्कोहॉले म्हणजे सजातीय संयुगांची एक मालाच असून तिच्यातील संयुगांचे सर्वसामान्य सूत्र CnH2n+1 OH असे (किंवा अल्किल गटाच्या जागी R घालून R.OH असे) असते.
अल्कोहॉलांना नाव देण्याच्या अनेक पद्धतींपैकी मुख्य म्हणजे (१) अल्कोहॉलाशी अनुरूप अशा हायड्रोकार्बनाच्या नावातील मूळ शब्दास‘इल’ हा प्रत्यय व अल्कोहॉल हा शब्द जोडून उदा., मिथेनापासून मिथिल अल्कोहॉल किंवा (२) त्या हायड्रोकार्बनाच्या नावास ‘ऑल’ प्रत्यय जोडून उदा., मिथेनापासून मिथेनॉल. (३) मिथिल अल्कोहॉलाला ‘कार्बिनॉल’ हे नाव दिले जाते व इतर अल्कोहॉले ही कार्बिनॉलाचे अनुजात आहेत असे मानून त्यानुसार नावे दिली जातात (पहा : कोष्टक क्र.१ )
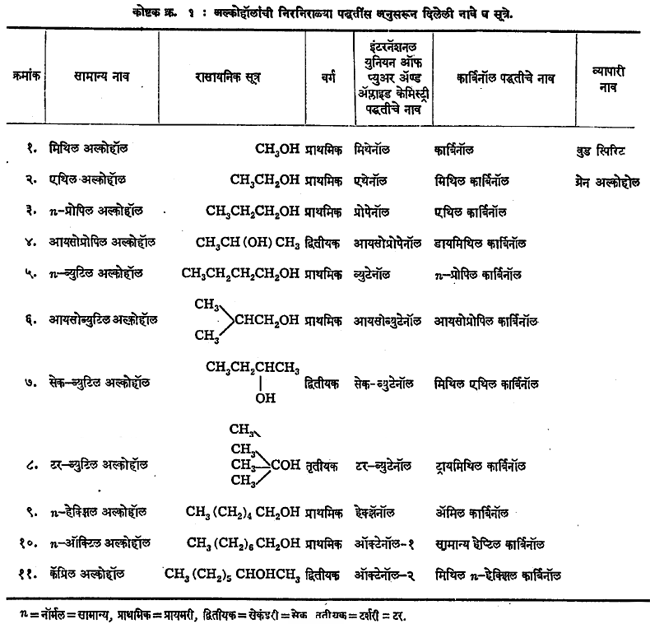
(४) मिथिल अल्कोहॉलाला ‘वुड स्पिरिट’ (लाकडापासून काढलेले स्पिरिट) यासारखी सामान्य भाषेतील नावेही कधीकधी वापरतात. महत्त्वाच्या अशा अल्कोहॉलांची निरनिराळ्या प्रमुख पद्धतींस अनुसरून दिलेली नावे व सूत्रे कोष्टक क्र. १ मध्ये दिलेली आहेत.
मिथिल किंवा एथिल अल्कोहॉलांचा एकेकच प्रकार असतो. पण प्रोपिल अल्कोहॉलाचे (C3H7OH) दोन व ब्युटिल अल्कोहॉलाचे (C4H9OH) चार भिन्न भिन्न संरचना (अणूंची मांडणी) असणारे समघटक (सारखेच घटक असलेले परंतु निरनिराळे गुणधर्म व संरचना असणारे पदार्थ) असू शकतात व अल्कोहॉलांतील कार्बनांची संख्या वाढत गेली म्हणजे समघटकांची संख्याही वाढत जाते. अल्कोहॉलांतील OH चे स्थान लक्षात घेऊन त्यांचे प्राथमिक (प्रा. = प्रायमरी), द्वितीयक (सेक.= सेकंडरी) आणि तृतीयक (टर.= टर्शरी) असे तीन वर्ग केले जातात. त्यांच्यातील भेद खाली दाखविलेल्या ब्युटिल अल्कोहॉलांच्या चार संरचनांच्या उदाहरणावरून कळून येईल.

वरील संरचनांतील n-ब्युटिल व आयसोब्युटिल अल्कोहॉलांतील OH गट ज्याला जोडला गेला आहे त्या कार्बन अणूला दोन हायड्रोजन अणू सरळ जोडलेले आहेत. प्राथमिक अल्कोहॉलातील OH चे स्थान असे असते. म्हणजे त्यांच्यात -CH2OH हा अल्कोहॉली गट असतो. द्वितीयक अल्कोहॉलातील OH ज्याला जोडलेला असतो त्या कार्बन अणूला एकच हायड्रोजनअणू सरळ जोडलेला असतो. उदा., द्वितीयक ब्युटिल अल्कोहॉल. द्वितीयक अल्कोहॉलात = CH(OH) हा अल्कोहॉली गट असतो. तृतीयक अल्कोहॉलातील OH गट ज्याला जोडलेला असतो त्या कार्बन अणूला कोणताच हायड्रोजन सरळ जोडलेला नसतो. तृतीयक अल्कोहॉलात ≡ C(OH) हा अल्कोहॉली गट असतो. OH च्या भिन्न भिन्न स्थानांमुळे या अल्कोहॉलांचे गुणधर्मही भिन्न असतात.
गुणधर्म : अल्कोहॉलांच्या मालेतील नीच स्थान असणारी अल्कोहॉले रंगहीन द्रव व उच्च स्थान असणारी पांढरी व घन असतात. नीच अल्कोहॉलांना विशिष्ट प्रकारचा वास व जळजळीत चव असते. उच्च अल्कोहॉले जवळजवळ वासरहित असतात. समघटकी अल्कोहॉलांपैकी प्राथमिक अल्कोहॉलांचा क्वथनांक (उकळबिंदू) सर्वांत अधिक व तृतीयकांचा सर्वांत कमी असतो. नीच अल्कोहॉले पाण्यात विरघळतात. त्यांचे विद्राव उदासीन (अम्ल व क्षारक या दोहोंचेही गुणधर्म नसणारे, → अम्ले व क्षारक) असतात. रेणुभार (रेणूतील अणूंच्या अणुभारांची बेरीज, →रेणुभार) वाढत जाण्याबरोबर विद्राव्यता (विरघळण्याची क्षमता) कमी होत जाते व सेटिल अल्कोहॉलासारखी (C16H33OH) अल्कोहॉले पाण्यात विरघळत नाहीत. विद्राव्यता ही काही अंशी संरचनेवरही अवलंबून असते. उदा. n-ब्युटिल अल्कोहॉल हे पाण्यात मध्यम प्रमाणात विरघळते, पण तृतीयक ब्युटिल अल्कोहॉल कोणत्याही प्रमाणात विरघळते.
विक्रिया : हॅलोजनी अम्ले, फॉस्फरस ट्राय- व पेंटा-हॅलाइडे, थायोनील क्लोराइड (SOCl2) इ. विक्रियाकारकांशी अल्कोहॉलांची विक्रिया घडवून आणून त्यांच्यातील OH गटाचे प्रतिष्ठापन (एक गट काढून तेथे दुसरा बसविणे) करता येते व त्यांची अल्किल हॅलाइडे{उदा., एथिल अल्कोहॉलापासून (C2H5OH)एथिल क्लोराइड (C2H5CI)}तयार करता येतात. अल्कोहॉलांची व कार्बनी (सेंद्रिय) किंवा अकार्बनी अम्लांची विक्रिया होऊन⇨एस्टरे तयार होतात. अल्कोहॉले व सोडियम किंवा पोटॅशियम यासारख्या तीव्र विद्युत् धन (धन आयन उत्पन्न करण्याची प्रवृत्ती असलेल्या) धातू यांची विक्रिया होऊन OH गटातील H विमुक्त (मोकळा) होतो व सोडियम किंवा पोटॅशियम याची अल्कॉक्साइडे, उदा., एथिल अल्कोहॉलापासून C2H5ONaकिंवा C2H5OK, तयार होतात. ती विद्युत् संयोगी (एका अणूकडून दुसऱ्या अणूकडे इलेक्ट्रॉन जाऊन तयार झालेली) असतात. (उदा., सोडियम अल्कॉक्साइडाचे सूत्र RO-Na+असे लिहावे लागेल. येथे+ आणि- ही चिन्हे अनुक्रमे इलेक्ट्रॉन मिळाल्याची व गमावल्याची निदर्शक आहेत).
अल्कोहॉलांची ऑक्सिडीकारकांशी [→ ऑक्सिडीभवन] होणारी विक्रिया भिन्न भिन्न प्रकारची असते. प्राथमिक अल्कोहॉलांच्या ऑक्सिडीभवनाने प्रथम ⇨आल्डिहाइड व नंतर आल्डिहाइडांचे ऑक्सिडीभवन होऊन अम्ल मिळते. त्या आल्डिहाइडात व अम्लात असणाऱ्या कार्बन अणूंची संख्या मूळच्या अल्कोहॉलाच्या कार्बन अणूंइतकीच असते.
द्वितीयक अल्कोहॉलांच्या ऑक्सिडीभवनाने ⇨कीटोन तयार होते. त्या कीटोनातील कार्बनांची संख्याही मूळच्या अल्कोहॉलाच्या इतकीच असते. उदासीन किंवा क्षारकीय (अम्लाशी विक्रिया झाल्यास लवण देणाऱ्या) विद्रावात तृतीयक अल्कोहॉलांचे ऑक्सिडीभवन होत नाही. पण अम्लविद्रावात ते सहज होते व त्यांच्यापासून कीटोन व अम्ल यांचे मिश्रण तयार होते. त्या कीटोनातील किंवा अम्लातील कार्बन अणूंची संख्या मूळच्या अल्कोहॉलातील कार्बन अणूंपेक्षा कमी असते.
पुढील सूत्रांवरून या विक्रियांची कल्पना येईल : प्राथमिक
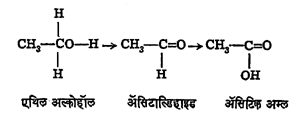
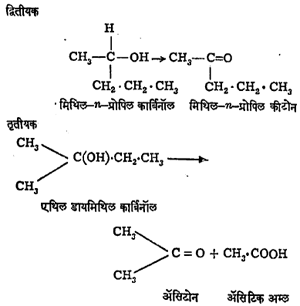
वर दिलेल्या विक्रियांवरून प्राथमिक, द्वितीयक व तृतीयक अल्कोहॉले ओळखता येतात.
कृती : अल्कोहॉले तयार करणाऱ्या कृतींपैकी सर्वांत जुनी म्हणजे नीरा, फळांचे रस इ. आंबवून म्हणजे त्यांचे किण्वन करून पिण्याची दारू करण्याची कृती होय. एथिल अल्कोहॉलाच्या उत्पादनासाठी ती अजूनही वापरली जाते. कार्बोहायड्रेटांचे किण्वन करून n- ब्युटिल व ॲमिल अल्कोहॉलांपैकी दोन अल्कोहॉले हीसुद्धा मिळविली जातात. त्यांशिवाय नैसर्गिक वायूतील (खनिज इंधन वायूतील) कार्बोहायड्रेटांचे ऑक्सिडीकरण करून किंवा कार्बन मोनॉक्साइडाचे ⇨ क्षपण करून, आल्डिहाइडांचे व कीटोनांचे क्षपण करून किंवा एस्टरांचे जलीय विच्छेदन करून (पाण्याबरोबर विक्रिया करून घटक वेगळे करून) अल्कोहॉले मिळविली जातात.
⇨ ग्रीन्यार विक्रिया वापरूनही अल्कोहॉले तयार करता येतात, पण व्यापारी उत्पादनांसाठी ती वापरली जात नाही. तथापि इतर पद्धतींनी न मिळू शकणारी प्राथमिक, द्वितीयक किंवा तृतीयक अल्कोहॉले तयार करण्यासाठी तिचा उपयोग होतो. वरील पद्धतींपैकी महत्त्वाच्या अशा पद्धतींची माहिती पुढे निरनिराळ्या अल्कोहॉलांच्या स्वतंत्र वर्णनात दिलेली आहे.
मोनोहायड्रिक अल्कोहॉले : या वर्गातील प्रमुख अल्कोहॉले म्हणजे मिथिल, एथिल, प्रोपिल, ब्युटिल, ॲमिल, कॅप्रिल, लॉरिल, बेंझिल, स्टिअरिल इ. होत. यांपैकी काही महत्त्वाच्या अल्कोहॉलांसंबंधी खाली माहिती दिली आहे. तसेच उच्च अल्कोहॉलांसंबंधी खाली माहिती दिली आहे. तसेच उच्च अल्कोहॉले हा परिच्छेदही पाहावा.
मिथिल अल्कोहॉल : CH3OH.(इतर नावे मिथेनॉल, कार्बिनॉल, वुड अल्कोहॉल आणि वुड स्पिरिट). रंगहीन द्रव, गोड वास, जळजळीत चव, पोटात गेले असता विषारी. याची ज्योत फिकट निळी असते. हे बरेच ज्वालाग्राही असून त्याची वाफ व हवा यांचे मिश्रण स्फोटक असते. त्याचे वि.गु. ०·७९२४ असून क्वथनांक ६४·७० से. व द्रवांक (वितळबिंदू) ९७·८० से. आहे.
मिथेनापासून मिथिल क्लोराइड व त्यापासून मिथिल अल्कोहॉल १८५८ साली बर्थेलॉट यांनी तयार केले. १९३० च्या सुमाराला कार्बन मोनॉक्साइड व हायड्रोजन याच्या संश्लेषणाने (कृत्रिम रीतीने) मिथिल अल्कोहॉल तयार करण्यात आले. हल्ली मिथिल अल्कोहॉलाचे बहुतेक उत्पादन कार्बन मोनॉक्साइड वा कार्बन डाय-ऑक्साइड किंवा दोन्ही व हायड्रोजन यांच्या मिश्रणाचे धातवीय ऑक्साइड उत्प्रेरक (विक्रियेत भाग न घेता विक्रियेची गती वाढविणारा पदार्थ) वापरून २५०-४००० से. तापमानास व उच्च दाबाखाली (१००-६०० वा. दा.) क्षपण करून करतात. नैसर्गिक वायूतील हायड्रोकार्बनांचे भागशः ऑक्सिडीकरण करून आणि लाकडापासून लोणारी कोळसा बनविताना मिळणाऱ्या पायरोलिग्नियस अम्लांपासून काही प्रमाणात मिथिल अल्कोहॉलाचे उत्पादन करतात. मिथिल या ग्रीक शब्दाचा अर्थ लाकूड किंवा दारू असा असून लाकडापासून तयार करतात म्हणून हे नाव दिले गेले.
याचे मुख्य उपयोग म्हणजे फॉर्माल्डिहाइडाच्या उत्पादनात मोटारीतील व विमानातील उष्णता प्रारणकामधील (एंजिनात निर्माण होणारी उष्णता काढून टाकणाऱ्या उपकरणामधील) शीतक माध्यमाचे गोठण्याचे तापमान खाली आणण्यासाठी मिथिल अमाइने, मिथिल क्लोराइड इ. रसायनांच्या संश्लेषणासाठी शाई, आसंजके (चिकटविण्याचे पदार्थ), काढून टाकावयाचे रंग इ. विरघळविण्यासाठी रॉकेटांचे व विमानांचे इंधन म्हणून एथिल अल्कोहॉल पिण्यास अयोग्य करण्यासाठी आणि नैसर्गिक वायूचे निर्जलीकरण करण्यासाठी हे होत.
एथिल अल्कोहॉल : CH3CH2OH.(इतर नावे एथेनॉल व मिथिल कार्बिनॉल). हे मानवाच्या उपयोगात असलेले सर्वांत जुने अल्कोहॉल आहे. रासायनिक संयुग म्हणून त्याचा शोध लागण्यापूर्वी, अगदी प्राचीन कालापासून आसवे, अरिष्टे, मद्य इ. स्वरूपांत त्याचा वापर करीत. हल्ली तो वरील स्वरूपात वापरतातच शिवाय रासायनिक उद्योगातही एक महत्त्वाचे रसायन म्हणून वापरतात.
गुणधर्म : रंगहीन, विशिष्ट सुगंध व जळजळीत चव असलेला जलशोषक, प्रवाही द्रव. पाण्यात सर्व प्रमाणात विद्राव्य. सर्व कार्बनी विद्रावकांत (विरघळविणाऱ्या पदार्थांत) तो मिसळतो. तो उत्तम विद्रावक आहे. तो ज्वालाग्राही असून त्याच्या ज्वलनाने फिकट निळ्या रंगाची ज्योत मिळते. ज्वलनाने त्याचे अपघटन (मूळ रेणूचे तुकडे पडून लहान रेणू अथवा अणू बनणे) होऊन कार्बन डाय-ऑक्साइड व पाणी ही तयार होतात. त्याच्या ज्वलनाने खूप उष्णता निर्माण होते, मात्र प्रकाश मिळत नाही. एथिल अल्कोहॉल व बाष्प किंवा हवा यांच्या मिश्रणाने स्फोटक मिश्रण तयार होते. क्वथनांक ७८·४० से., द्रवांक -११२·३० से. व प्रज्वलन तापमान (पदार्थ पेट घेण्यास लागणारे किमान तापमान) १८·३० से. आहे. पाणी व निर्जल अल्कोहॉल ही मिसळल्यास त्यांच्या मिश्रणाचे घनफळ हे मूळचे पाणी व अल्कोहॉल यांच्या घनफळाच्या बेरजेपेक्षा कमी असते. एथिल अल्कोहॉल उदासीन असते.
व्यापारी उत्पादन : ज्याच्यात साखर किंवा साखरेच्या रूपात आणता येतील अशी कार्बोहायड्रेटे आहेत अशा कोणत्याही पदार्थाचे किण्वन करून एथिल अल्कोहॉल तयार करता येते. अशा पदार्थांचे पुढील तीन गट करता येतील : (१) ऊस, बीट, सारखेच्या कारखान्यातील मळी, द्राक्षे, सफरचंदे, काजूची बोंडे, संत्री, अननस, मोहाची फुले इत्यादींतील साखरेचे सरळ अल्कोहॉलात रूपांतर करता येते. (२) धान्ये, बटाटे व स्टार्चयुक्त कंद किंवा मुळे यांच्यातील स्टार्चाचे माल्ट एंझाइम (जीव-रासायनिक विक्रियांत उत्प्रेरकाचे कार्य करणारा प्रथिनयुक्त पदार्थ) किंवा विशिष्ट बुरशीच्या विक्रियेने प्रथम जलीय विच्छेदन करून त्याचे किण्वनक्षम (आंबवण्यास योग्य) अशा शर्करांत रूपांतर करावे लागते व त्या शर्करांच्या किण्वनाने अल्कोहॉले मिळविता येते. (३) सेल्युलोजी पदार्थ : लाकूड, धान्यांची धाटे इ. भाग, भुस्सा यांच्यावर खनिज अम्लांची विक्रिया करून यांचे शर्करांत रूपांतर करावे लागते.
कोणत्याही रीतीने शर्करा तयार झाली म्हणजे यीस्ट या सूक्ष्मजीवामधील एंझाइमाने तिचे किण्वन करून एथिल अल्कोहॉल तयार करता येते. उदा., लाकडावर बऱ्याच दाबाखाली अम्लांची विक्रिया केल्यास त्याच्यातील सेल्युलोजाचे शर्करांत रूपांतर होते. एक टन लाकडापासून साधारणतः ९५% अल्कोहॉल असलेला १०५·५ लिटर एथिल अल्कोहॉल मिळतो. कागदाचा लगदा तयार करण्याच्या कारखान्यातील फुकट जाणाऱ्या सल्फाइड-द्रवात सेल्युलोज व अर्ध-सेल्युलोज यांचे जलीय विच्छेदन होऊन तयार झालेल्या शर्करा असतात.
स्वीडनमधील व अमेरिकेतील कारखान्यांतील अशा द्रवांपासूनही अल्कोहॉल मिळविले जाते परंतु ते शुद्ध नसते.
अशा अनेक प्रकारच्या पदार्थांपासून एथिल अल्कोहॉल तयार करता येत असले, तरी उत्पादन फायदेशीर होण्याच्या दृष्टीने वरीलपैकी काही थोडे पदार्थच वापरता येणे शक्य असते. मद्ये तयार करण्यासाठी धान्ये, बटाटे वा फळे वापरली जातात, पण ती महाग असल्यामुळे औद्योगिक उत्पादनासाठी त्यांचे उपयोग परवडत नाही व धान्याची टंचाई असल्यास ती वापरणेही इष्ट नसते. दुसऱ्या महायुद्धाच्या काळात मात्र त्यांचा उपयोग करण्यात आला.
भारतातील उत्पादन-पद्धती : भारतात एथिल अल्कोहॉलाचे जवळजवळ सर्व उत्पादन साखर कारखान्यातील मळीपासून (मोलॅसिसपासून) करतात. त्यासाठी मळी प्रथम विरळ करून तिच्यातील साखरेचे प्रमाण १० ते १३ टक्क्यांवर आणतात. या विद्रावात अल्प प्रमाणात अमोनियम सल्फेट व सल्फ्यूरिक अम्ल घालतात. अमोनियम सल्फेटामुळे यीस्टाच्या वाढीसाठी आवश्यक असणाऱ्या नायट्रोजनाचा पुरवठा होतो, तर सल्फ्यूरिक अम्लामुळे इतर जंतूंच्या वाढीस प्रतिबंध होतो. शिवाय विद्रावाच्या pH ची [→ पीएच मूल्य] पातळी चार-पाचच्या आसपास राहते. या किण्वनासाठी थोड्याशा अम्लतेची आवश्यकता असते. नंतर हा विद्राव मोठ्या लाकडी हौदात ओतून त्याच्यात विशिष्ट जातीच्या यीस्टाचा विद्राव घालतात. ही किण्वनाची क्रिया ऊष्मदायी (उष्णता उत्पन्न करणारी) असल्यामुळे हौदातील विद्रावाचे तापमान हळूहळू वाढू लागते. वाढत्या तापमानाचे नियंत्रण करण्यासाठी त्या हौदात नळ्यांमधून थंड पाणी खेळविण्याची सोय असते. किण्वन सुरू असताना हौदातील विद्रावाते तापमान ३६० से. च्या पुढे जाऊ दिले जात नाही किण्वन पूर्ण झाल्यावर त्या विद्रावाचे वि. गु. १·०२५-१·०२८ एवढे असते व त्यामध्ये एथिल अल्कोहॉलाचे प्रमाण सु. ५ ते ७ टक्के असते. या विद्रावाचे ऊर्ध्वपातन करून (वाफ करून व ती थंड करून) एथिल अल्कोहॉल वेगळे करतात. मळीच्या विद्रावाचे किण्वन होत असताना एथिल अल्कोहॉलाशिवाय ॲमिल, प्रोपिल, ब्युटिल यांसारखी इतर अल्कोहॉलेही तयार होत असतात व ऊर्ध्वपातन करताना ही अल्कोहॉले असेलला जो अंश मिळतो, त्याला
⇨फ्युझेल तेल म्हणतात.
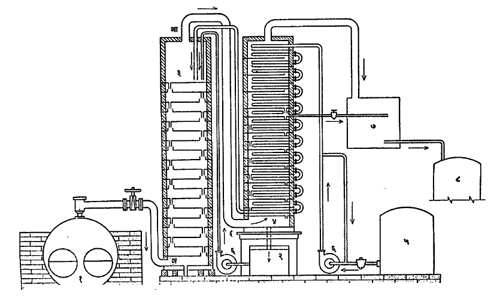
किण्वन केलेल्या विद्रावाचे ऊर्ध्वपातन :ऊर्ध्वपातनासाठी वापरल्या जाणाऱ्या ऊर्ध्वपातकांपैकी कॉफे यांच्या ऊर्ध्वपातकाचे (पहा आकृती) व त्याच्यात घडून येणाऱ्या क्रियांचे वर्णन येथे दिले आहे. या वर्णनावरून किण्वन केलेल्या विद्रावापासून एथिल अल्कोहॉल कसे मिळविले जाते हे कळून येईल. कॉफे-ऊर्ध्वपातकात एक विश्लेषक (घटक निराळा करणारा) व एक परिशोधक (ऊर्ध्वपातनाने द्रव्य शुद्ध करणारा) असे दोन स्तंभ असतात. प्रथम दोन्ही स्तंभ वाफेने भरावे लागतात, बाष्पित्रामधून (वाफ तयार करण्याच्या उपकरणामधून) वाफ डावीकडील विश्लेषक स्तंभाच्या तळाशी अ या ठिकाणाहून दाबाने आत घातली जाते. ती त्याच स्तंभाच्या वरच्या टोकापर्यंत पोहोचल्यानंतर आ या नळीवाटे परिशोधक स्तंभामध्ये इ येथे आत शिरते व स्तंभातून वर चढत जाते आणि नंतर वरच्या बाजूने बाहेर पडते. ह्या दोन्ही स्तंभांतील तापमान आवश्यक तितके झाले की, परिशोधक स्तंभाच्या वरीलबाजूकडील नळीतून किण्वन झालेला विद्राव पंपाच्या साहाय्याने त्याच्यात नेतात. हा विद्राव स्तंभामध्ये असलेल्या नागमोडी नळीतून खाली येत असताना त्याचे तापमान वाढत जाते. तो स्तंभाच्या खालील बाजूने नळीवाटे बाहेर नेऊन विश्लेषक स्तंभात त्याच्या वरच्या बाजूने आत सोडला जातो. या स्तंभात तांब्याचे सच्छिद्र पत्रे बसविलेले असतात. परिशोधक स्तंभातून येणारा किण्वन झालेला उष्ण विद्राव विश्लेषक स्तंभाच्या वरच्या भागातील पत्र्यावर प्रथम पडतो. तेथून तो हळूहळू व टप्प्याटप्प्याने खालील पत्र्यांवर पडू लागतो. याच स्तंभातील खालून वर जाणाऱ्या वाफेमुळे विद्रावातील अल्कोहॉलाचे बाष्पीभवन होते व ते स्तंभाच्या वरील बाजूकडे जाते.
ते बाष्प व वाफ ही वरील बाजूच्या नळातून बाहेर पडून परिशोधक स्तंभात त्याच्या खालच्या भागात इ येथून शिरतात व नंतर त्या स्तंभात वर चढत जातात. त्याच वेळी किण्वन झालेला विद्राव वरून खाली येत असतो व त्याच्यामुळे वर चढत जाणारी वाफ व अल्कोहॉलाचे बाष्प ही हळूहळू थंड होऊ लागतात. ती थंड होताना प्रथम जो भाग द्रवीभूत होतो तो मुख्यतः फ्युझेल तेल व अल्पसे एथिल अल्कोहॉल यांचा असतो. हा द्रव वेगळा काढून घेतला जातो. त्याला ‘फेंट’ असे म्हणतात. वाफ व अल्कोहॉलाचे बाष्प ही थोडी अधिक वर गेल्यावर त्यांचे तापमान अल्कोहॉलाच्या क्वथनबिंदूच्या थोडे खाली इतके झालेले असते. त्यामुळे अल्कोहॉलाचा द्रव तयार होतो व तो एका नळीच्या वाटे बाहेर नेऊन साठविण्यात येतो. स्तंभातून वर जाणाऱ्या वाफेत आल्डिहाइडा-सारखी जी अधिक बाष्पनशील संयुगे असतात त्यांचे द्रवीभवन होत नाही व ती परिशोधक स्तंभाच्या माथ्याकडील भागातून बाहेर नेली जातात. फ्युझेल तेलात थोडे एथिल अल्कोहॉल असते व ते तेल परत विश्लेषक स्तंभात नेले जाते आणि पुन्हा ऊर्ध्वपातन झाल्यावर त्याच्यातील एथिल अल्कोहॉल वेगळे मिळते.
किण्वन केलेल्या रसायनातील अल्कोहॉल वेगळे काढण्यासाठी कॉफे यांच्या ऊर्ध्वपातकाखेरीज इल्गे, बार्बेट इत्यादींनी शोधून काढलेले ऊर्ध्वपातक वापरले जातात. त्यांच्या कार्याचे स्वरूप कॉफे यांच्या ऊर्ध्वपातकासारखेच असते पण त्यांच्या रचनेच्या तपशिलात फरक असतो. असा अभिकल्प (आराखडा) असणाऱ्या ऊर्ध्वपातकांचा दुसऱ्या महायुद्धाच्या काळात भारतात उपयोग करण्यास सुरुवात झाली.
वरील प्रकारचे ऊर्ध्वपातक वापरून मिळणाऱ्या ऊर्ध्वपातित विद्रावात अल्कोहॉलाचे प्रमाण घनफळाच्या ९० ते ९५ टक्के (भाराच्या ८५·६ ते ९२·४ टक्के) इतकेच व उरलेले पाणी असते. त्याला ‘रेक्टिफाइड स्पिरिट’ म्हणतात. त्या विद्रावात चुनकळी घालून चोवीस तास ठेवतात व नंतर त्याचे ऊर्ध्वपातन करून अधिक अल्कोहॉल असलेला विद्राव मिळवितात. ९५·६ टक्के अल्कोहॉल व उरलेले पाणी यांचे मिश्रण हे ७८·१५० से. स्थिर क्वथनांकी (उष्णता दिली तरी तापमान वाढत नाही असे) मिश्रण असते व ते तसेच ऊर्ध्वपातित होते व पाणी आणि अल्कोहॉल वेगळी होत नाहीत.
ऊर्ध्वपातकापासून मिळणाऱ्या ऊर्ध्वपातित विद्रावापासून वर उल्लेख केलेल्या ‘चुनकळी’ –पद्धतीने शक्य तितके अधिक अल्कोहॉल असेलला विद्राव मिळविण्याची पद्धती व्यापारी उत्पादनासाठी परवडत नाही. अल्कोहॉलाचे व्यापारी प्रमाणात निर्जलीकरण करण्यासाठी यूसीन द मेल यांनी १९२३ साली शोधून काढलेल्या यंत्रसामग्रीचा उपयोग करतात. ९५% अल्कोहॉल असलेल्या विद्रावात बेंझीन घातले म्हणजे ६४·९० से. ला उकळणारे एक तृतीयक स्थिर क्वथनांकी मिश्रण तयार होते, असे सिडनी यंग यांनी केलेल्या प्रयोगांवरून दिसून आले (१९०३). या तत्त्वानुसार केवळ (निर्जल) अल्कोहॉलाचे मोठ्या व्यापारी प्रमाणात उत्पादन करणे शक्य झाले.
९५% अल्कोहॉल असलेल्या विद्रावात बेंझीन घालून त्याचे ऊर्ध्वपातन केले म्हणजे प्रथम ऊर्ध्वपातित झालेला विद्राव स्थिर क्वथनांकी व त्रिअंगी (तीन घटक संयुगे असणारे) मिश्रण असतो. त्याचा क्वथनांक ६४·९० से. व संघटन पाणी ७·४%, एथिल अल्कोहॉल १८·५% व बेंझीन ७४·१% असे असते. ऊर्ध्वपातनाने सर्व पाणी निघून गेल्यानंतर होणाऱ्या ऊर्ध्वपातनाने जो अंश मिळतो तो द्विअंगी (दोन घटक असलेले) स्थिर क्वथनांकाचे मिश्रण असतो. त्याचा क्वथनांक ६८·२० से. असून तो एथिल अल्कोहॉल ३२·४% व बेंझीन ६७·३% यांचे मिश्रण असतो. सर्व बेंझीन निघून गेल्यानंतर ७८·१० से. क्वथनांक असणारे शुद्ध अल्कोहॉल ऊर्ध्वपातित होते.
व्यापारी उत्पादनाच्या इतर पद्धती : एथिल अल्कोहॉलाचे व्यापारी उत्पादन करण्यासाठी पुढील पद्धतीही वापरल्या जातात.
(१)खनिज तेलाचे भंजन (तापवून व फोडून) करून मिळणारे एथिलीन हे सांद्र (९८%) सल्फ्यूरिक अम्लाने ७५-८०० से. तापमानात व १७·५८-३५·१६ किग्रॅ. चौ. सेंमी. इतक्या दाबाखाली शोषून घेतले जाईल असे करतात. यात होणाऱ्या विक्रियेमुळे एथिल हायड्रोजन सल्फेट व एथिल सल्फेट तयार होतात.
C2H4 + (HO)2SO2 → C2H5O · SO2 · OH
एथिलीन सल्फ्यूरिक अम्ल एथिल हायड्रोजन सल्फेट
C2H5 O·SO2·OH + C2H4 →(C2H5O)2SO2
एथिल हायड्रोजन सल्फेट एथिलीन एथिलीन सल्फेट
वरील विक्रियांनी तयार झालेल्या मिश्रणात सुमारे तितक्याच घनफळाचे पाणी घालतात व ते मिश्रण तापवितात. जलीय विच्छेदन होऊन एथिल अल्कोहॉल व काही थोडे डाय एथिल ईथर ही तयार होतात.
C2H5O·SO2·OH + H2O → C2H5OH + H2 SO4
एथिल हायड्रोजन सल्फेट पाणी एथिल अल्कोहॉल
(C2H5O)2 SO2 + 2H2O → 2C2H5OH + H2SO4
एथिल सल्फेट एथिल अल्कोहॉल
(C2H5O)2SO2 + C2H5OH → (C2H5)2O+C2H5O·SO2·OH
एथिल सल्फेट एथिल डाय एथिल एथिल
अल्कोहॉल ईथर हायड्रोजन सल्फेट
या पद्धतीत डाय एथिल ईथर हे उपफल म्हणून मिळते. पण ते अनावश्यक असल्यामुळे विक्रियेचे तापमान, जलीय विच्छेदनाची स्थिती इत्यादींवर नियंत्रण करून त्याचे प्रमाण शक्य तितके कमी केले जाते. जलीय विच्छेदन पूर्ण झाल्यावर त्या मिश्रणातील एथिल अल्कोहॉल हे भागात्मक ऊर्ध्वपातनाने वेगळे केले जाते. उरलेल्या सल्फ्यूरिक अम्लाची सांद्रता वाढवून त्याचा पुन्हा उपयोग केला जातो. या पद्धतीत सल्फ्यूरिक अम्लाचा पुष्कळ उपयोग केला जात असल्यामुळे सर्व यंत्रसामग्री व उपकरणे अम्लविरोधी असणे आवश्यक असते. वरील विक्रिया घडून येण्यासाठी काही कारखान्यांत लोह, मॅग्नेशियम, तांबे इ. धातूंची ऑक्साइडे उत्प्रेरक म्हणून वापरली जातात.
(२)एथिलीन व पाण्याची वाफ दाबाखाली उत्प्रेरकावरून नेऊन पुढील विक्रियेने एथिल अल्कोहॉल तयार केले जाते :
(३)ॲसिटिलिनापासून ॲसिटाल्डिहाइड तयार करतात आणि त्याची वाफ व हायड्रोजन यांचे मिश्रण निकेलाचे सूक्ष्म कण असलेल्या उत्प्रेरकांवरून, १००-१४०० से. तापमानात नेल्यावर
ॲसिटाल्डिहाइडाचे क्षपण होऊन एथिल अल्कोहॉल तयार होते.
अनेक देशांत एथिल अल्कोहॉल तयार करण्यासाठी किण्वन-पद्धतच वापरली जाते. परंतु दुसऱ्या महायुद्धानंतर अमेरिकेच्या संयुक्त संस्थानांत व यूरोपातील काही देशांत संश्लेषणाने तयार केलेल्या अल्कोहॉलाचे प्रमाण वाढत गेलेले आहे व १९५८ साली त्या देशांतील एथिल अल्कोहॉलाच्या एकूण उत्पादनाच्या ते ९०% होते. साखर कारखान्यातील मळी, धान्ये इत्यादींच्या किंमतीत वारंवार फेरफार होतात व त्यामुळे एथिल अल्कोहॉलाचे उत्पादन संश्लेषण-पद्धतीनेच करण्याची प्रवृत्ती वाढत आहे.
उपयोग : मद्य म्हणून एथिल अल्कोहॉलाचा उपयोग होतोच पण आधुनिक कालात त्याचा उपयोग रासायनिक वा इतर उद्योगधंद्यांत लागणारी संयुगे व सामान्य व्यवहारात किंवा युद्धात वापरल्या जाणाऱ्या शेकडो वस्तू तयार करण्यासाठी मध्यस्थ पदार्थ किंवा कच्चा माल म्हणून होतो. अशा कामासाठी दर वर्षी लाखो लिटर एथिल अल्कोहॉलाचा खप होतो व तो उत्तरोत्तर वाढतच आहे. त्याच्यापासून तयार करण्यात येणाऱ्या संयुगांपैकी सर्वांत जास्त महत्त्वाचे म्हणजे ॲसिटाल्डिहाइड होय.
त्याच्याशिवाय इतर महत्त्वाची संयुगे म्हणजे ब्युटाडाइन, ॲसिटिक अम्ल, एथिल क्लोराइड, एथिलीन डाय ब्रोमाइड व एथिल ईथर ही होत. एथिल अल्कोहॉल हे उत्कृष्ट व पाण्याच्या खालोखाल उपयोगी पडणारे विद्रावक आहे. गोठण्यास प्रतिबंधक म्हणूनही त्याचा उपयोग होतो. औषधे, अत्तरे, सौंदर्य-प्रसाधने, लाखेची पॉलिशे, प्लॅस्टिक व प्लॅस्टिककारी द्रव्ये, जंतुनाशके इ. बनविण्यासाठी ते वापरले जाते. इंधन म्हणूनही त्याचा उपयोग होतो. घनफळाने ५ ते २५% निर्जल अल्कोहॉल व पेट्रोल यांचे मिश्रण मोटारीचे इंधन म्हणून उपयुक्त ठरलेले आहे. फ्रान्स, पश्चिम जर्मनी, ऑस्ट्रिया, स्वीडन, ब्राझील इ. देशांत मोटारीसाठी अशा मिश्रणाचा उपयोग करतात. पेट्रोलाची टंचाई होती त्या वेळी भारतातही असे मिश्रण वापरले जात असे. अशा मिश्रणासाठी वापरल्या जाणाऱ्या अल्कोहॉलाला ‘पॉवर अल्कोहॉल’ म्हणतात.
बहुतेक देशांत पिण्याच्या दारूवर गेली कित्येक शतके कर बसविला जात आहे. त्या करापासून त्यांना बरेचसे उत्पन्न मिळत आलेले आहे. रासायनिक उद्योगधंद्यांत एथिल अल्कोहॉल उपयुक्त व कित्येक धंद्यांत अनिवार्य असल्यामुळे त्याच्यापासून बनविण्यात येणाऱ्या अनुजातांचे मूल्य अर्थात त्याच्या किंमतीवर अवलंबून असते व आंतरराष्ट्रीय स्पर्धेत टिकून राहण्यासाठी त्या अनुजातांची किंमत शक्य तितकी कमी असावी लागते. पिण्याच्या दारूवरील कराइतकाच कर औद्योगिक उत्पादनासाठी वापरल्या जाणाऱ्या एथिल अल्कोहॉलावर आकारल्यास त्याच्यापासून तयार केलेल्या वस्तू अर्थात अतिशय महाग पडतील, असे एकोणिसाव्या शतकाच्या मध्यासच दिसून आले होते. औद्योगिक उत्पादनासाठी वापरले जाणारे एथिल अल्कोहॉल करमुक्त करणारा कायदा प्रथम इंग्लंडात झाला. आधुनिक उद्योगधंदे चालू असलेल्या सर्वच देशांत औद्योगिक अल्कोहॉलाला कराच्या बाबतीत बरीच सवलत असते. पण ते पिण्यासाठी वापरले जाऊ नये या बाबतीत दक्षता घ्यावी लागते व त्यासाठी निरनिराळ्या सरकारी यंत्रणाची योजना केलेली असते.
कित्येक रासायनिक प्रयोगांसाठी व औषधे, सौंदर्य-प्रसाधने, स्वाददायक अर्क व खाद्यपदार्थ तयार करण्यासाठी शुद्ध एथिल अल्कोहॉल किंवा रेक्टिफाइड स्पिरिट आवश्यक असते. सरकारमान्य शिक्षणसंस्था, प्रयोगशाळा, रासायनिक कारखाने इत्यादींनाही ते आवश्यक असते. ते त्यांना करमुक्त किंवा सवलतीच्या दरात मिळू शकते. इतर कित्येक कामांसाठी कमी-अधिक भेसळ असलेले अल्कोहॉल चालू शकते. एथिल अल्कोहॉल पिण्यास अयोग्य व्हावे म्हणून, सहज वेगळी करता येणार नाहीत अशा द्रव्यांची भर त्यात घालून, ते करमुक्त किंवा करात सवलत देऊन पुरविले जाते. स्टोव्ह पेटविण्यासाठी व स्पिरिटच्या दिव्यासाठी वापरले जाणारे स्पिरिट हे अशा भेसळीचे असते. भेसळ असलेल्या व पिण्यास अयोग्य अशा अल्कोहॉलाला ‘विकृत अल्कोहॉल’ (डिनेचर्ड स्पिरिट) म्हणतात. निरनिराळ्या वस्तूंच्या (उदा., ॲसिटाल्डिहाइड, एथिल ईथर, बाह्यांगाला लावावयाची औषधे, पॉलिशे, साबण) व इतर निरनिराळ्या पदार्थांच्या उत्पादनासाठी निरनिराळ्या द्रव्यांची भेसळ असलेली विकृत अल्कोहॉले वापरली जातात.
कोणत्या पदार्थाच्या उत्पादनासाठी कोणती भेसळ असलेले विकृत अल्कोहॉल वापरावयाचे यासंबंधी सरकारी आदेश असतात. एथिल अल्कोहॉल किंवा मद्ये यांच्या उत्पादनावर व विनियोगावर तसेच त्यांच्या उत्पादनाचे व विक्रीचे हिशेब यांच्यावर कडक देखरेख असते. विकृत अल्कोहॉलाच्या विक्रीवर किंवा उपयोगावर तितकी बंधने नसतात. अमेरिकेसारख्या देशात ती नाममात्र आहेत. त्यांच्यावर कर नसतो किंवा असलाच तर उपेक्षणीय असतो.
एथिल अल्कोहॉलाचे मापन : एथिल अल्कोहॉलावरील कर हा एखाद्या ऊर्ध्वपातित द्रवातील अल्कोहॉलाचे प्रमाण किती आहे यावर अवलंबून असतो. ते प्रमाण कळल्यावर कर ठरविण्यात येतो. ते प्रमाण ठरविण्याची पद्धत अर्थात साधी सुटसुटीत व व्यापारी व्यवहारात सहज वापरता येईल अशी असावी लागते. दारूवरील कर ही महत्त्वाची उत्पन्नाची बाब असल्यामुळे अशी पद्धत शोधून काढण्याचे बरेच प्रयत्न पाश्चिमात्य देशांत झाले. १८ व्या शतकाच्या उत्तरार्धात ब्रिटनमधील क्लार्क यांनी तरकाटा (द्रवाचे विशिष्ट गुरुत्व काढण्याचे एक उपकरण) वापरून मद्यातील अल्कोहॉलाचे प्रमाण ठरविण्याच्या पद्धतीचा शोध लावला. तरकाटा मद्यात सोडल्यावर तो त्याच्यात किती बुडतो हे तरकाट्याच्या अंकावलीवरून (स्केलवरून) कळते व बुडण्याच्या मानावरून अल्कोहॉलाचे प्रमाण कळते. क्लार्क यांना १००% एथिल अल्कोहॉलाची माहिती नव्हती. त्यांचा तरकाटा, त्या काट्यावरील एक विशिष्ट खुणेपर्यंत ज्या अल्कोहॉलात बुडतो त्याला त्यांनी ‘प्रूफ’ असे नाव दिले. त्याच्यापेक्षा कमी अल्कोहॉल असणाऱ्या मद्यास‘अंडरप्रूफ’ व अधिक अल्कोहॉल असणाऱ्या मद्यास ‘ओव्हरप्रूफ’ अशी नावे दिली गेली. त्यानंतर सु. तीस वर्षांनी क्लार्क-तत्त्व वापरून पण अधिक चांगला तरकाटा तयार केला गेला. निरनिराळ्या तापमानांच्या व अल्कोहॉलाचे निरनिराळे प्रमाण असलेल्या जलीय द्रवांत हा तरकाटा किती बुडतो हे दाखविणारी कोष्टके तयार करण्यात आली. एखाद्या नमुन्याचे तापमान किती आहे व त्याच्यात तरकाटा किती बुडतो, हे पाहिल्यावर त्या कोष्टकांवरून त्याच्यातील अल्कोहॉलाचे प्रमाण चटकन कळते. साइक्स-तरकाटा १८१६ साली प्रथम वापरात आला व इंग्लंडात अजूनही तो वापरला जातो. साइक्स-पद्धतीस अनुसरून प्रूफ अल्कोहॉल म्हणजे १६० से. तापमान असताना ज्याच्या भाराने ४९·२९% किंवा घनफळाने ५२·१०% इतका शुद्ध अल्कोहॉल असतो तो विद्राव. प्रूफ हे मानक (संदर्भ-प्रमाण) मानून एखाद्या मद्यातील अल्कोहॉलाचे प्रमाण दिले जाते. प्रत्येक ०·५% अल्कोहॉल म्हणजे एक अंश, अशा हिशेबाने एखाद्या मद्यातील अल्कोहॉल प्रूफपेक्षा किती अंश कमी किंवा अधिक हे सांगितले जाते. उदा., ३० अंडरप्रूफ किंवा प्रूफचे अमुक अंश (उदा., ७० अंश) असे म्हणतात. शुद्ध १००% अल्कोहॉल ७५·३५ ओव्हरप्रूफ असते. अमेरिकेत प्रूफचे मूल्य किंचित वेगळे आहे. दशमान-पद्धती वापरणाऱ्या देशांत निराळे मानक वापरले जाते.
ब्रिटिशांपासून आलेली प्रूफ-पद्धतीच अद्यापि भारतात चालू आहे. साइक्स ए व साइक्स बी हे तरकाटे व ब्रिटिश सरकारने केलेली ६१० फॅ. ते १००० फॅ. तापमानात वापरावयाची कोष्टके वापरली जातात. कर आकारताना अल्कोहॉलाचे प्रमाण ठरविण्यासाठी वरील तरकाट्याची पद्धत वापरली जाते. ती अल्कोहॉल व पाणी यांच्या मिश्रणासाठीच वापरता येते. त्यांच्याशिवाय इतर काही द्रव्ये असली तर निराळ्या पद्धती वापराव्या लागतात.
प्रोपिल अल्कोहॉल : C3H7OH. पूर्वी उल्लेख केल्याप्रमाणे याचे दोन समघटक असतात :
(१) n-प्रोपिल अल्कोहॉल : CH3CH2CH2OH. (इतर नावे : प्रोपेनॉल व एथिल कार्बिनॉल). रंगहीनसुवासिक द्रव्य. क्वथनांक ९७·२० से. किण्वन-पद्धतीने एथिल अल्कोहॉल तयार करताना मिळणाऱ्या फ्युझेल तेलात हे असते. संश्लेषणाने मिथिल अल्कोहॉल तयार करताना हे उपफल (मुख्य पदार्थाबरोबर मिळणारा दुसरा पदार्थ) म्हणून मिळते. याचे व्यापारी उत्पादन पुढील विक्रियेद्वारे केले जाते :
Ni
CH ≡ C· CH2OH+2H2 → CH3 ·CH2· CH2OH
प्रोपार्गिल अल्कोहॉल n- प्रोपिल अल्कोहॉल
अलीकडे प्रोपार्गिल अल्कोहॉलाचे उत्प्रेरकांच्या सान्निध्यात क्षपण करून ते मिळविण्यात येऊ लागले आहे. पाणी , एथिल अल्कोहॉल व ईथर यांमध्ये ते मिसळते. सौंदर्यप्रसाधन-निर्मितीत व प्रोपिऑनिक अम्ल बनविण्यासाठी ते वापरतात.
(२) आयसोप्रोपिल अल्कोहॉल : (CH3)2·CH·OH.(इतर नावे : आयसोप्रोपेनॉल व डायमिथिल कार्बिनॉल). खनिज तेलाचे भंजन करून मिळणाऱ्या वायूतील प्रोपिलीन (CH3-CH=CH2) वायू सांद्र सल्फ्यूरिक अम्लात घेऊन, मिळणाऱ्या एस्टराचे जलीय विच्छेदन करून व्यापारी उत्पादन केले जाते.
या प्रक्रियेत डायआयसो प्रोपिल ईथर हे उपफल म्हणून मिळते. त्याचा ऑक्टेन-अंक (ऑक्टेन मिसळून इंधनाला दिलेला विशिष्ट अंक) ९८ असून विस्फोटविरोधी (मोटार एंजिनाच्या इंधनात विस्फोट टाळण्यासाठी मिश्रण करण्यात येणारे, → अंतर्ज्वलन-एंजिन) द्रव्य म्हणून त्याचा उपयोग केला जातो.
रंगहीन द्रव. क्वथनांक ८२·४० से. पाणी, एथिल अल्कोहॉल व ईथर यांमध्ये मिसळते. एस्टरे, ॲसिटोन व कीटोन तयार करण्यासाठी विद्रावक म्हणून व उच्च ऑक्टेनी इंधन तयार करण्यासाठी त्याचा उपयोग होतो.
ब्युटिल अल्कोहॉल : C4H9OH. याचे चार समघटक आहेत.
n-ब्युटिल अल्कोहॉल : CH3CH2CH2CH2OH. (इतर नावे : ब्युटेनॉल व n–प्रोपिल कार्बिनॉल). याचे व्यापारी उत्पादन ॲसिटाल्डिहाइडापासून संश्लेषणाने करतात.

स्टार्चाचे किंवा साखरेच्या कारखान्यातील मळीचे क्लॉस्ट्रिडियम ॲसिटोब्युटिलिकम नावाच्या सूक्ष्मजीवाने किण्वन करूनही n-ब्युटिल अल्कोहॉल बनवितात. व्हाइट्समान यांनी १९११ साली शोधून काढलेल्या या प्रक्रियेत ॲसिटोन व n–ब्युटिल ॲल्कोहॉल तयार होतात.
आयसोब्युटिल अल्कोहॉल : (CH3)2CH·CH2OH.(इतर नावे : आयसो-ब्युटेनॉल, आयसोप्रोपिल कार्बिनॉल). संश्लेषणाने मिथिल अल्कोहॉल बनविताना उपफल म्हणून हे मिळते. क्वथनांक १०८० से.
सेक.-ब्युटिल अल्कोहॉल : CH3CH2CH(OH).CH3. (इतर नावे : सेक.-ब्युटेनॉल, मिथिल एथिल कार्बिनॉल). खनिज तेलाच्या भंजनाने मिळणाऱ्या १-किंवा २-ब्युटिनापासून तीव्र सल्फ्यूरिक अम्लाची विक्रिया व जलसंयोजन करून (पाण्याच्या अणूबरोबर संयोग करून) याचे व्यापारी उत्पादन केले जाते.
क्वथनांक १००० से. ब्युटेनोन व एस्टरे व लॅकर पदार्थांचे (लॅकर्स) विद्रावक तयार करण्यासाठी याचा उपयोग करतात.
टर.-ब्युटिल अल्कोहॉल : (CH3)3-C-OH. (इतर नावे : टर.-ब्युटेनॉल व ट्रायमिथिल कार्बिऩॉल). खनिज तेलाच्या भंजनाने (तापवून अपघटन करून खालच्या रेणूंची संयुगे करणे) मिळविलेल्या आयसोब्युटिनाचे जलसंयोजन करून म्हणजे संश्लेषणाने टर.-ब्युटिल अल्कोहॉल तयार केले जाते.
द्रवांक २५·५० से. क्वथनांक ८३० से. याचा उपयोग मुख्यतः क्षार (सोडियम, पोटॅशियम इ. अल्कली मूलद्रव्यांची क्षारके) तयार करण्यासाठी केला जातो.
ॲमिल अल्कोहॉले : C5H11OH. याचे आठ समघटक असून ते सर्व ज्ञात आहेत.
क्वथनांक
(१) n- ॲमिन अल्कोहॉल CH3CH2CH2CH2CH2OH
१३८० से.
(२) आयसोॲमिल अल्कोहॉल (CH3)2 CHCH2CH2OH
१३०० से.
(3) क्रियाशील ॲमिल अल्कोहॉल CH3CH2 .CH(CH3)CH2OH
१२८० से.
(४) निओपेंटिल अल्कोहॉल (CH3)3 C.CH2OH
११३० से.
(५) पेंटेन-२-ऑल CH3CH2 CH2CH(OH)CH3
१२०० से.
(६) पेंटेन-३-ऑल CH3CH2 CH(OH)CH2CH3
११७० से.
(७) ३.मिथिल ब्युटेन-२-ऑल (CH3)2CH·CH(OH)·CH3
११४० से.
(८) २.मिथिल ब्युटेन-२-ऑल (टर.ॲमिल अल्कोहॉल)
(CH3)2C(OH)CH2·CH3 १०२० से.
फ्युझेल तेलात असणाऱ्या तीन ॲमिल अल्कोहॉलांपैकी मुख्य म्हणजे आयसोॲमिल व क्रियाशील ॲमिल अल्कोहॉल ही होत. n-ॲमिल अल्कोहॉलही अल्पसे असते. कृत्रिम सुगंधी द्रव्ये व अर्क बनविण्यासाठी लागणारी एस्टरे वरील तीन अल्कोहॉले असलेल्या मिश्रणापासून बनविली जातात.
n- ॲमिल अल्कोहॉल हे एथिल अल्कोहॉलाच्या मानाने अधिक मादक व अधिक विषारी असते. किण्वनात त्याच्या जोडीने तयार झालेले समघटकही प्रकृतीस अपायकारक असतात. किण्वनक्षम अशा शर्करांपासून ही अल्कोहॉले तयार होत नाहीत. परंतु धान्ये, बटाटे इ. ज्या स्टार्चांचे किण्वन केले जाते, त्यांच्यात नेहमी असणाऱ्या प्रथिनांपासून ती तयार होतात.
‘पेंटॅसॉल’ या व्यापारी नावाचा एक विद्रावक लॅकर व्हर्निशाच्या उद्योग-धंद्यात मोठ्या प्रमाणात वापरला जातो. तो सहा ॲमिल अल्कोहॉलांचे मिश्रण असतो.
फुरफुरील अल्कोहॉल : (२-फ्यूरेन कार्बिनॉल). रंगहीन द्रव. पाणी व कार्बनी विद्रावकांत विद्राव्य. हवेशी संबंध आल्यास त्याचा रंग तपकिरी-काळा होतो व विद्राव्यता कमी होते.  द्रवांक -१४·६३० से. क्वथनांक १७०० से. उत्प्रेरकाच्या साहाय्याने फुरफुराल्डि-हाइडापासून संश्लेषणाने त्याचे उत्पादन केले जाते. त्याच्यापासून बनविलेल्या रेझिनांचा उपयोग बऱ्याच उद्योगधंद्यांत केला जातो.
द्रवांक -१४·६३० से. क्वथनांक १७०० से. उत्प्रेरकाच्या साहाय्याने फुरफुराल्डि-हाइडापासून संश्लेषणाने त्याचे उत्पादन केले जाते. त्याच्यापासून बनविलेल्या रेझिनांचा उपयोग बऱ्याच उद्योगधंद्यांत केला जातो.
डायहायड्रिक अल्कोहॉले : या वर्गातील सर्वांत महत्त्वाचे अल्कोहॉल म्हणजे एथिलीन ग्लायकॉल होय. पोटॅशियम परमँगॅनेटाच्या सौम्य क्षारकीय विद्रावातून एथिलिनाचे बुडबुडे जाऊ देऊन ते तयार करता येते.
त्याचे व्यापारी उत्पादन एथिलिनापासून पुढील रीतीने केले जाते :
क्लोरीन असलेल्या पाण्यातून एथिलीन जाऊ दिल्यावर एथिलीन क्लोरोहायड्रिन तयार होते. त्याचे सोडियम कार्बोनेटाच्या
CH2 — CH2
क्लोरोहायड्रिन | | तयार होते. त्याचे सोडियम कार्बोनेटाच्या
OH CI
पाण्यातील विद्रावाने जलीय विच्छेदन करून ग्लायकॉल मिळते.
गुणधर्म : एथिलीन ग्लायकॉल हे रंगहीन व तेलासारखे दाट असून त्याची चव गोड असते. पाण्यात व एथिल अल्कोहॉलात ते सर्व प्रमाणात मिसळते. त्याचे गुणधर्म मोनोहायड्रिक अल्कोहॉलांसारखे असतात. परंतु त्याच्या दोन गटांपैकी एकाची क्रिया अगोदर व दुसऱ्याची मागाहून घडविता येते. त्यामुळे त्याच्यापासून सोडियमाचा एक किंवा दोन अणू असलेली मोनो- व डाय-सोडियम ग्लायकोलेटे यांसारखी संयुगे किंवा मोनो- किंवा डाय-एस्टरे तयार करता येतात.
उपयोग : एथिलीन ग्लायकॉल मुख्यतः पॉलिएस्टर रेझिने व पॉलिएस्टर तंतू तयार करण्यासाठी, तसेच मोटारीतील व विमानातील उष्णता प्रारणकामधील शीतक माध्यमाचे गोठण्याचे तापणान खाली आणण्यासाठी वापरतात. या वर्गातील इतर अल्कोहॉले म्हणजे प्रोपिलीन ग्लायकॉल, ट्राय एथिलीन ग्लायकॉल इ. ग्लायकॉले होत.
ट्रायहायड्रिक अल्कोहॉले : या वर्गातील महत्त्वाचे अल्कोहॉल म्हणजे ग्लिसरॉल किंवा ग्लिसरीन हे होय.
[CH2OH.CH(OH).CH2OH]ग्लिसरॉलाच्या रेणूत दोन प्राथमिक व एक द्वितीयक अल्कोहॉल-गट असतात व त्या दोन्ही गटांचे गुणधर्म ग्लिसरॉलात आलेले असतात. ग्लिसरॉलातील एकाच किंवा दोन किंवा तीनही अल्कोहॉली गटांशी कार्बनी अम्लांची विक्रिया होते व ⇨एस्टरे तयार होतात. त्यांना ‘ग्लिसरॉइडे’ म्हणतात.
वनस्पतिज व प्राणिज तेलांत व वसेत (चरबीत) आढळणारी काही (उदा., पामिटिक, स्टिअरिक, ओलेइक इ.) अम्ले व ग्लिसरॉल यांची एस्टरे निसर्गात आढळतात व त्यांच्या जलीय विच्छेदनाने ग्लिसरॉल तयार होते. साबण तयार करताना ही अम्ले क्षारांबरोबर उकळली म्हणजे त्यांचे जलीय विच्छेदन होऊन ग्लिसरॉल हे उपफल म्हणून मिळते. उद्योगधंद्यांत ते पुरे पडत नाही, म्हणून अमेरिकेच्या संयुक्त संस्थानांत प्रोपिलिनापासून संश्लेषणानेही ग्लिसरॉल तयार केले जाते [ → ग्लिसरीन].
उच्च अल्कोहॉले : सहा किंवा अधिक कार्बनी अणू ज्यांच्या रेणूत असतात अशा अल्कोहॉलांना सामान्यतः ‘उच्च अल्कोहॉले’ म्हणतात. त्यांपैकी महत्त्वाची म्हणजे CnH2n+1OH असे सामान्य सूत्र असणारी अल्कोहॉले होत. त्यांच्यापैकी कित्येकांची एस्टरे चरबी, तेले, मेणे इत्यादींत आढळतात. C12H25OH किंवा त्याच्या खालची अल्कोहॉले सामान्य तापमानात द्रव असतात पण त्याच्यावरची अल्कोहॉले घन असतात. उच्च अल्कोहॉले पाण्यात जवळजवळ किंवा पूर्णपणे अविद्राव्य असतात.
नैसर्गिक पदार्थांत एस्टरांच्या रूपात आढळणाऱ्या काही उच्च मोनोहायड्रिक अल्कोहॉलांसंबंधी कोष्टक क्र. २ मध्ये माहिती दिली आहे.

उच्च वसाम्लांच्या एथिल किंवा ग्लिसरील एस्टरांचे उत्प्रेरकांच्या साहाय्याने क्षपण करून कित्येक उच्च अल्कोहॉलांचे व्यापारी उत्पादन आता केले जाते. त्यांपैकी मुख्य म्हणजे लॉरिल (C12H25OH), मिरिस्टिल(C14H29OH), पामिटिल (C16H33OH) व स्टिअरिल (C18H37OH) अल्कोहॉले ही होत. या अल्कोहॉलांची RO.SO2.ONa या सामान्य सूत्राची सोडियम अल्किल सल्फेटे तयार करून ती पृष्ठक्रियाशील विक्रियक (पाण्यात विरघळविण्यास पृष्ठताणात बदल घडवून आणणारे पदार्थ), पायसकारक (एकमेकांत न मिसळणाऱ्या दोन द्रवांचे मिश्रण म्हणजे पायस स्थिर ठेवणारा पदार्थ), आर्द्रताकारक, कीटकनाशक,
कवकनाशक पदार्थ म्हणून वापरली जातात. या सोडियमी लवणांना खूप फेस येतो व त्यांच्यावर कठीण पाण्याचा परिणाम होत नाही म्हणून साबणाऐवजी ती वापरली जातात. उदा., शांपू बनविण्यासाठी सोडियम लॉरिल सल्फेट (C12H25SO4Na) बरेच वापरले जाते. संश्लेषणानेही उच्च मोनोहायड्रिक अल्कोहॉले तयार केली जातात. उच्च पॉलिहायड्रिक अल्कोहॉले सैद्धांतिक दृष्ट्या उच्च पॅराफिनांतील हायड्रोजनांचे प्रतिष्ठापन करून चार, पाच किंवा सहा OH असलेली अल्कोहॉले करता येणे शक्य आहे. तथापि संश्लेषणाने ती तयार करण्यात अनेक अडचणी आहेत. पण नैसर्गिक पदार्थांत तशी अल्कोहॉले आढळलेली आहेत. उदा., कित्येक दगड-फुलांत (लायकेन) व काही सागरी शैवलांत एरिथ्रिटॉल CH2OH.CHOH.CHOH.CH2OH)आढळते. मॅनात (म्हणजे ॲश वृक्षाच्या वाळलेल्या रसात) ‘मॅनिटॉल’ नावाचे सहा OH असणारे घन अल्कोहॉल सापडले आहे. त्याचे सूत्र CH2(OH).(CHOH)4.CH2(OH) असे आहे. तसेच सूत्र असणारे ‘सॉर्बिटॉल’ व‘डल्सिटॉल’ या नावाने मॅनिटॉलाचे दोन प्रकाशीय समघटक [→ समघटकता] निसर्गात आढळलेले आहेत.
अतृप्त अल्कोहॉले : तृप्त अल्कोहॉलांप्रमाणे अतृप्त (काही संयुजा मुक्त असलेले, àसंयुजा) अल्कोहॉलेही असतात. एथिलीन किंवा ॲसिटिलीन आणि कार्बोनिल संयुगे यांच्या विक्रिया करून अतृप्त मोनोहायड्रिक व डायहायड्रिक (ग्लायकॉल) अल्कोहॉले तयार करतात. फॉर्माल्डिहाइड वापरल्यास प्राथमिक अल्कोहॉले आणि इतर आल्डिहाइडे किंवा कीटोने वापरल्यास अनुक्रमे द्वितीयक व तृतीयक अल्कोहॉले मिळतात. व्हिनिल अल्कोहॉल (CH2=CHOH) हे तयार करणे अवघड आहे. ॲलिल अल्कोहॉल(H2C= CHCH2OH) हे लसणीच्या तेलात सापडते. ते रंगहीन, उग्र वासाचे व पाण्यात विद्राव्य आहे. प्रोपार्गिल अल्कोहॉल (HC≡C.CH2OH) रंगहीन, बाष्पनशील व जिरॅनियमाच्या वासासारखा वास असणारा द्रव आहे. त्याचा उपयोग औषधांत करतात. क्रोटिल अल्कोहॉल (CH3CH=CHCH2OH) रंगहीन द्रव असून पाण्यात कमी विद्राव्य आहे. व्हिनिल एथिलीन अल्कोहॉले धातू, काच, प्लॅस्टिक इत्यादींसाठी उपयोगी आसंजके (चिकटविणारे पदार्थ) तयार करण्यासाठी वापरतात. सिट्रोनेलॉल, जिरॅनिऑल, नेरॉल, फायटॉल, फार्नेसॉल यांसारखी अतृप्त अल्कोहॉल ⇨बाष्पनशील तेलांत आढळतात. त्यांना टर्पिन अल्कोहॉले म्हणतात. त्यांचा उपयोग सुगंधी द्रव्यांच्या व्यवसायात केला जातो.
भारतीय उद्योग : भारताच्या जकात मंडळाच्या अहवालानुसार १९४७ च्या सुमारास भारतात १९ कारखाने (६०,००० किलोलिटर क्षमतेचे) विविध प्रकारची अल्कोहॉले बनवीत होते. १९६५ मध्ये ६० कारखाने (२,७५,००० किलोलिटर क्षमतेचे) निर्मिती करीत होते. त्यांपैकी ३७ कारखाने साखर कारखान्यांशी जोडलेले होत. डायरेक्टर जनरल ऑफ टेक्निकल डेव्हलेपमेंटच्या अहवालानुसार १९७२ साली ६५ कारखाने (३,१२,००० किलोलिटर क्षमतेचे) अल्कोहॉले निर्मिती करीत होते.
पहा : औद्योगिक सूक्ष्मजीवशास्त्र मद्य.
संदर्भ : 1. Beyer, H. Organic Chemistry,London, 1963.
2. C.S.I.R. The Wealth of India-Industrial Products,Vol. I,New Delhi,1948.
3. Fieser, L. F. Fieser, M. Organic Chemistry, Bombay, 1962.
4. Finar, I. L.Organic Chemistry, 2 Vols.,London, 1962.
5.Thorpe, J. F. Whiteley, M. A. Thorpe’s Dictionary of Applied Chemistry, Vol. I,London, 1966.
फडके, ग. ह. मिठारी, भू. चिं. ठाकूर, अ.ना.