सिलिकोने : कृत्रिम रीतीने बनविलेला म्हणजे संश्लेषित द्रव्यांचा गट. ही द्रव्ये घन, द्रव, वायू व द्रायू (द्रव आणि वायू) या रुपांत असतात. सिलिकोन ग्रीज, रबर वा फेनक्षम चूर्ण असू शकते. व्यापारी सिलिकोने ही द्रायू, रबरे व रेझिने यांचे विविध प्रकार असतात. उष्णतेमध्ये स्थिर राहणाऱ्या, जलप्रतिसारक आणि सिलिकॉन अणूला जोडलेल्या कार्बनी मूलकाच्या बहुवारिकांच्या गटाला ‘सिलिकोने’ म्हणतात. पॉलिसिलोक्झेन हे याचे रसायनशास्त्रातील तांत्रिक नाव आहे. चिकटविणारा पदार्थ (अभिलागी) असलेले डायमिथिल सिलिकोन हे या गटातील एक सामान्य सिलिकोन आहे. निसर्गात आढळणाऱ्या कोणत्याही द्रव्यापेक्षा सिलिकोने वेगळी असतात. तेले, प्लॅस्टिके किंवा रबरे यांसारखी कार्बनी द्रव्ये आणि वाळू, काच व क्वॉर्ट्झ खनिज यांसारखी अकार्बनी द्रव्ये यांच्या संकरातून सिलिकोने तयार होतात. ऑक्सिजनानंतर सिलिकॉन हे भूकवचातील सर्वांत विपुल असणारे मूलद्रव्य असून सिलिकॉन हे सिलिकोनांमधील महत्त्वाचे मूलद्रव्य आहे. त्यावरुनच सिलिकोन हे नाव आले आहे. सिलिकोन अंशतः कार्बनी असले, तरी कार्बनी द्रव्याचे वैशिष्ट्य असणारे कार्बन हे मूलद्रव्य सिलिकोनांच्या संरचनेच्या कण्यात नसते. सिलिकोनांच्या शृंखलेत सिलिकॉन व ऑक्सिजन यांचे अणू एकाआड एक असतात आणि प्रत्येक सिलिकॉन अणूला कार्बनी गट थेट जोडलेला असतो. सिलिकॉन अणूंचे वलय बनले असल्यास त्या संयुगाला वलयी सिलिकोन म्हणजे सायक्लो सिलोक्झेन म्हणतात. सर्वसाधारणपणे बहुसंख्य सिलिकोनांमध्ये मिथिल (–CH3) व फिनिल (–C6H5) हे दोन कार्बनी गट असतात.
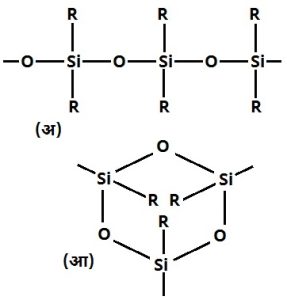
गुणधर्म : एखादे द्रव्य किती उष्णतेला, वातावरणक्रियेला व कालप्रभावनाला (मुरविण्याच्या काळाला) टिकून राहते, हे त्यातील अणू एकत्र बांधून ठेवणाऱ्या बंधांच्या बलाने निश्चित होते. उष्णतेत स्थिर राहण्याच्या व वातावरणक्रियेला विरोध करण्याच्या बाबतींत सिलिकोने ही कार्बनी द्रव्यांच्या तुलनेत अनेकपट चांगली असतात. वाळू , काच व क्वॉर्ट्झ यांच्याप्रमाणे सिलिकोनांच्या संरचनेचा सांगाडा सिलिकॉन व ऑक्सिजन यांचे अणू एकाआड एक असलेल्या शृंखलेचा वा वलयाचा असतो. या शृंखलेतील दुवे बळकट असतात. कार्बनी रेणू धरुन ठेवणाऱ्या दोन कार्बन अणूंमधील बंधाच्या बलापेक्षा सिलिकॉन व ऑक्सिजन यांच्या अणूंधील बंध दीडपट बळकट असतो.
सिलिकोने बनविताना कार्बनी गटांसह असलेल्या सांगाड्यावरील इतर द्रव्यांमुळे सिलिकोनांना जलप्रतिसारकक्षमता, वंगणक्षमता, नम्यता (लवचिकता) व हाताळण्यातील सुलभता हे उपयुक्त गुणधर्म प्राप्त होतात.
तुलनात्मक दृष्ट्या साधी सिलिकोने नितळ व पातळ द्रव असतात. मात्र सिलिकोनातील शृंखला जशी अधिक लांब व शाखायुक्त होते तशी सिलिकोने अधिक श्यान (दाट) होतात. सिलिकोन रबरांमध्ये काही आडवे दुवे असलेल्या दीर्घ रेणवीय शृंखला असतात, तर सिलिकोन रेझिनांची रेणवीय संरचना बरीच गुंतागुंतीची असते.
सर्वसाधारणपणे उष्णता, आर्द्रता व इतर अनेक रसायनांची क्रिया यांना सिलिकोने तीव्र विरोध करतात. ती उत्कृष्ट विद्युत् निरोधक असतात. उष्णता, पाणी किंवा ऑक्सिडीकारक यांमुळे त्यांचे अपघटन होत नाही. तापमानाच्या विस्तृत पल्ल्यात त्यांचे हे गुणधर्म टिकून राहतात. त्यांचे हे स्थैर्य वा दृढता सिलिकेटी खनिजांच्या तोडीची असते. त्यांच्या रेणूंमधील हायड्रोकार्बन गटांवर त्यांचे तेल, ग्रिजे, शीतनके, अभिलागी, रबरे, रेझिने, एनॅमले, रंगलेप, जलरोधी द्रव्ये व फेसाचा निरास करणारी द्रव्ये इ. उपयोग अवलंबून असतात. सिलिकोने मानवी शरीरक्रियावैज्ञानिक दृष्ट्या अक्रिय असल्याने पर्यायी कृत्रिम अवयवांसाठीची द्रव्ये म्हणून ती अतिशय महत्त्वाची आहेत (उदा., वक्षात रोपित करावयाचे द्रव्य, हृदयाच्या झडपा वगैरे असे कृत्रिम भाग शरीरात कायमचे बसविता येतात). सिलिकोन रबर अतिशय कमी तापमानालाही लवचिक राहते हा त्याचा गुणधर्म मोलाचा आहे. मात्र त्याचे ताणबल कमी असल्याने चूर्णरुप सिलिकोने ते प्रबलित करतात.
सिलिकोन रेझिनांवर आर्द्रता, ऑक्सिजन, उष्णता व सूर्यप्रकाश यांचा अगदी अल्प परिणाम होतो. त्यांची चकाकी दीर्घकाळ टिकून राहते. तसेच त्यांच्या यांत्रिक व विद्युतीय गुणधर्मांवर तापमानाचा विशेष परिणाम होत नाही. त्यामुळे किमान व कमाल तापमानांच्या स्थितींत ती इतर रेझिनांहून श्रेष्ठ दर्जाची असतात.
सिलिकोनांचे प्रकार : व्यापारी सिलिकोनांचे द्रायू, रबरे, रेझिने इ. विविध प्रकार असून काहींचे वर्णन पुढे दिले आहे.
सिलिकोन द्रायू : अगदी भिन्न श्यानता असलेले तरल द्रव, दाट तेले व रबरासारखे डिंक अशा प्रकारची द्रायुरुप सिलिकोने उष्णतारोधी असून ती सहजगत्या जळत नाहीत. सामान्य कार्बनी द्रव्ये तयार करण्यासाठी लागणारी रसायने, पाणी व सभोवतालची परिस्थिती यांचा या सिलिकोनांवर थोडाच परिणाम होतो. तसेच सिलिकोनांचा प्लॅस्टिके, रबरे, रंगलेप, सजीव ऊतके व जीव यांच्यावर थोडाच परिणाम होतो किंवा होतही नाही. या सिलिकोनांचे गोठणबिंदू खूप कमी असून ती चांगली विद्युत् निरोधक, जलप्रतिसारक व पारदर्शक असतात.
द्रायू सिलिकोने स्वच्छ व धूररहित असल्याने ती ग्रिजांपेक्षा अधिक चांगली ठरतात. त्यांच्यामुळे टायर, इतर रबरी किंवा प्लॅस्टिक भाग उत्पादनाच्या वेळी साच्याला चिकटत नाहीत. मोटारगाड्या, फर्निचर, प्लॅस्टिक किंवा एनॅमलाचे पृष्ठभाग व चष्म्यांच्या काचा यांसाठीच्या मेणांमध्ये आणि पॉलिश करण्यासाठी वापरण्यात येणाऱ्या द्रव्यांमध्ये सिलिकोन द्रायू वापरतात. कापड व चामडे यांच्यावर सिलिकोन द्रायूंचे संस्करण करतात. त्यामुळे त्यांच्यामध्ये पाणी, शाई व टोमॅटोचा रस यांसारखे पाण्याशी निगडित पदार्थ शोषले जात नाहीत आणि त्यांचे डाग पडत नाहीत. अशा कापडाची धुलाई किंवा निर्जल धुलाई केली, तरी सिलिकोने निघून जात नाहीत. शिवाय सिलिकोनांमुळे कापड ताठर वा कडक होत नाही.
घड्याळे व गोलक धारवे यांच्यासाठी सिलिकोन तेले व ग्रिजे कायमचे वंगण म्हणून वापरतात. जलप्रतिसारक सिलिकोनांमुळे विटा व काँक्रीटच्या भिंती पावसात कोरड्या राहतात. स्नानगृहे व स्वयंपाक घरातील फरश्या जलाभेद्य करण्यासाठी सिलिकोने व्यापक प्रमाणात वापरतात.
नाजूक उपकरणांमध्ये संदमन द्रायू व आंदोलन निरोधक म्हणून सिलिकोन द्रायू वापरतात. हे द्रायू अधिक संपीडनक्षम (दाबले जाऊ शकणारे असल्याने) ते विमानाच्या अवतरण गिअरमध्ये वापरतात. सीलबंद करणारे द्रव्य म्हणून हे द्रायू वापरतात. विमानातील ठिणगी, गुडद्या, रेडिओ, आकाशक, क्ष-किरण सामग्री, स्विचे, सागरी एंजिनातील प्रज्वलन प्रणाली, उच्च तापमानात वापरावयाची धारित्रे व रोहित्रे यांमध्ये सिलिकोन द्रायू वापरतात. हे सिलिकोन सौंदर्यप्रसाधनांत व इलॅस्टोमर द्रव्यांत वापरतात. (इलॅस्टोमर हे रबर वा प्लॅस्टिक यांच्यासारखे द्रव्य असून, सर्वसाधारण तापमानाला कमी ताण लावून ते मूळ लांबीच्या दुप्पट ताणता येते आणि ताण काढल्यावर लगेचच ते जवळजवळ पूर्वीच्या लांबीचे होते).
सिलिकोन रबरे : उच्च रेणुभार असलेल्या सिलिकोनांचे व्हल्कनीकरण करुन ही रबरे तयार होऊ शकतात. ती नैसर्गिक रबरापेक्षा वेगळी ओळखणे अवघड असते. ती ताणली जातात आणि त्यांचा गोळा आपटल्यास तो वर उसळी घेतो. या रबरांच्या चादरी, नळ्या, नाजुक आकाराच्या विविध वस्तू व रबडीही बनविता येतात. सिलिकोन द्रायूंचे असाधारण गुणधर्म यांच्यातही असतात. अगदी कमी किंवा जास्त तापमानाला सिलिकोन रबर लवचिक राहते. काल, हवामान, पाणी, वीज तसेच बहुतेक अम्ले, अल्कली, लवणे व तेले यांचा सिलिकोन रबरांवर परिणाम होत नाही.
सिलिकोन रबर भट्टीच्या तापमानाला वितळत नाही, तसेच −७९° से. इतक्या कमी तापमानाला ते कठीण किंवा ठिसूळ होत नाही. म्हणून भट्टीची दारे, विमानाच्या व रणगाड्याच्या एंजिनांसंबंधीच्या दोलन पेट्या (रॉकर बॉक्स) सीलबंद करण्यासाठी तसेच धारित्रे व रोहित्रे यांतील मायणी (बुशिंग), स्वयंचलित प्रेषणातील तेल सीलबंद करणे व हवाबंद करणारी गॅस्केटे यांच्यासाठी सिलिकोन रबरे वापरतात. जहाजावरील संदेशवहनाच्या केबली आणि विशिष्ट विद्युत् चलित्रांतील वेटोळी व नाविक नियामक प्रणाली यांमध्ये विद्युत् निरोधनासाठी हे रबर वापरतात.
सिलिकोन रेझिने : या रेझिनांच्या जलप्रतिसारकक्षम व उष्णतारोधक या गुणधर्मांमुळे विद्युत् निरोधन व संरक्षक पुटे वा लेप यांमध्ये लक्षणीय प्रगती झाली. पुटांसाठीची ही रेझिने रंगलेप, व्हार्निश व एनॅमल यांमध्ये वापरतात. सिलिकोन रेझीनयुक्त रंगलेपाचे लेप २६०° ते ५४०° से. तापमानापर्यंत फुगत नसल्याने त्यांचे पापुद्रे निघत नाहीत. बाह्य हवामानामुळे यांचे रंग व चकाकी कमी होत नाहीत. हे रंगलेप जहाजावरील कामांसाठीही वापरतात. पटलनासाठीच्या (लॅमिनेशन करण्यासाठी असलेल्या) या रेझिनांमुळे कागद, कापड, ॲस्बेस्टस, फायबर ग्लास (काचेचे कापड) यांच्या बळकट आणि टिकाऊ चादरी बनविता येतात. त्या विद्युत् उद्योगात निरोधक म्हणून वापरतात. विमोचक (रिलीझ) सिलिकोन रेझिने अन्य द्रव्ये न चिकटणारे पृष्ठभाग तयार करण्यासाठी वापरतात. बेकरीतील पाव भाजण्यासाठीची तबके, इस्त्रीचे भाग इत्यादींवर यांची पुटे देतात. जलप्रतिकारक सिलिकोन रेझिनांमुळे बांधकामांत व काँक्रिटमध्ये पाणी शिरत नाही. साचेकामासाठी वापरण्यात येणारी ही रेझिने पटलन रेझिनांसारखी असतात. परंतु ही कागद व कापड यांऐवजी भरणद्रव्यांसाठी वापरतात. अतिशय नाजुक कामांसाठी लागणारे साचे बनविण्यासाठी ही वापरतात. स्विचे, विद्युत् गुडद्या, सॉकेट, इलेक्ट्रॉनीय सामग्रीचे भाग यांसाठी त्यांचा उपयोग होतो. विद्युत् निरोधनासाठी उपयुक्त सिलिकोन रेझिने उष्णता, ओझोन वायू व संक्षारक (रासायनिक झीज घडवून आणणारे) वातावरण यांमध्ये टिकून राहतात. यामुळे दीर्घकाळ टिकणारी उपकरणे तयार करता आली. याशिवाय वायूंच्या बाबतीत उच्च पार्यता हा पृष्ठीय गुणधर्म असल्यामुळे सिलिकोन रेझिनांचे अनेक उपयोग होतात.
टोकाची तापमाने व हवामानाची प्रतिकूल परिस्थिती यांमध्ये विशिष्ट उपयोगांसाठी खास प्रकारची सिलिकोन रेझिने तयार करतात. भट्ट्या व चुली यांचे भाग, धुराडी, तापनाचे नळ, निष्कास नळ, एंजिनाचे व टरबाइनांचे भाग, उच्च तापमानात वापरावयाची यंत्रसामग्री आणि उपकरणे यांना उष्णतारोधक सिलिकोन रंगलेप व व्हार्निश लावतात. बहुधा ही ॲल्युमिनियम रंगद्रव्यांबरोबर वापरतात.
मिथिल प्रतिष्ठापित सिलिकोन बहुवारिकांवर आधारलेले रंगलेप इमारतीच्या बाहेरच्या भिंतींना लावतात, कारण ते वातावरणक्रियेला विरोध करतात. यांच्यामुळे पृष्ठभाग जलप्रतिसारक होऊन आर्द्रतेपासून त्याचे संरक्षण होते. पुष्कळदा हे रंगलेप बांधकामाच्या संरक्षणासाठी वापरतात. कारण याच्यामुळे बांधकामाचा मूळ तजेला टिकून राहतो व त्यातील छिद्रे मोकळी राहतात.
सिलिकोन संसिक्त (मिश्रित) व्हार्निशे व रेझिने विद्युतीय यंत्रसामगी व प्रयुक्त्या यांचे संरक्षण करण्यासाठी उपयुक्त आहेत. विद्युत् चलित्रातील स्थात्याभोवतीची व विद्युत् जनित्रातील वेटोळी आणि रोहित्रातील गुंडाळ्या यांच्यावर यांचा लेप देतात. विद्युत् निरोधक सिलिकोनांमुळे खडतर कामांसाठी वापरण्यात येणारी विद्युत् चलित्रे, जनित्रे व रोहित्रे यांचा कार्यकाल दहा ते शंभरपट वाढतो आणि ती अधिक कार्यक्षमपणे कार्य करतात.
पहा : ग्रीन्यार विक्रिया; प्लॅस्टिक व उच्च बहुवारिके; रेझिने.
संदर्भ : 1. Arkles, B. Organosilicon Chemistry IV, 2000.
2. Brook, M. A. Silicon in Organic, Organometallic and Polymer Chemistry, 2000.
3. Paul, S. Surface Coatings Science and Technology, 1985.
4. Tomanek, A. Silicones and Industry : A Compendium for Practical Use, Instruction and Reference, 1991.
ठाकूर, अ. ना.