खनिजविज्ञान : खनिजांचे भौतिक गुणधर्म, रासायनिक संघटन, ती निसर्गात आढळण्याच्या रीती, त्यांना ओळखण्याच्या पद्धती, त्यांचे उपयोग इत्यादींचा विचार ज्या विज्ञानात केला जातो, त्याला खनिजविज्ञान म्हणतात. पृथ्वीवरील खडक बव्हंशी खनिजांचे बनलेले असतात. निरनिराळ्या खडकांतील खनिजे निरनिराळ्या प्रकारांची किंवा निरनिराळ्या प्रमाणात असतात. आपणास माहीत असलेली जवळजवळ सर्व खनिजे पृथ्वीवरील खडकांपासून, तर काही थोडीच पृथ्वीच्या बाहेरून उदा., अशनींपासून (पृथ्वीवर पोहोचणाऱ्या उल्केच्या खनिजयुक्त भागापासून) मिळतात.
खडकातून काढलेल्या सर्वच नैसर्गिक पदार्थांना सामान्य व्यवहारात खनिजे असे म्हणतात. पण शास्त्रीय परिभाषेतील खनिज या संज्ञेत जे पदार्थ सामान्यत: घन व समांग (एकजिनसी) आहेत, ज्यांचे रासायनिक संघटन काही विशिष्ट अशा रासायनिक सूत्राने दाखविता येण्यासारखे आहे, ज्यांची आंतरिक रचना स्फटिकी आहे आणि जे अजैव क्रियांनी निर्माण झाले आहेत त्यांचाच समावेश केला जातो.गार्, शेंदेलोण, संगजिरे, हरताळ (ऑर्पिमेंट), अभ्रक, सुवर्णमाक्षिक (पायराइट्स), हिंगूळ, हिरा, पुष्कराज (टोपॅझ) ही खनिजांची परिचित अशी उदाहरणे होत.
कित्येक सूक्ष्मकणी खडक (उदा., महाराष्ट्रात सर्वत्र आढळणारा बेसाल्ट) नुसत्या डोळ्यांनी पाहिले असता एकजिनसी दिसतात, पण त्यांची पातळ चकती किंवा चुरा सूक्ष्मदर्शकाने पाहिल्यावर ते दोन किंवा अनेक खनिजांचे बनलेले असल्याचे कळून येते. केवळ काही अगदी थोडे खडकच मुख्यत्वेकरून फक्त एकाच खनिजाचे बनलेले असतात. नैसर्गिक सोने, चांदी, तांबे, हिरा, ग्रॅफाइट, गंधक यासांरखी काही खनिजे एकाच मूलद्रव्याची बनलेली असतात पण अशी खनिजे विरळाच आढळतात. बहुसंख्य खनिजे दोन किंवा अधिक मूलद्रव्यांची रासायनिक संयुगे असतात. उदा., क्वॉर्ट्झ हे निसर्गात वारंवार आढळणारे खनिज सिलिकॉनाचा एक व ऑक्सिजनाचे दोन अणू मिळून तयार झालेले संयुग असते व त्याचे रासायनिक सूत्र SiO2 असे असते.
इतिहास : मानवाचा आधिभौतिक व बौद्धिक विकास हा नवनवीन खनिजांचा शोध आणि त्यांचा अधिकाधिक उपयोग यांच्याशी मोठ्या प्रमाणात निगडीत आहे. खनिजांच्या उत्पादनावर व पुरवठ्यावर राष्ट्राचे आर्थिक स्थैर्य बऱ्याच प्रमाणात अवलंबून असते. खनिजांचे महत्त्व इतके आहे की, त्यांच्याशिवाय उद्योगधंद्याचे पान हलत नाही. युद्धाच्या व शांततेच्या काळी अतिशय महत्त्वाच्या आणि गरजेच्या वस्तू, अस्त्रे, वाहने वगैरे अनेक गोष्टी खनिजांपासून बनवितात. त्यांचा उपयोग अगदी आवश्यक व अटळ असतो. काही खनिजे अतिशय महत्त्वाची व मोक्याची असतात.
एकोणिसाव्या शतकात इंग्लंडमध्ये झालेल्या औद्योगिक क्रांतीपासून खनिजांची मागणी पुष्कळ वाढली. त्यामुळे खनिजे शोधणे व त्यांचा उपयोग करणे हे कार्य फार मोठ्या प्रमाणात खऱ्या अर्थाने सुरू झाले. नवीन खनिजांचे शोध लागले. खनिजांचे विविध व नवीन उपयोग समजू लागले. खाणकामाच्या व इतर उद्योगधंद्यांची वाढ झपाट्याने होऊ लागली. खनिजांचे राष्ट्रीय महत्त्व पहिल्या जागतिक महायुद्धाच्या वेळेस प्रचितीला आले. यावेळी अमेरिकेसारख्या देशाला देखील युद्ध चालविण्यामध्ये अनेक अडचणी येऊ लागल्या. अन्न आणि इंधन पुरविणाऱ्या बोटी कमी पडू लागल्या, तसेच युद्धात वापरली जाणारी अस्त्रे व स्फोटक पदार्थही कमी पडू लागले. मग खनिजांचे महत्त्व, उपयोग, त्यांचा शोध व संशोधन यांवर राष्ट्रीय पातळीवर विचार सुरू झाला.
एच्. सी. सॉर्बी यांनी ध्रुवण सूक्ष्मदर्शकामध्ये सुधारणा करून त्याचा उपयोग खडकांच्या पातळ चकत्यांचे परीक्षण करण्यासाठी केला. पुढे ए. क्ल्वॉझो यांनी १८६७ साली सूक्ष्मदर्शक वापरून खनिजांच्या प्रकाशीय गुणधर्मांची पाहणी करून खनिजे ओळखण्याचे गुणधर्म निश्चित केले ही माहिती एकत्र करून एक सारणी (कोष्टक) तयार केली. यामुळे रूढ खनिजविज्ञानाचे नवे दालन उघडले गेले.
आधुनिक खनिजविज्ञानात ⇨इलेक्ट्रॉन विवर्तन, अवरक्त वर्णपटलेखन [वर्णपटातील तांबड्या रंगाच्या अलीकडील अदृश्य किरणांचे वर्णपटलेखन → वर्णपटविज्ञान]. न्यूट्रॉन विवर्तन, अणुकेंद्रीय चुंबकीय अनुस्पंदन [→ अनुस्पंदन], अणुकेंद्रीय व इलेक्ट्रॉन परिवलनी अनुस्पंदन इ. तंत्रांचा उपयोग खनिजे ओळखण्यासाठी आणि त्यांच्या स्फटिकांच्या आणवीय संरचना कशा आहेत ते ठरविण्यासाठी केला जातो. ही तंत्रे वापरून मिळविलेल्या माहितीवरून रूढ खनिजविज्ञानाच्या पद्धतींनी व क्ष-किरण विवर्तनाचे तंत्र वापरून मिळविलेल्या माहितीचा खरेखोटेपणा पडताळून अचूक माहिती मिळविता येणे शक्य झाले आहे. बऱ्याच वेळा पूवीच्या माहितीला दुजोरा मिळतो आणि त्या माहितीत भरही पडते. अशा रीतीने खनिजविज्ञानाची प्रगती सतत चालू आहे.
खनिजांची उत्पत्ती : निसर्गात आढळणारी खनिजे भूवैज्ञानिक प्रक्रियांनी तयार झालेली असतात. त्यामुळे त्यांच्या अध्ययनाने भूवैज्ञानिक प्रकियांबद्दल बरीच माहिती मिळते. बहुतेक सर्व खनिजे कुठल्या ना कुठल्या प्रकारच्या खडकात आढळतात. काही खनिजे कशी तयार होतात हे सहज समजते किंवा पाहता येते. उदा., समुद्राच्या पाण्याचे बाष्पीभवन होऊन साधे मीठ, जिप्सम यांसारख्या पदार्थांचे निक्षेप (साठे) तयार होतात. इतर प्रकारांनी खनिजे कशी तयार होतात हे समजणे जरा कठीण असते. खनिजे मुख्यत: पुढील प्रक्रियांनी तयार झालेली असतात. अग्निज खडकांतील – (१) बहुतेक सर्व खनिजे शिलारसात विरघळलेल्या स्थितीत असलेल्या द्रव्यांचे, तो निवून घन होत असताना स्फटिकीभवन होऊन तयार होतात (२) काही खनिजे शिलारसातून बाहेर पडणाऱ्या वाफांचे व वायूंचे संद्रवण (द्रवात रूपांतर) होऊन आणि गरम विद्रावांचे बाष्पीभवन किंवा संघनन (घनात रूपांतर) होऊन तयार होतात. अवसादी (गाळाच्या) खडकांतील – (१ ) बरीचशी खनिजे पूर्वीच्या खडकांतून वाहून आलेली असतात. अशी खनिजे न झिजणारी, कठीण आणि मजबूत असतात. उदा., क्वॉर्ट्झ, इल्मेनाइट, गार्नेट, झिर्कॉन (२) इलाइट, माँटमोरिलोनाइट, अभ्रके यांसारखी मृद्-खनिजे अगोदरच्या खडकांतून फुटून, तुटून, बारीक होऊन आलेली असतात पण नंतर त्यांचे रासायनिक प्रकियेने पुनर्घटन होते (३) नैसर्गिक पाण्यात विरघळलेल्या द्रव्यांचे उदा., हॅलाइट (मीठ), जिप्सम, पाण्याचे बाष्पीभवन होऊन निक्षेपण (साचण्याची क्रिया) होते (४) नैसर्गिक पाण्यातील कार्बन डाय-ऑक्साइड निघून गेल्यामुळे त्याच्यात विरघळलेले कॅल्शियम कार्बोनेट निक्षेपित होते (५) अवसादी खडकांत खनिजे तयार होण्यासाठी काही जैव पदार्थही हातभार लावतात. उदा., अवसादी गंधकाचे निक्षेप. रूपांतरित (बदल होऊन तयार झालेल्या) खडकांतील खनिजे दाब किंवा उष्णता किंवा या दोहोंच्या प्रभावामुळे खडकांचे घन अवस्थेत रूपांतरण होत असताना त्यांच्यातील घटकांचे पुनर्स्फटिकीभवन होऊन तयार होतात. उदा., अभ्रक, हॉर्नब्लेंड, गार्नेट, स्टॉरोलाइट इत्यादी. शिलारसातील उष्ण वाफ आणि क्रियाशील वायू शेजारच्या किंवा आसपासच्या खडकांत शिरले म्हणजे त्यांची त्या खडकांतील घटकांशी विक्रिया होऊन तोरमल्ली (टुर्मलीन), पुष्कराज, फ्ल्युओरस्पार इ. खनिजे तयार होतात. अगोदर असलेल्या खडकात बाहेरून काही द्रवरूप आणि वायुरूप पदार्थ शिरून प्रतिष्ठापनाच्या (एकाची जागा दुसऱ्या पदार्थाने घेण्याच्या) प्रक्रियेनेही काही खनिजे तयार होतात.
खनिजांचे व धातुकांचे बहुतेक निक्षेप जलतापीय (उच्च तापमानाच्या) विद्रावांतील निक्षेपण होऊन तयार होतात. चुनखडकातील कॅल्साइटाच्या शिरा, अवसादातील बराइट, गंधक इ. निक्षेप, बॉग लोह (मुख्यत्वे गोएथाइट, दलदलीच्या प्रदेशात पाण्याच्या संयोगाने तयार झालेले आयर्न ऑक्साइड) तसेच सिलिकेचे बरेच प्रकार भूमिजलातून निक्षेपित होतात. बहुतेक धातुक निक्षेप सापेक्षत: उच्च तापमानास तयार होतात. त्यांच्या सभोवार सामान्यत: रूपांतरणाने तयार झालेल्या भिन्न खनिजांचे पट्टे तयार झालेले असतात.
खनिजांची नावे : सैंधव, अभ्रक, सुवर्णमाक्षिक इ.सु. पाऊणशे खनिजांची नावे मराठी भाषेत रूढ आहेत. ती परंपरागत व प्राचीन काळापासून चालत आलेली आहेत. इंग्रजी व इतर यूरोपीय भाषांतही तशीच आणि सु. तेवढीच नावे आहेत. खनिजांच्या आधुनिक अध्ययनास सुरुवात होऊन उत्तरोत्तर नवीन खनिजे सापडत गेल्यावर त्यांचा शोध लावणाऱ्या वैज्ञानिकांनी त्यांना आपापल्या आवडीप्रमाणे नावे दिली. खनिजाचा प्रथम शोध लावणाऱ्याने दिलेले नावच वापरावयाचे असा संकेत आहे. आधुनिक खनिजविज्ञानाचा प्रारंभ व वाढ ही पाश्चिमात्य देशांत झाली आणि शास्त्रीय लिखाणात पाश्चिमात्यांनी दिलेली नावेच सर्व भाषांत वापरली जातात. त्यांपैकी पुष्कळशी नावे लॅटिन किंवा ग्रीक शब्दांवरून तयार केलेली आहेत. काही खनिजांना दोन किंवा क्वचित अधिक नावेही दिली जातात, त्यांपैकी एखादे त्या भाषेतील रूढ नाव असते. उदा., सुवर्णमाक्षिकाला इंग्रजीत पायराइट्स या शास्त्रीय नावाशिवाय ‘फूल्स गोल्ड’ म्हणजे मूर्खाचे सोने असे नावही दिले आहे.
बऱ्याचशा खनिजांच्या शास्त्रीय नावांचा शेवट आइट (किंवा इट) या अक्षरांनी (उदा., अल्बाइट, ब्रूकाइट, झिओलाइट) होतो. काही नावे व्यक्तींच्या नावांवरून (उदा., शीलाइट, स्मिथसोनाइट) तर काही भौगोलिक स्थानांच्या नावांवरून (उदा., लॅब्रॅडोराइट, व्हिस्यूव्हिअनाइट) दिली गेली आहेत. काही नावे खनिजाच्या भौतिक गुणधर्मावरून दिली गेलेली आहेत. उदा., मॅग्नेटाइट हे चुंबकीय (मॅग्नेटिक) असल्यामुळे त्यानुरूप व ॲझुराइट हे नाव त्या खनिजाच्या ॲझूर म्हणजे मोरचुदासारख्या निळ्या रंगावरून दिले गेले. स्टॅनाइट या खनिजात कथिल असते आणि कथिलाच्या लॅटिन नावावरून हे नाव दिलेले आहे. झिंकाइट, फ्ल्यूओराइट, मॉलिब्डेनाइट इ. नावेही खनिजातील एखाद्या रासायनिक मूलद्रव्यावरून दिलेली आहेत.
दोन हजारांहून अधिक खनिजे म्हणजे खनिजांच्या जाती आतापर्यंत माहीत झालेल्या आहेत आणि यापुढील काळात काही नवी खनिजे आढळतील, यात शंका नाही. पण खनिजांच्या वारंवार आढळणाऱ्या अशा सु. वीसच जाती आहेत व पृथ्वीच्या कवचाचा सु. ९८ टक्के भाग त्यांचा बनलेला आहे. सामान्य खडक हे त्या विसांपैकी एखाद्या किंवा एकापेक्षा अधिक जातींचे बनलेले असतात म्हणून त्या जातींना शैलकर किंवा शैलनिर्माती (खडक ज्यांचे बनलेले आहेत अशी) खनिजे म्हणतात. त्यांच्यापैकी सर्वांत महत्त्वाची म्हणजे फेल्स्पारे होत. फेल्स्पारांत पुढील जातींचा समावेश होतो : (१) पोटॅश फेल्स्पार (KAISi3O8), (२) अल्बाइट (NaAlSi3O8), (३) ॲनॉर्थाइट (CaAl2Si2O8), ॲनॉर्थाइटाने अल्बाइटाचे कोणत्याही प्रमाणात प्रतिष्ठापन होणे शक्य असते. अल्बाइटाचे उत्तरोत्तर अधिक प्रतिष्ठापन होत जाऊन तयार झालेल्या खनिजांना अनुक्रमे ऑलिगोक्लेज, अँडेसाइन, लॅब्रॅडोराइट, बायटोनाइट आणि अखेरीस ॲनॉर्थाइट अशी नावे आहेत. ही सर्व खनिजे मिळून तयार होणाऱ्या गटाला अल्बाइट-ॲनॉर्थाइट माला, प्लॅजिओक्लेज माला किंवा प्लॅजिओक्लेज फेल्स्पारे अशी नावे आहेत.
फेल्स्पारांच्या मानाने कमी महत्त्वाची अशी सिलिकेटी खनिजे म्हणजे कृष्णाभ्रक, पायरोक्सिने, अँफिबोले व ऑलिव्हिने ही होत. ती मुख्यत: Mg, Fe यांची किंवा Mg, Fe, Ca यांची किंवा वरील घटकांच्या जोडीस Al, Na किंवा K असणारी सिलिकेटे असतात. शुभ्र अभ्रक हे मुख्यत: K, Al व OH असलेले सिलिकेट असते.
खनिजांचे वर्गीकरण : खनिजांच्या वर्गीकरणाच्या अनेक पद्धती आहेत, त्यांपैकी सर्वांत सोयीची म्हणजे त्यांच्या रासायनिक संघटनावर आधारलेली पद्धती होय. केवळ मूलद्रव्यांच्या स्वरूपात असलेल्या खनिजांचा एक स्वतंत्र वर्ग केला जातो. रासायनिक संयुगांच्या स्वरूपात असणाऱ्या खनिजांचे त्यांच्यातील धनायनास (संयुगाच्या विद्रावात जो अणुगट ऋण विद्युत् भारित असतो व विद्रावात विद्युत् प्रवाह सोडला असता धन अग्राकडे जातो त्यास) अनुसरून वर्ग केले जातात. खनिजांच्या अत्यंत महत्त्वाच्या अशा वर्गांची व त्यांच्यातील काही खनिजांची नावे खाली दिली आहेत.
(१) मूलद्रव्यांचा वर्ग : याच्यात सोने, चांदी, तांबे, प्लॅटिनम, हिरा, ग्रॅफाइट, गंधक इ. सु. वीस खनिजांचा समावेश होतो. (२) सिलिकेटांचा वर्ग : हा वर्ग सर्वांत मोठा असून त्याच्यात फेल्स्पारे, अँफिबोले, पायरोक्सिने, अभ्रके इत्यादींचा समावेश होतो. (३) ऑक्साइडांचा वर्ग : क्वॉर्ट्झ, मॅग्नेटाइट, हेमॅटाइट, बॉक्साइट इत्यादी. (४) कार्बोनेटांचा वर्ग : कॅल्साइट, मॅग्नेसाइट (MgCO3), सीडेराइट, ॲरॅगोनाइट इत्यादी. (५) सल्फेटांचा वर्ग : बराइट (BaSO4), ॲनहायड्राइट इत्यादी (६) सल्फाइडांचा वर्ग : सुवर्णमाक्षिक, गॅलेना हिंगूळ इत्यादी.
रासायनिक संघटनास अनुसरून केलेल्या प्रत्येक वर्गाचे अनेक उपवर्ग किंवा गट करण्यात येतात व ते खनिजांच्या स्फटिकी संरचनेवर आधारलेले असतात. समान संरचना असणारी खनिजे एकाच गटात घालण्यात येतात. उदा., कार्बोनेटांच्या वर्गातील कॅल्साइट व ॲरॅगोनाइट ही दोन प्रमुख खनिजे आहेत. त्या दोहोंचे रासायनिक संघटन सारखेच म्हणजे CaCO3 आहे, पण त्यांचे स्फटिक भिन्न प्रकारचे म्हणजे पहिल्याचे समांतर षट्फलकीय व दुसऱ्याचे समचतुर्भुजी असतात म्हणून त्यांना निरनिराळ्या गटांत घालतात [→ स्फटिकविज्ञान]. उलट कॅल्साइट व मॅग्नेसाइट यांचे संघटन भिन्न असले, तरी त्यांची स्फटिकी संरचना सारखीच असल्यामुळे त्यांना एकाच गटात घालतात. त्याच कारणासाठी ॲरॅगोनाइट (CaCO3) व सेऱ्युसाइट (PbCO3) यांना एकाच गटात घालतात. सिलिकेटांच्या वर्गातील फेल्स्पारे, अभ्रके, अँफिबोले, पायरोक्सिने, ऑलिव्हिने इ. खनिजांचे गट हेही खनिजांच्या स्फटिकी संरचना लक्षात घेऊन केलेले आहेत.
अध्ययनाच्या सोयीसाठी खनिजविज्ञानाचे (१) स्फटिकविज्ञान, (२) भौतिक खनिजविज्ञान, (३) रासायनिक खनिजविज्ञान, (४) प्रकाशीय खनिजविज्ञान, (५) खनिज अभिज्ञान किंवा वर्णनात्मक खनिजविज्ञान, (६) क्रमिक सहजनन खनिजविज्ञान व (७) प्रायोगिक खनिजविज्ञान असे विभाग करण्यात येतात.
स्फटिकविज्ञान : सामान्यत: खनिजे घन असतात. खनिजाची प्रत्येक जाती ही विशिष्ट अशा रासायनिक घटकांची बनलेली असते. हे रासायनिक घटक म्हणजे निरनिराळ्या मूलद्रव्यांचे अणू व आयन (विद्युत् भारित अणू, रेणू वा अणुगट) पद्धतशीरपणे मांडले जाऊन खनिजांचे स्फटिक तयार होतात. घनावस्था ही मूलत: स्फटिकी असते. जे पदार्थ पूर्वी अस्फटिकी समजले गेले होते, त्यांपैकी बहुतेक सर्व अगदी सूक्ष्म स्फटिकांचे बनलेले म्हणजे गूढस्फटिकी असल्याचे दिसून आले आहेत. ठराविक रासायनिक संघटन व स्फटिकी संरचना यांवरून एखादे विशिष्ट खनिज म्हणजे त्याची जाती निश्चित ठरविता येते. या दोन गुणधर्मांची माहिती एखादे खनिज निश्चित ठरविण्यासाठी पुरेशी असते. कारण खनिजांचे इतर सर्व गुणधर्म तत्त्वत: या दोन्हींमुळेच निर्माण होतात. खनिजांतील घटक अणूंची मांडणी विशिष्ट साचा तयार होईल अशी नियमित असल्यामुळे वाढीस अनुकूल अशी परिस्थिती असली म्हणजे त्यांचे बाह्य आकारही नियमित होतात. कोणताही स्फटिक नैसर्गिक रीतीने तयार झालेल्या चार किंवा अधिक सपाट पृष्ठांनी मर्यादित झालेला असतो. या पृष्ठांना फलक, पैलू किंवा अनीक म्हणतात. फलकांचे आकारमान व संख्या ही कितीही लहान किंवा मोठी असोत, ते आडवे, तिरपे किंवा उभे असोत, त्यांची मांडणी स्फटिकांच्या आंतरिक संरचनेस अनुसरून व नियमबद्ध असते. खनिजांच्या स्वरूपाबद्दलची अगदी सुरुवातीची माहिती त्यांच्या स्फटिकांच्या बाह्य संरचनांवरून, उदा., पृष्ठांची मांडणी, निरनिराळ्या स्फटिक पृष्ठांमधील कोन, या कोनांचे संबंध, स्फटिकांचे ⇨ पाटन यांच्यावरून म्हणजे स्फटिकांच्या आकारविज्ञानाची पाहणी करून मिळाली. स्फटिकांच्या पद्धतशीर वाढीमुळे तयार झालेल्या त्यांच्या भूमितीय आकारांचा विचार स्फटिकविज्ञानात करण्यात येतो. खनिजे ओळखण्यासाठी त्यांच्या स्फटिकांच्या आकारविज्ञानाची माहिती फार उपयुक्त असल्यामुळे स्फटिकविज्ञानाचा विकास प्रामुख्याने खनिजवैज्ञानिकांनी केला. खनिजांच्या आधुनिक अध्ययनास सुरुवात झाल्यापासून स्फटिकांच्या पद्धतशीर अध्ययनाकडे लक्ष देण्यात आले आहे. या विज्ञानाच्या अभ्यासाच्या पद्धती भिन्न आहेत. या सर्व कारणांनी ते एक स्वतंत्र व महत्त्वाचे विज्ञान झाले असून त्याचा उपयोग भौतिकी, रसायनशास्त्र, धातुविज्ञान इ. विज्ञान शाखांत केला जातो.
गणितातील ⇨गट सिद्धांतानुसार स्फटिकी पदार्थ, म्हणजे वस्तूंच्या त्रिमितीय आवर्ती संरचना, स्फटिकांच्या पुढील सहा गटांत (समुहांत) विभागता येतात : (१) त्रिनताक्ष, (२) एकनताक्ष, (३) समचतुर्भुजी वा विषमलंबाक्ष (४) षट्कोणीय किंवा चतुराक्ष, (५) चतुष्कोणीय किंवा द्विसमलंबाक्ष व (६) घनीय किंवा त्रिसमलंबाक्ष. हे स्फटिकांचे गट म्हणजे संरचनात्मक घट असे मानता येईल. प्रत्येक संरचनात्मक घटात एखाद्या मूलद्रव्याच्या अणूंची ठराविक संख्या असते. काटेकोर गणिती हिशोबानुसार या सहा समुहांचे ३२ स्फटिक वर्ग होतात. निरनिराळ्या वस्तू आवर्ती पद्धतीने अवकाशात मांडण्याचे २३० प्रकार होतात. त्यांना अवकाश गट असे म्हणतात [→ स्फटिकविज्ञान].
संरचनात्मक स्फटिकविज्ञान : क्ष-किरण विवर्तन तंत्राचा उपयोग करून स्फटिकाच्या आंतरिक संरचनेची सविस्तर माहिती उदा., संरचनेची सममिती, अवकाश गट, निरपेक्ष परिमाणे, एकक घटातील अणूंचे प्रकार म्हणजेच स्फटिक संरचना माहीत होऊ लागल्या. सुरुवातीला या तंत्राचा उपयोग करून फक्त खनिजांच्या स्फटिक संरचनांची माहिती मिळविण्यात आली, पुढे इतर अनेक पदार्थांच्या संरचना शोधून काढण्यात आल्या. या संशोधनासाठी हल्ली इलेक्ट्रॉन विवर्तन, न्यूट्रॉन विवर्तन, अवरक्त वर्णपटलेखन इ. तंत्रे वापरण्यात येतात.
भौतिक खनिजविज्ञान : स्फटिकमय खनिजांच्या बाह्य आकाराप्रमाणेच त्यांचे पुष्कळसे भौतिक गुणधर्म त्यांच्या आंतरिक म्हणजे घटक अणूंच्या संरचनेवर अवलंबून असतात. उदा., हिरा व ग्रॅफाइट ही दोन्ही कार्बनाची बनलेली असतात. पण त्यांची आंतरिक संरचना भिन्न असल्यामुळे हिरा अत्यंत कठीण व त्याचे वि. गु. ३.५२ असते. उलट ग्रॅफाइट अगदी मऊ असते व कागदावर घासल्यावर चरा न पडता त्याची रेघ उठते आणि त्याचे वि. गु. २.३ असते. भौतिक गुणधर्मांवरून खनिजाची जात ओळखणे सामान्यत: शक्य असते. निदान ती ओळखण्यात त्यांची बरीच मदत होते. साध्या, सोप्या कसोट्या वापरून खनिजांच्या भौतिक गुणधर्मांची परीक्षा करता येते. म्हणून त्या गुणधर्मांची माहिती व्यावहारिक दृष्ट्या अत्यंत उपयुक्त ठरते. भौतिक गुणधर्मांपैकी मुख्य म्हणजे पुढील होत.
पाटन : एखाद्या खनिजावर योग्य तितकी प्रेरणा (उदा., दाब) दिली असता ते त्यातील काही विशिष्ट समतलास अनुसरून भंग पावते व भंग पावण्याने तयार झालेली पृष्ठे सपाट गुळगुळीत असतात. अशा प्रकारे भंग पावण्याच्या गुणधर्मास पाटन म्हणतात. उदा., अभ्रक कुटत असताना ते फुटून त्याचे एकमेकांस समांतर, सपाट, गुळगुळीत व चकचकीत पत्रे तयार होतात. सुरीने चिरूनही तसेच पत्रे सुलभपणे वेगळे काढता येतात. काही खनिजांत एकच पाटन असते. उदा., अभ्रक, ऑजाइट या खनिजात एकमेकांस जवळजवळ लंबकोन करणारी दोन पाटनतले असतात. गॅलेनाचे स्फटिक घनाकार असतात व घनाच्या प्रत्येक पृष्ठाला समांतर अशी एकूण तीन पाटनतले त्याच्या स्फटिकात असतात. कित्येक खनिजांत यापेक्षा अधिक पाटनतले असतात. भंग पावण्याची सुलभता व भंग पावून निर्माण झालेल्या पृष्ठाचा गुळगुळीतपणा किंवा खडबडीतपणा ही लक्षात घेऊन उत्कृष्ट, चांगले, स्पष्ट, अस्पष्ट, अंधुक, इ. विशेषपणे वापरून पाटनाचे वर्णन केले जाते. क्वॉर्ट्झ व इतर कित्येक खनिजांत पाटन नसते. अस्फटिकी पदार्थांत ते अर्थान नसते [→ पाटन].
विभाजनतले : दाब (प्रतिबल) पडला असता कित्येक स्फटिकांत दुर्बल संरचना असणारी तले निर्माण होतात व त्या तलांस अनुसरून ते स्फटिक सहज भंग पावू शकतात. इतर कित्येकांत यमलन (जुळेपणा) उद्भवते (त्याला द्वितीयक यमलन म्हणतात). यमल (जुळ्या) स्फटिकांचे दोन घटक ज्या तलाने जोडले गेलेले असतात त्या तलास अनुसरूनही स्फटिक भंग पावणे शक्य असते. यमलनाची अनेकदा पुनरावृत्ती झालेली असली आणि यमलांचे घटक जोडणारी तले समांतर असली किंवा प्रारंभी उल्लेख केल्यासारखी दुर्बल संरचनेची अनेक समांतर तले निर्माण झालेली असली म्हणजे ती पाटनासारखी दिसतात. अशा तलांना विभाजनतले म्हणतात. ती ऑजाइट, कॅल्साइट, मॅग्नेटाइट, कुरुविंद इ. खनिजांच्या प्रतिबल-पीडित नमुन्यांत आढळतात. अपीडित नमुन्यांत ती असत नाहीत. ऑजाइट (001), कुरुविंदात (0001) व (1011),
मॅग्नेटाइटात (111) व कॅल्साइटात (1011) ही पृष्ठे विभाजनतले असतात.
कठिनता : कोणत्याही पदार्थाच्या सपाट पृष्ठाचा अपघर्षणास (खरडून टाकण्यास) किती विरोध होतो यावरून त्या पदार्थाच्या कठिनतेचे मान कळते. चाकूचे पाते किंवा कानस यांनी एखाद्या खनिजाच्या पृष्ठावर ओरखडा काढण्याचा प्रयत्न केला असता ओरखडा उठतो की नाही व उठत असल्यास किती जोराने ओरखडावे लागते यांवरून त्या खनिजाच्या कठिनतेचे ढोबळ मान कळते. निरनिराळ्या पदार्थांची कठिनता ठरविण्यासाठी सामान्यत: मोस मापक्रम वापरतात. [→ कठिनता].
कठिनता काही अंशी स्फटिकातील दिशांवर अवलंबून असते व निरनिराळ्या दिशांनी ओरखडले, तर कठिनतेचे मान भिन्नभिन्न असल्याचे आढळून येणे शक्य असते. पण सर्वसामान्य खनिजातील दिशापरत्वे होणारे कठिनतेतील फरक अत्यल्प असतात. सामान्य खनिजांपैकी कायनाइट व कॅल्साइट ही दोनच खनिजे अशी आहेत की, ज्यांच्या दिशापरत्वे होणाऱ्या कठिनतेमधील फरक कळून येण्यासारखे असतात. कायनाइटाच्या स्फटिकांच्या लाबीस अनुसरून कठिनता पाच आणि तिच्याशी लंब अशा दिशेस कठिनता सात असते. कॅल्साइटाच्या बहुतेक सर्व फलकांची कठिनता तीन, पण (0001) या फलकाची फक्त दोन असते.
सूक्ष्मग्राही उपकरणे वापरून स्फटिकांच्या दिशेतील कठिनतेचे अत्यल्पसे फरकही मापणे शक्य असते पण खनिजे ओळखणे एवढेच उद्दिष्ट असेल, तर मोस पद्धतीने मिळालेली फले पुरेसी होतात.
भंजन पृष्ठे : कोणतेही स्फटिकी पदार्थ पाटनाच्या किंवा विभाजनाच्या दिशांखेरीज इतर कोणत्याही दिशेने व अस्फटिकी पदार्थ कोणत्याही दिशेने भंग पावले म्हणजे जी पृष्ठे निर्माण होतात त्यांना भंजन पृष्ठे म्हणतात. बहुसंख्य खनिजांची भंजन पृष्ठे विषम म्हणजे खडबडीत आणि अगदी अनियमित असतात. काहींची सम म्हणजे लहान लहान खळगे, उंचवटे असलेली पण एकंदरीत सपाट असतात. काहींची भंजन पृष्ठे दंतुर म्हणजे तुटलेल्या लोखंडासारखी अतिशय खडबडीत, टोकदार उंचवटे व अनियमित खड्डे असल्यासारखी असतात. उदा., नैसर्गिक तांबे. काहींची भंजन पृष्ठे शंखाभ म्हणजे काच फुटल्यावर निर्माण होणाऱ्या वक्र, खोलगट पृष्ठासारखी असतात. क्वॉर्ट्झ, फ्लिंट आणि ज्वालाकाच यांची भंजन पृष्ठे शंखाभ असतात. काही खनिजांचे भंजन लाकडाच्या धलपीसारखे असतात.
दृढता : एखादे खनिज फोडताना, तोडताना, कुटताना, वाकविताना किंवा कापताना त्याच्याकडून जो प्रतिरोध होतो त्याला दृढता म्हणतात. पुढील संज्ञा वापरून दृढतेचे निरनिराळे प्रकार दर्शविले जातात : (१) ठिसूळ : सहज फुटणारे किंवा चुरा होणारे, उदा., क्वॉर्ट्झ, कॅल्साइट (२) घातवर्ध्य , घनवर्धनीय : हातोड्याने ठोकून ज्याचे पातळ पत्रे तयार करता येतात. उदा., नैसर्गिक सोने. (३) छेद्य : सुरीने कापता येते पण हातोड्याने ठोकळ्यास चुरा होतो. उदा., जिप्सम (४) तंतुक्षम : ज्याची तार काढता येते. उदा., नैसर्गिक प्लॅटिनम (५) नम्य : ते दाब देऊन वाकविता येते व दाब काढल्यावर वाकलेलेच राहते, पूर्वीचा आकार पुन्हा धारण करीत नाही. उदा., संगजिरे (६) प्रत्यास्थ (स्थितिस्थापक) : जे दाब दिल्यावर वाकते पण दाब काढून घेताच पूर्वस्थितीला येते. उदा., शुभ्र अभ्रकाचे पातळ पत्रे.
आघात आकृती : निमुळते, बोथट व किंचित गोलसर टोक असलेल्या छिन्नीने काही खनिजांच्या पृष्ठांवर आघात केला असता आघात केलेल्या पृष्ठावर फुलीसारख्या किंवा तीन किंवा सहा आरे असलेल्या ताऱ्यासारख्या सूक्ष्म भेगा निर्माण होतात. अशा रीतीने तयार झालेल्या आकृतीला आघात आकृती म्हणतात. आघात आकृतीच्या आऱ्यांच्या दिशा स्फटिकी दिशांशी संबद्ध असतात व भिन्न भिन्न पृष्ठांवर उठणाऱ्या आकृत्या किंवा दिशा साहजिकच भिन्न असतात. उदा., सैंधवाच्या घनीय पृष्ठावर चार आरे असलेली आकृती उठते तिचे आरे कर्ण दिशेने व द्वादशफलकी पृष्ठांस समांतर असतात. सैंधवाच्या अष्टफलकी स्फटिकांच्या पृष्ठांवर तीन आऱ्यांची आकृती उठते.
अभ्रकाच्या पाटनपत्र्यावर उठणारी आघात आकृती सहा आरे असलेल्या ताऱ्यासारखी असते व तिच्यातील एका रांगेत असणाऱ्या आऱ्यांच्या एका जोडीची दिशा (010) पृष्ठाला व इतरांच्या दिशा, (110) व (001) यांचे फलकं एकमेकांस छेदतात त्या कडांना जवळजवळ समांतर असतात. अभ्रकाच्या स्फटिकाचा आकार अनियमित असला, तर त्याच्या पाटनपत्र्यातील आघात आकृतीवरून त्याची स्फटिकी दिशा-निश्चिती (अभिविन्यास) करता येते. संगजिऱ्याच्या पाटनपत्र्यांवरही अभ्रकासारखी आघात आकृती उठते.
निमुळत्या छिन्नीने आघात करण्याऐवजी नुसते दाबण्यानेही अभ्रकाच्या पत्र्यावर तशीच पण स्पष्ट आकृती उठते. तिला दाब आकृती म्हणतात.
विशिष्ट गुरुत्व (वि. गु.) : एखाद्या खनिजाचा भार व ४० से. तापमानास त्या खनिजाच्या घनफळाइतके घनफळ असणाऱ्या पाण्याचा भार यांचे गुणोत्तर, हे त्या खनिजाचे विशिष्ट गुरुत्व असते. ते काही अंशी खनिजाच्या आंतरिक संरचनेवर व काही अंशी खनिजाच्या रासायनिक संघटनावर अवलंबून असते. हिरा व ग्रॅफाइट ही दोन्ही कार्बनाची बनलेली असतात, पण त्यांच्यातील कार्बन अणूंची मांडणी भिन्न असल्यामुळे हिऱ्याचे वि. गु. ३.५२ ग्रॅफाइटाचे २.३ असते. कॅल्साइट (षट्कोणीय समूह) व ॲरॅगोनाइट (विषमलंबाक्ष समूह) ही दोन्ही कॅल्शियम कार्बोनेटाची बनलेली असतात, पण त्यांपैकी पहिल्याचे वि. गु. २.७१ व दुसऱ्याचे २.९४ इतके असते.
भारी अणुभाराच्या मूलद्रव्यांपासून बनलेल्या खनिजांचे वि. गु. हलक्या मूलद्रव्यांपासून बनलेल्या खनिजांपेक्षा साहजिकच अधिक असते. उदा., कॅल्शियमाचा अणुभार ४०.०८, बेरियमाचा १३७.३६ व शिशाचा २०७.२१ असून त्यांच्या सल्फेटी खनिजांचे विशिष्ट गुरुत्व सोबतच्या सारणीत दिल्याप्रमाणे असते.
|
खनिज |
सूत्र |
वि. गु. |
|
ॲनहायड्राइट बराइट अँग्लिसाइट |
CaSO4 BaSO4 PbSO4 |
२.९३ ४.५० ६.३० |
फेल्स्पारे, क्वॉर्ट्झ, कॅल्साइट इ. सामान्य खनिजांचे वि. गु. २.६ ते २.७१ इतके असते. धातुकी म्हणजे ज्यांच्यापासून धातू काढल्या जातात त्या खनिजाचे वि. गु. सामान्यत: पाच किंवा त्याच्याहून अधिक असते.
खनिजाची जात ओळखण्यास वि. गु. अतिशय उपयोगी पडते. खनिजाचा एक घ.सेंमी. आकारमानाचा तुकडा वि.गु. काढण्यास पुरेसा होतो. जॉली स्प्रिंग तराजू, जलस्थैतिक तराजू, दांड्याचा तराजू इ. वापरून वि.गु. काढता येते. खनिज बारीक कणांच्या स्वरूपात असेल, तर विशिष्ट गुरुत्व कुपी किंवा पिक्नॉमीटर वापरून वि.गु. काढता येते. खनिजाचे वि.गु. काढण्यासाठी ब्रोमोफॉर्म (वि.गु. २.८९) किंवा मिथिलीन आयोडाइड (वि. गु. ३.३३) यांसारख्या द्रवाचाही उपयोग करतात. वरील दोन द्रव एकमेकांत मिसळून आणि त्यांच्या मधले वि.गु. असलेली मिश्रणे तयार करतात. ब्रोमोफॉर्म व मिथिलीन आयोडाइड ही ॲसिटोनाशीही (वि.गु. ०.७९) मिसळतात व ते मिसळून २.८९ पेक्षा कमी वि.गु. असणारे द्रव तयार करतात. अशा मिश्र व ज्ञात वि.गु. द्रवांपैकी एकेक घेऊन त्याच्यात खनिजाचे बरीक कण टाकतात व ते बुडतात का द्रवावर तरंगतात हे पाहतात. बुडाल्यास त्याचे वि.गु. अधिक व तरंगत राहिल्यास कमी हे यावरून कळते. वि.गु. काटेकोर ठरविण्यासाठी द्रवात ॲसिटोनाची हळूहळू भर घालून असे मिश्रण तयार करतात, की ज्याच्यात ते कण बुडणार नाहीत किंवा तरंगणार नाहीत. नंतर त्या द्रवाचे वि.गु. काढले जाते व तेच खनिजाचे वि.गु. असते [→ घनता व विशिष्ट गुरुत्व].
चमक किंवा द्युती : खनिजाच्या पृष्ठावरून प्रकाश परावर्तित होत असताना त्या पृष्ठाचे एकूण दिसणारे स्वरूप म्हणजे चमक होय. चमकेचे मुख्य प्रकार : (१) धातवीय (धातूसारखी). उदा., गॅलेना, पायराइट्स कॅल्कोपायराइट, (२) अधातवीय : धातूंच्या चमकेसारखी नसणारी चमक. अधावतीय चमक असणारी खनिजे पूर्ण अपारदर्शक नसतात. त्यांच्या पातळ कडांतून थोडा तरी प्रकाश जाऊ शकतो. अधातवीय चमकेचे मुख्य प्रकार पुढील होत. : (अ) काचेसारखी उदा., क्वॉर्ट्झ (आ) राळेसारखी उदा., स्फॅलेराइट (इ) मोत्यासारखी उदा., ॲपोफिलाइटाचे पाटनपृष्ठ (ई) रेशमासारखी उदा., तंतुमय जिप्सम. (उ) मेणासारखी तेलकट उदा., नेफेलीन व (ऊ) वज्रसम किंवा हिऱ्यासारखी तेजस्वी उदा., हिरा, अँग्लिसाइट.
धातवीय आणि अधातवीय चमकांत काटेकोर भेद करता येतोच असे नाही व त्याच्या संधिप्रकारास उपधातवीय म्हणतात. उदा., सिलोमेलेन.
रंग : रंग हा खनिजांचा प्रथम दर्शनी दिसून येणारा गुणधर्म असून कित्येक, विशेषत: अधातवीय खनिजे ओळखण्यास त्यांच्या रंगाची विशेष मदत होते. उदा., पायराइट्स आणि कॅल्कोपायराइट यांचा रंग पितळी, ॲझुराइटाचा मोरपिशी निळा, मॅलॅकाइटाचा हिरवा, हिंगुळाचा भडक तांबडा, मॅग्नेटाइटाचा काळा व गॅलेनाचा शिशासारखा काळसर असतो व रंगावरून ती चटकन ओळखता येतात.
रंग हा काही अंशी रासायनिक संघटनावर अवलंबून असतो. परंतु रंगहीन व रंग असणारी मूलद्रव्ये असा भेद करता येत नाही. कारण काही मूलद्रव्यांचे अनेक निरनिराळ्या संयुजा (इतर अणूंशी वा अणुगटांशी संयोग पावण्याच्या क्षमता) असणारे आयन तयार होतात. त्यांपैकी काही रंगहीन व काही रंगीत व भिन्नभिन्न रंगांचे असणे शक्य असते. ॲल्युमिनियम, सोडियम, पोटॅशियम, कॅल्शियम व बेरियम यांचे आयन रंगहीन व टिटॅनियम, क्रोमियम, मँगॅनीज, लोह, कोबाल्ट, निकेल यांचे आयन रंगीत असतात.
रंग काही अंशी खनिजात असलेल्या रंगीत मूलद्रव्यावर किंवा त्याच्यात समाविष्ट झालेल्या इतर रंगीत खनिजांच्या कणावर अवलंबून असतात. उदा., फ्ल्युओरस्पार या खनिजाचे रंगहीन, पांढरे, पिवळे, हिरवे, गुलाबी, निळे, जांभळे, उदी यांसारखे रंग असणारे नमुने आढळतात. कधीकधी त्याच्या एकाच नमुन्यात असे रंग इतस्तत: विखुरलेले किंवा नियमित पट्ट्यांच्या स्वरूपात असतात. क्वॉर्ट्झाचेही स्वच्छ रंगहीन, जांभळे, पिवळसर, गुलाबी इ. प्रकार आढळतात. सारांश, केवळ रंगावरून खनिजे ओळखता येत नाहीत. आणखी असे की, कित्येक खनिजांची पृष्ठे नैसर्गिक क्रियांमुळे गंजतात व कलंकित होतात. म्हणून त्यांचे तुकडे करून कोरी पृष्ठे पाहावी लागतात. क्वचित खनिजाच्या पृष्ठावरील कलंकावरून खनिजाचा मागमूस मिळतो.
कस : सूक्ष्म कणी चूर्णाचा रंग म्हणजे कस होय. एका विशिष्ट दगडी गोट्यावर सोने घासून सोन्याची कसोटी घेतली जाते, ही परिचित अशी गोष्ट आहे. खनिजांच्या कसोटीसाठी झिलई न केलेली भाजलेली चिनी मातीची वडी वापरतात. तिच्या किंचित खरबरीत पृष्ठावर खनिज घासल्यावर त्या खनिजाच्या कसाची रेघ उठते. या वडीची कठिनता सु. सात असते. त्यापेक्षा अधिक कठीण खनिजांसाठी तिचा उपयोग होत नाही व अधिक कठीण खनिजांचा कस मिळविण्यासाठी कानशीचा किंवा कठीण दगडाच्या तुकड्याचा उपयोग केला जातो. काही व विशेषत: धातवीय चमक असणारी खनिजे ओळखण्यासाठी कसाचा रंग उपयुक्त असतो. उदा., पायराइट्स व कॅल्कोपायराइट या दोहोंचे रंग पितळी किंवा सोन्यासारखे असतात. पण कसाच्या रंगावरून त्यांच्यात व सोन्यात सहज भेद करता येतो. वरील दोन्ही खनिजांचा कस काळा, हिरवट काळा किवा काळसर उदी असतो. हेमॅटाइट हे पोलादासारख्या काळ्या ते काळसर रंगाचे असते पण त्याचा कस तांबूस विटकरी रंगाचा असतो. एखाद्या खनिजाचे रंग विविध असू शकतात, पण त्या सर्वांचा कस मात्र सारखाच असतो.
पारदर्शकता : काही खनिजे काचेसारखी पारदर्शक असतात. काही दुधी काचेप्रमाणे काहीशी पारदर्शक किंवा पारभासी असतात. त्यांच्यातून प्रकाश जाऊ शकतो, पण पलीकडील वस्तू दिसत नाही. ज्यांच्या पातळ कडांतून किंवा सूक्ष्म कणातूनही प्रकाश पार जाऊ शकत नाही अशांना अपारदर्शक म्हणतात.
काही खनिजांचे नमुने फिरवून किंवा न फिरविता पाहत असताना व त्यांच्या पृष्ठावरून किंवा आतून येणारा प्रकाश पाहत असताना इंद्रधनुष्याच्या रंगांसारखे रंग दिसतात. त्यांच्या प्रकारावरून त्यांना वर्णविलास व वर्णदीप्ती किंवा वर्णछटा म्हणतात.
तारादर्शकता : काही व मुख्यत: षट्कोनी समूहातील खनिजांत त्यांच्या उभ्या अक्षाच्या दिशेने पाहिले असता ताऱ्यासारखा आकार असणारे प्रकाशाचे किरण दिसतात. उदा., नील किंवा शनी या खनिजाच्या काही जाती.
संदीप्ती : प्रदीतीखेरीज (उच्च तापमानामुळे प्रकाश देण्याखेरीज) इतर कोणत्याही कारणामुळे एखाद्या खनिजातून प्रकाश बाहेर पडू लागला म्हणजे त्या आविष्कारास संदीप्ती म्हणतात. संदीप्ती सामान्यत: अंधुक असते व फक्त काळोखातच दृष्टीस पडते.
संदीप्तीचे अनेक प्रकार असून ती अनेक कारणांनी उत्पन्न होते. उदा., फ्ल्युओरस्पार, स्फॅलेराइट व लेपिडोलाइट ही खनिजे घासल्याने, त्यांचा चुरा केल्याने किंवा त्यांना ओरखडल्याने संदीप्त होतात. काही खनिजे लाल होण्याच्या तापमानापेक्षा कमी तापमानापर्यंत तापविली असता संदीप्त होतात उदा., फ्ल्युओरस्पार. कित्येक खनिजांवर जंबुपार (वर्णपटातील जांभळ्या रंगाच्या पलीकडचा) प्रकाश किंवा क्ष-किरण किंवा ऋण किरण (विरल वायूतून विद्युत् प्रवाह जाऊ दिला असता ऋण अग्रापासून निर्माण होणारा ऋण विद्युत् भारित कणांचा म्हणजे इलेक्ट्रॉनांचा प्रवाह) पाडले असता संदीप्त होतात. उदा., फ्ल्युओरस्पार, विलेमाइट, शीलाइट, हिरा इत्यादींच्या काही जाती. वर उल्लेख केलेल्या खनिजांपैकी कित्येक खनिजे सूर्यप्रकाशात राहू देऊन नंतर काळोखात नेल्यावर ती संदीप्त झालेली दिसली व त्यावरून या आविष्काराकडे लक्ष गेले.
सूक्ष्मदर्शकाच्या साहाय्याने परीक्षण : खनिजांच्या चुऱ्याचे किंवा त्यांच्या पातळ छेदांचे विशिष्ट प्रकारच्या म्हणजे ध्रुवण किंवा ध्रुवणकारी (एकाच प्रतलात कंप पावणारा प्रकाश ज्यात मिळतो अशा) सूक्ष्मदर्शकाच्या साहाय्याने परीक्षण केले जाते. पारदर्शक खनिजासाठी (शिलाविज्ञानीय) साधा ध्रुवण सूक्ष्मदर्शक व अपारदर्शक खनिजांसाठी परावर्तनकारी (धातुकी अथवा धातुविज्ञानीय) सूक्ष्मदर्शक वापरले जातात. त्यांच्या उपयोगाची माहिती प्रकाशीय खनिजविज्ञान विभागात दिलेली आहे.
चुंबकीय व विद्युत् गुणधर्म : सामान्य खजिनांपैकी मॅग्नेटाइट व पायरोटाइट ही दोनच खनिजे चुंबकीय असून ती सामान्य लोहचुंबकाने आकृष्ट होतात. मॅग्नेटाइटाच्या लोडस्टोन नावाच्या जातीच्या अंगी लोहचुंबकासारखे चुंबकत्व व ध्रुवत्व असते.
दाब विद्युत् : स्फटिकाच्या एखाद्या अक्षाच्या दोन्ही टोकांवर दाब दिला असता त्याच्या पृष्ठावर विद्युत् भार निर्माण झाला, तर त्या भाराला ⇨ दाब विद्युत् म्हणतात. ज्यांना सममितीचा मध्य नसतो अशा स्फटिकांतच विद्युत् भार तयार होतो. अशांपैकी महत्त्वाचे खनिज म्हणजे क्वॉर्ट्झ होय.
ताप विद्युत् : योग्य तेवढ्या तापमानापर्यंत स्फटिक तापविला असता त्याच्या एकाच अक्षाच्या एका अग्रास ऋण व दुसऱ्या अग्रास धन विद्युत् भार एकाच वेळी निर्माण होतात. उदा., तोरमल्ली. ज्यांना सममितीचा मध्य नसतो अशा स्फटिकांपैकी एकच ध्रुवीय अक्ष असणाऱ्या स्फटिकांत हा आविष्कार मुख्यत: आढळतो.
रासायनिक खजिनविज्ञान : खनिजे ओळखण्यासाठी व त्यांच्या वर्गीकरणासाठी त्यांचे रासायनिक संघटन माहीत असणे आवश्यक असते. हे संघटन गुणात्मक व परिमाणात्मक पद्धतींनी काढण्यात येते. एखादे विशिष्ट मूलद्रव्य एखाद्या खनिजात आहे किंवा नाही, हे पुष्कळदा विश्लेषणाच्या सापेक्षत: साध्या व सुटसुटीत असणाऱ्या गुणात्मक पद्धती वापरून (उदा., फुंकनळी परीक्षेने) ठरविता येते. या पद्धतीला शुष्क पद्धती असेही म्हणतात. केवळ अशा परीक्षेवरून मिळविलेली माहिती व खनिजांचे भौतिक गुणधर्म यांच्यावरून खनिज ओळखणे शक्य असते. मात्र सैद्धांतिक कामासाठी किंवा एखाद्या खनिजात एखादा घटक म्हणजे मूलद्रव्य किती प्रमाणात आहे हे पाहून त्याचे मूल्य ठरवायचे असेल, त्यावेळी परिमाणात्मक विश्लेषण करावे लागते. खनिजामध्ये कोणती मूलद्रव्ये आहेत व त्यांचे प्रमाण किती आहे, हे परिमाणात्मक विश्लेषणावरून समजते. खनिजात असणाऱ्या निरनिराळ्या मूलद्रव्यांच्या वजनांची टक्केवारी देऊन हे विश्लेषण देण्यात येते. खनिजाच्या पूर्ण विश्लेषणामध्ये त्यात असणाऱ्या सर्व मूलद्रव्यांच्या टक्केवारीची बेरीज सैद्धांतिक दृष्ट्या १०० असावी लागते. मात्र अचूकतेवर मर्यादा असल्यामुळे अगदी काळजीपूर्वक व पद्धतशीर विश्लेषण केल्यास ही बेरीज ९९.५ ते १००.५ या दरम्यान येते. या बेरजेवरून मग प्रत्येक घटक हा १०० भागांत किती प्रमाणात असेल ते काढण्यात येते. ही सुधारित टक्केवारी काही महत्त्वाचे हिशेब काढण्यासाठी वापरतात.
रासायनिक विश्लेषणावरून खनिजाचे रासायनिक सूत्र काढणे : रासायनिक विश्लेषणाची फले खनिजातील मूलद्रव्यांच्या वजनांच्या टक्केवारीच्या स्वरूपात दिलेली असतात. निरनिराळ्या मूलद्रव्यांचे अणुभार वेगवेगळे असल्यामुळे या टक्केवारीवरून खनिजातील निरनिराळी मूलद्रव्ये कुठल्या आणवीय प्रमाणात आहेत ते समजत नाही. विश्लेषणातील प्रत्येक मूलद्रव्याच्या टक्केवारीस त्या मूलद्रव्याच्या अणुभाराने भागून खनिजातील निरनिराळ्या मूलद्रव्यांचे आणवीय प्रमाण मिळते. मूलद्रव्यांच्या आणवीय प्रमाणांवरून त्यांचे गुणोत्तर काढता येते आणि त्यावरून रासायनिक सूत्र काढता येते. उदा., कॅल्कोपायराइट.
|
टक्केवारी |
अणुभार |
आणवीय प्रमाण |
आणवीय गुणोत्तर |
||||
|
तांबे (Cu) ३४.३० |
/ |
६३.५४ |
= |
०.५३९८ |
१ |
} |
|
|
लोह (Fe) ३०.५९ |
/ |
५५.८५ |
= |
०.५४७७ |
१ |
अंदाजे |
|
|
गंधक (S) ३४.८२ |
/ |
३२.०७ |
= |
१.०८५७ |
२ |
||
कॅल्कोपायराइटामध्ये तांबे १, लोह १ व गंधक २ या प्रमाणात आहेत (Cu: Fe : S = १ : १ : २). यावरून कॅल्कोपायराइटाचे रासायनिक सूत्र CuFeS2 असे ठरते.
खनिज ऑक्सिजनाचे संयुग असल्यास विश्लेषणाची फले ऑक्साइडांच्या टक्केवारीच्या स्वरूपात देतात. यावरून रासायनिक सूत्र काढण्यासाठी ऑक्साइडांच्या वजनांना त्यांच्या रेणुभाराने भागून त्यांचे रेणवीय प्रमाण काढावे लागते आणि त्यावरून रेणवीय गुणोत्तर काढता येते. या गुणोत्तरावरून खनिजाचे रासायनिक सूत्र मिळते.
स्फटिक किंवा ⇨ घन अवस्था रसायनशास्त्राचा उपयोग हल्ली खनिजविज्ञानात फार मोठ्या प्रमाणावर करण्यात येतो. स्फटिक रसायनशास्त्रात पुढील माहितीचा समावेश करण्यात येतो. (१) अणूंमध्ये बंध निर्माण करणारी प्रेरणा, (२) स्फटिक संरचनेचे ढोबळ व सविस्तर स्वरूप, (३) मूलद्रव्यांचे रासायनिक व संरचनात्मक गुणधर्म, (४) खनिजे व इतर पदार्थ यांचे स्वरूप आणि गुणधर्म. हॅलाइडे (फ्ल्युओरीन, क्लोरीन, ब्रोमीन, आयोडीन व ॲस्टेटीन यांची संयुगे), बहुतेक सर्व ऑक्साइडे व ऑक्सि-लवणे (ऑक्सिजनयुक्त अम्लांची लवणे) अशी पुष्कळशी खनिजे ही आयनी स्फटिक असतात. ऋणायन आणि धनायन हे दोन्ही स्थिर विद्युत् आकर्षणाच्या बंधांनी जोडलेले असतात. त्यांना आयनी किंवा ध्रुवीय बंध म्हणतात. शुद्ध अधातवी मूलद्रव्ये व पुष्कळशी सल्फाइडे मुख्यत्वेकरून सहसंयुजी (ज्यांत दोन अणूंमध्ये दोन वा अधिक इलेक्ट्रॉन समाईक असतात अशा) बंधांनी जोडलेली असतात. धातवी बंध शुद्ध धातूंमध्ये व काही सल्फाइडांत असतात. ब्रुसाइट, मॉलिब्डेनाइट यासांरखी खनिजे आणि अक्रिय (रासायनिक विक्रियांत सहजासहजी भाग न घेणारे, उदा., हीलियम) वायू कमी तापमानास घन केले असता त्यांच्यामध्ये दुर्बल असे व्हॅन डर व्हाल्स बंध (संयुजा बंधाखेरीज इतर आंतर-आणवीय आणि आंतर-रेणवीय आकर्षण प्रेरणांमुळे निर्माण होणारे बंध, व्हॅन डर व्हाल्स या शास्त्रज्ञांच्या नावाने ओळखण्यात येणारे) असतात.
स्फटिकांचे पुष्कळ गुणधर्म उदा., प्रकाशीय गुणधर्म, त्यांचे प्रकार, ठेवण, पाटन, त्यांचा स्पर्श, वाहकता, पृष्ठशोषकता इ. हे काही अंशी का होईना ज्या प्रकारचे बंध स्फटिकात असतात त्यांवर अवलंबून असतात. काही खनिजांची स्फटिक-संरचना अगदी साधी (उदा., साधे मीठ NaCl), तर काहींची अगदी जटिल (उदा., फल्स्पार, तोरमल्ली) असते. खनिजांची संरचनात्मक माहिती सहसंयोजनाचा भूमितीय पद्धतीने विचार करून साध्या सोप्या रीतीने सांगता येते. कुठल्याही प्रकारच्या एका अणूच्या (आयनाच्या) अगदी लगत व सभोवार असणाऱ्या दुसऱ्या प्रकारच्या अणूंच्या (आयनांच्या) संख्येवरून व त्यांच्या मांडणीच्या प्रकारावरून सहसंयोजन कशा प्रकारचे आहे ते समजते. सहसंयोजित गटांची निरनिराळ्या प्रकारांनी एकत्र जुळणी करून स्फटिक संरचनांचे वर्णन किंवा पृथक्करण करता येते. बऱ्याचशा खनिजांत अधातवी अणू (विशेषकरून ऑक्सिजन व गंधक) स्फटिक संरचनेत फार मोठी जागा व्यापतात. तसेच ते एकमेकांच्या अगदी जवळजवळ असतात म्हणजे त्यांची मांडणी घन संकुलन पद्धतीची असते. घन संकुलन पद्धतीने बंधित झालेल्या अधातवी (धनायन) अणूंमधील आंतरापोकळ्यांत धातवी अणू (ऋणायन) असलेली स्फटिक संरचना अशा खनिजात असते. घन संकुलन असणाऱ्या घनीय व षट्कोनी अशा दोन प्रकारच्या संरचना आहेत. दोन्हींमध्ये आंतरापोकळ्यांचे दोन संच असतात. एका संचातील प्रत्येक पोकळीच्या सभोवार सहा सहांचे किंवा अष्टफलकीय सहसंयोजन असलेले, सहा अधातवी अणू (धनायन) असतात व दुसऱ्या संचातील प्रत्येक पोकळीच्या सभोवार चारा चारांचे किंवा चतुष्फलकीय सहसंयोजन असलेले चार अधातवी अणू असतात. या पद्धतीने हॅलाइटाची (म्हणजे साध्या मिठाची NaCl) संरचना पुढीलप्रमाणे सांगता येते. यातील क्लोरिनाचे धनायन घनीय प्रकारच्या घन संकुलनाने जोडलेले असतात व सोडियमाने अणू अष्टफलकीय सहसंयोजनाच्या स्थानांवर असतात. स्फॅलेराइटात गंधकाचे अणू घनीय पद्धतीने घन संकुलित असतात. जस्ताचे अणू चतुष्फलकीय जागांवर असतात. व्ह्यूर्टझाइटातही जस्ताचे अणू चतुष्फलकीय स्थानांवर असतात. मात्र त्यातील गंधकाचे अणू षट्कोणी घन संकुलनाच्या जागा व्यापतात. ऑलिव्हिनामधील (Mg2SiO4) ऑक्सिजनाचे आयन जवळजवळ षट्कोणी घन संकुलनाच्या जागा व्यापतात व धातूंचे अणू दोन्ही प्रकारच्या जागांवर असतात. सिलिकॉन चतुष्फलकीय आंतरापोकळ्यांत आणि मॅग्नेशियम अष्टफलकीय पोकळ्यांत असतात.
स्फटिक रसायनशास्त्रातील अगदी सुरुवातीची असलेली महत्त्वपूर्ण माहिती ही जटिल अशा सिलिकेटी खनिजांच्या संरचनेची व त्यांच्या गुणधर्मांची होती. सिलिकॉन व ऑक्सिजन यांचा चतुष्फलक हा सिलिकेटांच्या संरचनेतील मूलभूत एकक असतो. एका सिलिकॉनाच्या सभोवार चतुष्फलकाच्या टोकांवर चार ऑक्सिजन असलेले हे सहसंयोजन असते. सिलिकेचे अनेक चतुष्फलक निरनिराळ्या प्रकारांनी जोडले जाऊन सिलिकेची भिन्न प्रकारची धनायन मूलके (रासायनिक विक्रियेत बदल न पावणारे पण सामान्यत: स्वतंत्र अस्तित्व नसणारे अणुगट) असलेल्या वेगवेगळ्या आणवीय संरचना निर्माण होतात. ठराविक प्रकारचे सिलिकेचे धनायन गट त्यांच्या आंतरापोकळ्यांत असणाऱ्या ऋणायनांनी बांधले जाऊन सिलिकेटांच्या प्रत्येक जातीतील संरचना तयार होते. स्फटिकांची ठेवण, पाटन, प्रकाशीय गुणधर्म, द्रव अवस्थेतील श्यानता (दाटपणा), पृष्ठशोषकता, क्रियाशीलता यांसारखे अनेक गुणधर्म सिलिकेटी मूलकांच्या प्रकारावर अवलंबून असतात.
स्फटिक कोश : खनिजातील मूलद्रव्यांचे अणू विशिष्ट पद्धतीने जोडले जाऊन त्यातील संरचनात्मक एकके तयार होतात. ही एकके म्हणजे अणूंचे सांगाडे असतात आणि ते एकमेकांस जोडले जाऊन स्फटिकी संरचना तयार होते. खनिजातील संरचनात्मक एकक असणाऱ्या आणवीय सांगाड्यास ‘स्फटिक कोश’ असे म्हणतात. कुठल्याही स्फटिकी पदार्थांच्या स्फटिक कोशामध्ये त्या पदार्थांच्या रासायनिक सूत्राच्या एककांची संख्या ठराविक असते. स्फटिक कोशाची परिमाणे आणि खनिजाची घनता ही माहीत असतील, तर स्फटिक कोशाचे संघटन सांगता येते.
स्फटिक कोशातील रासायनिक सूत्राच्या एककांची संख्या Z या अक्षराने दर्शविण्यात येते. उदा., स्फॅलेराइटात Z चे मूल्य ४ असते म्हणजे स्फॅलेराइटाच्या स्फटिक कोशामध्ये त्याच्या (Zn, Fe) S या सूत्राची चार एकके असतात. म्हणजेच त्यात धातूचे ४ व गंधकाचे ४ अणू असतात.
आधुनिक खनिजविज्ञानात खनिजाचे रासायनिक संघटन हे त्याच्या स्फटिक कोशाची परिमाणे देऊन सांगण्यात येते. या प्रकाराच्या माहितीचे वर्णन तक्त्यांत किंवा सारण्यांमध्ये पुढीलप्रमाणे देण्यात येते. उदा., ऑलिव्हीन खनिज. ते समचतुर्भुजी असते. अवकाश गट Pbnm, घनता (p) = ४.०७ ग्रॅ./घ.सेंमी., a = 4.79A०, b = 10.33 A०, c = 6.06 A० (a, b आणि c ही अक्षांची परिमाणे असून A० हे अँगस्ट्रॉम एकक = १०-८ सेंमी. आहे). यावरून आकारमान V = abc = 299.85 (Ao)3. एकक कोशातील रेणवीय वजन = (p) V / 1.66 = 735.17 या हिशोबांवरून तक्ते तयार केलेले असतात. ऑलिव्हिनात Z चे मूल्य ४ येते. यावरून सारणीमध्ये ऑलिव्हिनाच्या स्फटिक कोशाचे संघटन 4 [ (Mg, Fe)2 SiO4] असे दिलेले असते.
खनिजांचे गुणधर्म स्फटिकी संरचनेवर अगदी घनिष्ट रीतीने अवलंबून असल्यामुळे रासायनिक सूत्र संरचनात्मक सूत्राच्या स्वरूपात देण्याची पद्धत रूढ झाली आहे. स्फटिक कोशातील प्रत्येक प्रकारची एकमेव जागा एका विशिष्ट प्रकारच्या अणूने व्यापलेली असते. स्फटिक कोशामध्ये एका ठराविक प्रकरच्या स्थानाची पुनरावृत्ती होऊ शकते म्हणून ‘एकमेव’ हा शब्द येथे वापरला आहे. स्फटिक कोशातील एकमेव स्थानांची संख्या अवकाश गटाच्या सममितीवर अवलंबून असते. शुभ्र अभ्रकाचे रासायनिक सूत्र संरचनात्मक सूत्राच्या स्वरूपात
KAl2(Si3 Al O10)(OH)2
असे देतात. या सूत्रावरून ॲल्युमिनियमाच्या संरचनात्मक दोन जाती दिसून येतात. ॲल्युमिनियमाचे एक तृतीयांश अणू चतुष्फलकीय पद्धतीने व दोन तृतीयांश अणू अष्टफलकीय पद्धतीने सहसंयुजित असतात. चतुष्फलकीय ॲल्युमिनियम संरचनात्मक दृष्ट्या सिलिकॉनासारखा असतो. ॲल्युमिनियमाच्या अशा दोन प्रकारच्या एकत्र येऊन ॲल्युमिनो सिलिकेटाची पत्रके तयार होतात.
(Aa) (Bb)…. (Pp) या सूत्राचा विचार केल्यास सूत्रातील प्रत्येक कंस हा एक एकमेव आणवीय स्थान दर्शवितो, मोठे अक्षर मूलद्रव्ये दर्शविते व लहान अक्षर ते मूलद्रव्य किती वेळा एककात आढळते ते दर्शविते. सर्व लहान अक्षरांचे मूल्य एकच असल्यास फक्त सूत्रमय एककच शिल्लक राहते. संरचनेचा प्रकार व आदर्श सूत्रमय एकक यांच्यावर खनिजाची जाती निश्चित होते. खनिजाच्या जातीचे अशा प्रकारचे अगदी काटेकोर विनिर्देशन करणे आवश्यक असते. कारण एखाद्या खनिजामध्ये रासायनिक संघटन एकच आणि ठराविक नसून ते अभिसीमित (दोन मर्यादांच्या दरम्यानचे) असणे शक्य असते. खनिजाच्या रासायनिक संघटनाला अभिसीमा असल्यास त्यास त्या खनिजाची माला असे म्हणतात. मालेतील संघटनाच्या अभिसीमेच्या दोन टोकांचे विशिष्ट किंवा ठराविक संघटन असणाऱ्या घटकांना ‘अंत्य घटक’ असे म्हणतात. या प्रत्येक अंत्य घटकाला एक वेगळे व विशिष्ट नाव असते. हे सर्व ऑलिव्हीन खनिजाच्या मालेवरून स्पष्ट होते. ऑलिव्हीन मालेमध्ये फायलाइट (FeFeSiO4 किंवा Fe2SiO4) व फॉर्स्टेराइट (Mg2SiO4) हे दोन अंत्य घटक आहेत. फायलाइट ही जाती ऑलिव्हिनी संरचना असलेले फेरस ऑर्थोसिलिकेट असते व फॉर्स्टेराइट जातीदेखील तीच संरचना असलेले मॅग्नेशियम ऑर्थोसिलिकेट असते. ग्रॅम-मोलच्या (ग्रॅममध्ये दिलेल्या रेणुभाराच्या) दृष्टीने विचार करता ऑलिव्हिनामध्ये मॅग्नेशियमापेक्षा लोह जास्त असल्यास ऑलिव्हिनाची माला (Fe, Mg)2 SiO4 अशी दर्शवितात. दोन्ही अष्टफलकीय जागांत लोह व मॅग्नशियम वाटेल त्या प्रमाणात येत असतील, तर ऑलिव्हिनाचे सूत्र (Fe, Mg)2 SiO4 वा (Mg, Fe)2 SiO4 असे लिहितात व अष्टफलकीय ऋणायन अव्यवस्थित आहेत असे म्हणतात. जर लोह एकाच प्रकारची अष्टफलकीय जागा व्यापत असेल, व मॅग्नेशियम दुसरी विशिष्ट जागा व्यापत असेल, तर ऑलिव्हिनाचे सूत्र FeMgSiO4 असे लिहितात व अशा वेळी ऋणायन सुव्यवस्थित आहेत असे म्हणतात. कुठल्याही एका ठराविक दाब व तापमानास ऑलिव्हिनाचे स्फटिक अव्यवस्थित, सुव्यवस्थित अथवा दोन्हींच्या मिश्रणाचे असणे शक्य असते.
समरूपता,समरचनात्मकता : कुठल्याही एका ठराविक प्रकारच्या संरचनेमध्ये भिन्न आणवीय मूलद्रव्ये भाग घेऊ शकतात. ऑलिव्हिनामधील लोह व मॅग्नेशियमाप्रमाणे काही मूलद्रव्ये समरूपी माला तयार करतात, तर काहींची अशी माला होऊ शकत नाही. दुसऱ्या प्रकाराला एकमेकांची ‘समरूपे’ म्हणतात. माँटिसेलाइट Ca MgSiO4 व ट्रायफायलाइट LiFePO4 आणि ऑलिव्हीन ही समरूपी असतात. त्यांच्या संरचनेचा प्रकार व्यवस्थित ऑलिव्हिनाप्रमाणे असतो. हॅलाइट (NaCl), पेरिक्लेज (MgO), गॅलेना (PbS), बॅराइट (BaSO4), सेलेस्टाइट (SrSO4) व क्रोकोआइट (PbCrO4) या सर्वांत एकच प्रकारची संरचना असते. या गुणधर्माला ‘समरचनात्मकता’ असे म्हणतात. हा गुणधर्म सुरुवातीला लक्षात आला त्यावेळेस ज्या पदार्थांच्या रासायनिक सूत्रांत साम्य असते तेच समरूपी असतात असे समजत असत. उदा.,
KH2 PO4 KH2 AsO4 (NH4) H2PO4 (NH4) H2AsO4
यांचे स्फटिक समरूपी असून त्यांच्या समान पृष्ठांमधील कोन सारखे असल्याचे दिसून आले. या पाहणीवरून मिचर्लिख यांच्या मूळ व्याख्येनुसार ज्या खनिजांच्या रासायनिक सूत्रांत साम्य असून ज्यांचे स्फटिक एकमेकांसारखे असतात त्यांना समरूपी म्हणतात. परंतु खनिजांच्या क्ष-किरण अध्ययनावरून स्फटिकांचे स्वरूप हे त्यांतील आंतरिक संरचनेमुळे आलेले असते असे दिसून आले. म्हणजेच समरूपता ही समरचनात्मकतेमुळे आलेली असते. यावरून समरूपी पदार्थांना समरचनात्मक पदार्थ असे नाव देण्यात आले. पुढे ज्या पदार्थांच्या रासायनिक सूत्रांत वर वर पाहता साम्य नाही असे पदार्थही समरचनात्मक असतात असे आढळून आले. उदा., बर्लिनाइट (AlPO4) हे क्वार्ट्झाशी 2SiO2 (SiSiO4) व टँटॅलाइट FeTa2O6 हे ब्रूकाइटाशी 3TiO2 (TiTi2O6) समरचनात्मक असते. यांतील धातवी आयनांचे आकारमान जवळजवळ समान असते.
अशा रीतीने समरचनात्मकता निर्माण होण्यासाठी रासायनिक सूत्रात साम्य असण्यापेक्षा निरनिराळ्या पदार्थांतील अणूंचे आकारमान समान असणे अधिक आवश्यक असते. कॅल्शियम व मॅग्नेशियम हे रासायनिक दृष्ट्या समान असतात. परंतु क्वचितच समरचनात्मक असतात. कारण त्यांच्या आयनांच्या आकारमानांत बराच फरक असतो. Ca2+ ची आयनी त्रिज्या ०.११A० व Mg2+ ची ०.६६ A० असते [→ समरूपता].
बहुरूपता : कधीकधी एकच रासायनिक संघटन असणाऱ्या पदार्थाचे एकापेक्षा अधिक संरचनात्मक प्रकार आढळतात. या पदार्थांचे स्फटिक भिन्न प्रकारचे म्हणजे निरनिराळ्या स्फटिक समूहांचे असतात. या गुणधर्मास बहुरूपता असे म्हणतात. उदा., कॅल्साइट-ॲरॅगोनाइट CaCO3, पायराइट्स-मार्कॅसाइट FeS2, अँडॅल्युसाइट, सिलिमनाइट व कायनाइट Al2SiO5. निरनिराळ्या पदार्थांच्या बहुरूपांतील संरचनात्मक फरक भिन्न प्रमाणात असतात. वरील उदाहरणातील खनिजांच्या भिन्न आणवीय संरचना अगदी स्पष्ट असतात. खनिज तयार होण्याच्या वेळी असणाऱ्या ऊष्मारासायनिक परिस्थितीनुसार निरनिराळी बहुरूपे तयार होतात. दाब व तापमानाच्या परिस्थितीनुसारही स्फटिकात निर्माण होणाऱ्या सुव्यवस्थितपणा किंवा अव्यवस्थितपणा यांचा प्रकार व प्रमाण यांच्यामुळे थोड्या प्रमाणात होणारे बहुरूपी फरक निर्माण होतात. अशा रीतीने मायक्रोक्लीन व सॅनिडीन [(K, Na) Si3AlO8] यांच्यातील फरक ॲल्युमिनो सिलिकेटांच्या संरचनात्मक सांगाड्यातील चतुष्फलकीय स्थानावरील ॲल्युमिनियम व सिलिकॉन यांच्या सुव्यवस्थित मांडणीतील फरकांवरून समजतो.
स्फटिकामध्ये असणाऱ्या घटक पत्रकांच्या सुव्यवस्थित संरचनात्मक मांडणीमध्ये असणाऱ्या फरकामुळे काही खनिजांचे अगदी सूक्ष्म फरक असलेले बहुविध प्रकार तयार होतात. उदा., क्वॉर्ट्झ, ट्रिडिमाइट, क्रिस्टोबलाइट व कोएसाएट ही सिलिकेची खनिजे [→ बहुरूपता].
घन विद्राव : काही खनिजांमध्ये रासायनिक संघटन एकसम व ठराविक असे नसते. अशा खनिजांत संघटनाची अभिसीमा असण्याचा गुणधर्म असतो, त्याला घन विद्राव असे म्हणतात. खनिजाच्या आंतरिक संरचनेमध्ये होणाऱ्या (१) साध्या अणूंची अदलाबदल, (२) मूलकांची अदलाबदल, (३) काही स्थानांवर अणूंची अनुपस्थिती, (४) आंतरापोकळ्यांत स्थानापन्न होणारे अणू व (५) मिश्र स्फटिक यांच्यामुळे घन विद्रावण होते.
अणूंच्या साध्या अदलाबदलीमध्ये रासायनिक दृष्ट्या भिन्न असणाऱ्या अणूंच्या जाती संरचनात्मक दृष्टीने समान असतात. उदा., मॅग्नेशियम आणि फेरस लोह, ॲल्युमिनियम व सिलिकॉन, फ्ल्युओरीन, हायड्रॉक्सिल गट (OH) आणि ऑक्सिजन. अशा प्रकारच्या अणूंची एकमेकांशी अदलाबदल एकाच प्रकारच्या संरचनात्मक स्थानावर भिन्न प्रमाणात होऊन घन विद्राव तयार होतात. उदा., ऑलिव्हिनामध्ये (Mg, Fe, Mn)2 SiO4 मॅग्नेशियम, फेरस लोह मँगॅनीज यांचे अणू सिलिकेच्या स्वतंत्र चतुष्फलकांमध्ये असणाऱ्या अष्टफलकीय सहसंयोजनाच्या जागेत असतात. या अष्टफलकीय जागा सर्वच्या सर्व मॅग्नेशियम ते सर्वच्या सर्व लोह या अभिसीमेत कुठल्याही प्रमाणात भरल्या जाऊ शकतात, मात्र मँगॅनीज सापेक्षत: अगदी कमी जागा व्यापू शकते. याचाच अर्थ असा होतो की, लोह व मॅग्नेशियम यांचे सर्व प्रमाणात घन विद्रावण होऊ शकते, मात्र मँगॅनिजाच्या बाबतीत ते मर्यादित प्रमाणातच होते. ज्या वेळी भिन्न संयुजा असणाऱ्या अणूंचे धन विद्रावण होते त्यावेळी पूरक अणूंच्या बदलाने शेष विद्युत् भाराचे उदासिनीकरण (नाहीसा करणे) होते.
खनिजात मूलकांची अदलाबदल होते. यामध्ये Cl2, CO3 किंवा SO4 यांसारखे मूलक एकमेकांच्या स्थानांवर येतात. अशा प्रकारची अदलाबदल संरचनात्मक सांगाड्यात सिलकेटाप्रमाणे मोठ्या आकारमानाच्या पोकळ्या असणाऱ्या खनिजांतच मर्यादित असते. उदा., फेल्सपॅथॉइडे, स्कॅपोलाइटे इत्यादी.
संरचनात्मक रासायनिक सूत्रात साम्य असणाऱ्या अणूंचा घन विद्राव कंसात निर्देशित होतो उदा., (Mg, Fe)2SiO4. दोन प्रकारचे घन विद्राव असतात. (१) संपर्ण घन विद्रावण : हे फेरोमॅग्नेशियमी खनिजांत बऱ्याच वेळा आढळते. उदा. ऑलिव्हिने, पायरोक्सिने, अल्बाइट-ॲनॉर्थाइट प्लॅजिओक्लेज या घन विद्राव माला सुपरिचित आहेत. (२) मर्यादित घन विद्रावण : यात एक किंवा अनेक प्रकारचे अणू प्रामुख्याने असतात. ते अधोरेखेने दाखवितात. त्यांशिवाय इतर कमी महत्त्वाचे परंतु वैशिष्ट्यपूर्ण अणूही असतात. उदा., मायक्रोक्लीन (K,Na) Si3AlO8 व कृष्णाभ्रक K (Mg, Fe, Al)3 (Si, Al)4 O10 (OH, F)2.
आणवीय संरचनेतील काही धातूंचे, अधातूंचे किंवा दोहोंचे अणू गाळले जाऊन त्यांच्या जागा रिकाम्या राहून रासायनिक संघटनात बदल होणे शक्य असते. उदा., पायरोटाइटातील धातूच्या अणूंच्या कधीकधी एक पंचमांश जागा रिकाम्या असतात. त्यामुळे त्याचे सूत्र Fe1-x S असे होते. स्कुटेरूडाइटात अधातवी अणूंच्या एक षष्ठांश जागा रिकाम्या असू शकतात. त्यांचे सूत्र (CoNi) As3-x असते. साध्या अदलाबदलीने तयार झाले असे समजण्यात आलेले बरेच घन विद्राव संमिश्र स्फटिकांमुळे झाले असणे शक्य आहे. घन विद्राव कुठल्याही प्रकाराने झालेले असोत त्याचे प्रमाण पुढील गोष्टींवर अवलंबून असते. (१) अणूंमध्ये संरचनात्मक साम्य असणारे अणू उपलब्ध असणे, (२) स्फटिकांच्या संरचनेचा प्रकार, (३) स्फटिकांच्या वाढीच्या वेळेची संघटनात्मक परिस्थिती, दाब व तापमान. संरचनात्मक साम्य हे अणूंचे आकारमान व त्यांच्यातील बंधांचा प्रकार यांवर अवलंबून असते. उच्च तापमान घन विद्रावण होण्यास पोषक असते. घन विद्रावणामध्ये भाग घेणाऱ्या अणूंचे आकारमान जवळजवळ सारखे असावे लागते. तसेच त्यांच्या संयुजाही सारख्याच असाव्या लागतात. आकारमान सारखे असूनही संयुजांमधील फरक एकाहून अधिक असल्यास सामान्यत: आणवीय अदलाबदल होत नाही [→ घन विद्राव].
प्रकाशीय खनिजविज्ञान : स्फटिकी पदार्थांत निरनिराळे पण ठराविक प्रकाशीय गुणधर्म असतात. घनीय स्फटिकांखेरीज इतर सर्व प्रकारचे स्फटिक द्विप्रणमनी असतात. म्हणजे त्यांच्यातून प्रवास करीत असताना साधा प्रकाश दुभंगतो व त्यामुळे निर्माण होणारे दोन ध्रुवित (एकाच प्रतलात कंप पावणारे) किरण भिन्न दिशांत व भिन्न वेगांनी प्रवास करतात. घनीय पदार्थात फक्त एकच प्रणमनांक (प्रकाशाचा निर्वातातील वेग व पदार्थ माध्यमातील वेग यांचे गुणोत्तर, वक्रीभवनांक) असतो व इतर स्फटिक समूहांच्या पदार्थांत दोन असतात. खनिजांचे प्रणमनांक शोधून काढले, तर ते खनिज ओळखण्यास बरीच मदत होते. ध्रुवण सूक्ष्मदर्शक वापरून खनिजांचे प्रणमनांक काढता येतात. निरनिराळ्या किरणांच्या वेगांतील फरक, द्विप्रणमनामुळे निर्माण होणारे रंग व आकृत्या यांच्या साहाय्याने खनिज शोधण्याची एक संपूर्ण अशी प्रकाशीय पद्धत तयार झालेली आहे.
अपारदर्शक खनिजे (धातुके) धातुकी सूक्ष्मदर्शक वापरून तपासण्यात येतात. यात परावर्तित प्रकाशाच्या गुणधर्मांची पाहणी करण्यात येते [→ धातुरचनाविज्ञान].
सूक्ष्मदर्शकाच्या साहाय्याने परीक्षण : कित्येक खडकांचे किंवा खनिजांचे नमुने नुसत्या डोळ्यांनी किंवा एखाद्या भिंगाने तपासून पाहून त्यांचे घटक ओळखता येतात. पण पुष्कळ नमुने ओळखण्यासाठी सूक्ष्मदर्शकाचा उपयोग करावा लागतो. सूक्ष्मदर्शकाने करावयाच्या परीक्षणांसाठी पुढील दोन पद्धती वापरल्या जातात.
(१) तपासावयाच्या नमुन्याचे तुकडे करून व ते खलबत्त्यात कुटून सु. ०.१ ते ०.५ मिमी. व्यासाचे बारीक कण होतील असा त्यांचा चुरा करतात. तो चुरा पाण्याने धुऊन त्याच्यातील मातीसारखे कण काढून टाकतात. नंतर तो वाळवून चाळतात व त्याच्यातील भरड कण काढून टाकतात. चाळून घेतलेले बारीक कण एका काचपट्टीवर घेऊन सूक्ष्मदर्शकाने तपासतात. नमुन्याचा चुरा करण्याचे काम थोड्या वेळात होते, पण चुरा केल्यामुळे खनिजांचे आकार व संरचना यांचा नाश होतो. तसेच मूळच्या खडकांतील खनिजांची मांडणी कळत नाही. आणखी असे की, चुऱ्यातील कणांची स्थिती यदृच्छेवर अवलंबून असते. खडकातून किंवा खनिजातून एखाद्या विशिष्ट दिशेने जाणाऱ्या छेदाची पाहणी करणे आवश्यक असेल, तर त्याचे नमुने इष्ट दिशेने कापून त्या कापापासून तयार केलेल्या पातळ चकत्यांचे सूक्ष्मदर्शकाने परीक्षण करावे लागते. (२) तपासावयाच्या नमुन्याची ठिकरी किंवा कपची उगाळून, घासून तिची अगदी पातळ (०.०३ ते ०.०४ मिमी.) जाडीची चकती करून ती तपासतात. दगडाचा नमुना कापून त्याच्यापासून समांतर पृष्ठे असलेल्या चापट वडीसारख्या, सु. २.५ सेंमी. चौरस व एक मिमी. जाडीच्या चकत्या काढणारी यंत्रे उपलब्ध झाली आहेत. तशा चकत्या उगाळून पातळ छेद लवकर तयार करता येतात. तसे यंत्र नसेल तर, पुढील पद्धतीने पातळ छेद तयार करतात. छिन्नीने दगडाचा टवका काढून सु. तीन. सेंमी. व्यासाची व सु. एक मिमी. जाडीची ठिकरी किंवा कपची काढतात. तिची दोन्ही पृष्ठे अर्थात खडबडीत असून एकमेकांस समांतर नसतात. त्यांपैकी एक पृष्ठ सपाट तव्यावर किंवा काचेच्या तावदानावर पाणी व एमरीची पूड यांच्या मिश्रणात उगाळून ते पृष्ठ प्रथम सपाट करून घेतात. या कामासाठी भरड, मध्यम, बारीक व सूक्ष्म अशा चार प्रकारची एमरीची (किंवा कार्बोरंडमाची) पूड अनुक्रमे वापरतात. प्रत्येक पुडीसाठी वेगळा तवा वापरला जातो. प्रथम भरड पूड व पाणी असलेल्या तव्यावर ठिकरीचे एक पृष्ठ उगाळून घासतात. नंतर हे पृष्ठ अनुक्रमे अधिकाधिक बारीक पूड असलेल्या दुसऱ्या, तिसऱ्या व चौथ्या तव्यावर उगाळतात. यावेळी ठिकरीचे एक बाजू सपाट व गुळगुळीत झालेली असते. ती बाजू खाली करून ती ठिकरी एका काचपट्टीवर चिकटविली जाते. चिकटविण्यासाठी कॅनडा बाल्सम नावाचा डिंकासारखा पदार्थ वापरतात. तो प्रथम पातळ असतो, पण तापवून निवल्यावर घन होतो व लाखेप्रमाणे वस्तू चिकटवितो. नंतर ठिकरीचे उघडे पृष्ठ खाली करून ते घासण्याचे काम केले जाते.
प्रथम सर्वांत भरड व नंतर उत्तरोत्तर अधिक बारीक व शेवटी सूक्ष्म एमरी असलेल्या तव्यावर उगाळण्याचे
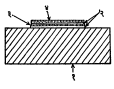
काम केले जाते. उगाळताना फक्त दगडाचे पृष्ठ घासले जाईल व काचपट्टी घासली जाणार नाही व काचपट्टी सपाट आडवी राहील अशी काळजी घ्यावी लागते. चकती किती पातळ करावयाची हे अनुभवाने समजते. चकती उगाळण्याच्या अखेरी अखेरीच्या अवस्थांत ती मधून मधून धुवून घेऊन सूक्ष्मदर्शकाने तपासून पाहतात. सूक्ष्मदर्शकाचे निकोल (ध्रुवित प्रकाश देणारे लोलक) जात्य असताना (एका निकोल लोलकाचे प्रमुख प्रतल दुसऱ्याच्या प्रमुख प्रतलाशी काटकोनात असल्यास पहिल्यातून बाहेर पडणारा ध्रुविंत प्रकाश दुसऱ्यातून पाहिल्यास नाहीसा होतो अशा स्थितीत) त्यांच्यामध्ये ठेवलेल्या खनिजांचे जे ध्रुवण रंग दिसतात त्यांवरून चकती पुरेशी पातळ झाली आहे की नाही ते कळते. ती पुरेशी पातळ झाली म्हणजे काचपट्टी आणि तिला चिकटविलेल्या ठिकरीची पातळ चकतीही स्वच्छ धुऊन सुकवितात. ती चकती सुरक्षित रहावी म्हणून ती एका पातळ (सु. ०.०१७ मिमी. जाड) काचेच्या तुकड्याने (काच-झाकणाने) झाकून टाकतात.
काच-झाकण चिकटविण्यासाठी कॅनडा बाल्सम वापरतात. अशी एक काचपट्टी व तिचा काल्पनिक छेद ही आ. १ मध्ये दाखविली आहेत. दोन्ही काचा व कॅनडा बाल्सम यांचा प्रणमनांक जवळजवळ सारखा म्हणजे सु. १.५४ असतो.
खनिजांच्या सूक्ष्म परीक्षणासाठी विशिष्ट प्रकारचे सूक्ष्मदर्शक वापरावे लागतात. त्यांची भिंगे सामान्य सूक्ष्मदर्शकांसारखीच असतात, पण त्यांच्यात दोन ध्रुवक बसविलेले असतात. हे ध्रुवक मंचाच्या खाली एक व वरच्या नळीत दुसरा अशा दोन कप्प्यांत अशा रीतीने बसविलेले असतात की, त्यांच्यामध्ये प्रकाश तरंगांच्या कंपनांच्या दिशा एकमेकींना काटकोन करतात. मंचाच्या वरच्या बाजूस असणाऱ्या ध्रुवकाला विश्लेषी ध्रुवक किंवा विश्लेषक म्हणतात. काही निरीक्षणांच्या वेळी त्यांपैकी एकच, सामान्यत: खालचा ध्रुवक वापरतात व विश्लेषक बाजूला केलेला असतो तर काही गुणधर्मांची परीक्षा करण्यासाठी दोन्ही ध्रुवक वापरून पाहिजे तेव्हा ते जात्य करण्याची सोय केलेली असते. सूक्ष्मदर्शकाच्या मंचकावर, वर्तुळाकार फिरू शकणारी एक गोल तबकडी बसविलेली असते तिला फिरता मंच म्हणतात. ज्याचे परीक्षण करावयाचे त्या खनिजाचे कण एका काचपट्टीवर घेऊन ती काचपट्टी फिरत्या मंचावर ठेवून सूक्ष्मदर्शकाने परीक्षण केले जाते. सूक्ष्मदर्शकाच्या साहाय्याने खनिजांच्या कोणत्या गुणधर्मांचे परीक्षण करता येते, याविषयी त्रोटक माहिती येथे दिली आहे.
प्रणमन : अपारदर्शक नसलेल्या खनिजावर प्रकाश पडला म्हणजे त्या प्रकाशाचा काही भाग खनिजाच्या पृष्ठापासून परावर्तित होतो आणि काही भागाचे प्रणमन (एका माध्यमातून दुसऱ्या माध्यमात जाताना प्रकाशाच्या दिशेत बदल होणे, वक्रीभवन) होते. प्रणमन हे खनिजांच्या घटक अणूंवर आणि त्यांच्या संरचनेवर अवलंबून असते. प्रत्येक खनिजाचा विशिष्ट प्रणमनांक असतो व त्याच्यावरून खनिज ओळखण्यास मदत होते. पारदर्शक खनिजांचे एकूण दृश्य म्हणजे त्यांच्या दिसण्याची ढब ही त्यांच्या प्रणमनांकावर अवलंबून असते. अतिशय कमी किंवा अतिशय जास्त प्रणमनांक असणारी खनिजे सामान्य खनिजांहून अगदी वेगळी उठावदार दिसतात. उदा., क्रायोलाइटाच प्रणमनांक १.३४१ हा इतर खनिजांच्या मानाने फारच कमी व जवळजवळ पाण्याच्या प्रणमनांकाइतका (१.३३५) असतो. ते पांढरे व ओलसर बर्फासारखे व इतर कोणत्याही पांढऱ्या खनिजापेक्षा वेगळे दिसते. हिरा (२.४१९), मौल्यवान रत्ने व सेऱ्युसाइटासारखी खनिजे त्यांच्या उच्च प्रणमनांकांमुळेच तेजस्वी दिसतात. सामान्य खनिजांचा प्रणमनांक १.५५ च्या जवळपास असतो व त्यांची चमक काचेसारखी असते.
खनिजांचा प्रणमनांक सामान्यत: त्यांच्या सूक्ष्मकणांचे परीक्षण करून ठरविला जातो. ज्याचा प्रणमनांक माहीत आहे अशा एखाद्या तेलाचे किंवा इतर द्रवाचे एक-दोन थेंब काचेच्या पट्टीवर ठेवून त्या द्रवात ज्याचा प्रणमनांक काढावयाचा आहे त्या खनिजाचे ४-६ कण बुडवून ठेवतात व काचपट्टी सूक्ष्मदर्शकाच्या मंचावर ठेवून त्या कणांचे निरीक्षण केले जाते. एखादे खनिज कसे दिसेल, हे त्या खनिजाच्या व ज्या द्रवात त्याचे कण बुडविलेले आहेत त्याच्या प्रणमनांकांतील फरकावर अवलंबून राहील. दोहोंचे प्रणमनांक जवळजवळ सारखे असले, तर खनिजांच्या कणांच्या कडा स्पष्ट दिसत नाहीत. ती दोन्ही रंगहीन किंवा सारख्याच रंगाची असली, तर खनिजाचे कण शेजारच्या द्रवात विरघळल्यासारखे दिसतात पण दोहोंचे प्रणमनांक भिन्न असले म्हणजे खनिजाच्या कडा स्पष्ट दिसतात. प्रणमनांकातील भेद जितका अधिक तितक्या खनिजांच्या कणांच्या कडा अधिक स्पष्ट दिसतात आणि ते उठून दिसते.
खनिजाचा प्रणमनांक तुलनात्मक पद्धतीने म्हणजे ज्यांचा प्रणमनांक अचूक माहीत आहे, अशा द्रवांचा उपयोग करून काढला जातो. ज्यांचा प्रणमनांक अचूक माहीत आहे, असे खाली उल्लेख केलेले द्रव किंवा त्यांची मिश्रणे प्रयोगशाळांत वापरली जातात. कंसात त्यांच्या प्रणमनांकांची अभिसीमा (मर्यादा) दिली आहे. निरनिराळी ऊर्ध्वपातित (वाफ करून व मग ती थंड करून अलग केलेली) खनिज तेले (१.३५ ते १.४५), टर्पेंटाइन व लवंगांचे तेल यांची मिश्रणे (१.४८ ते १.५३), लवंगांचे तेल व आल्फा मोनोब्रोमोनॅप्थॅलीन यांची मिश्रणे (१.५३ ते १.६५) आणि आल्फा मोनोब्रोमोनॅप्थॅलीन व मिथिलीन आयोडाइन यांची मिश्रणे (१.६५ ते १.७४).
वर उल्लेख केलेल्या द्रवांसारख्या किंवा मिश्र द्रवांसारख्या द्रवांपैकी एकेका द्रवात बुडविलेले एखाद्या
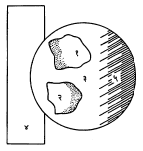
खनिजाचे कण पाहून कोणत्या द्रवात कणाच्या कडा दिसेनाशा होतात, हे सूक्ष्मदर्शकाने पाहतात. खनिजाचा प्रणमनांक हा ज्या द्रवात त्याच्या कणांच्या कडा दिसेनाशा होतात, त्या द्रवाच्या प्रणमनांकाइतका जवळजवळ असतो. प्रणमनांकाचे हे मूल्य स्थूल असते, पण खनिज ओळखण्यासाठी असे मूल्य सामान्यत: पुरेसे होते. खनिजाचा व द्रवाचा प्रणमनांक जवळजवळ सारखाच असताना व साध्या पांढऱ्या प्रकाशात निरीक्षण करीत असताना कणांच्या कडांशी रंगांच्या फिकट छटा दिसू लागतात. अशा वेळी सूक्ष्मदर्शकाचा मंच व त्याच्या खालचा आरसा यांच्यामध्ये, आरशाचा सु. अर्धा भाग झाकला जाईल अशा रीतीने पुठ्ठ्याचा एखादा तुकडा एका बाजूकडून आत सरकवून धरला म्हणजे मंचावरील काचपट्टीवर पडणारे बरेचसे किरण तिरपे पडतात. खनिजांच्या कणांच्या एका बाजूच्या कडेशी तांबूस व तिच्याविरुद्ध कडेशी निळसर रंग दिसू लागतो. अशा वेळी तांबूस व निळा या रंगांच्या मधे असणाऱ्या एखाद्या रंगाच्या बाबतीत द्रव खनिज यांचे प्रणमन समान असते. खनिजाचे कण व ते ज्याच्यात बुडविलेले असतात तो द्रव यांचे प्रणमन भिन्न असले म्हणजे कोणाचे प्रणमन अधिक आहे, हे ओळखण्यासाठी पुढील दोहोंपैकी एखादी पद्धती वापरली जाते.
(१) कण खडबडीत असले तर मध्यम वर्धनक्षमतेची सूक्ष्मदर्शक भिंगे वापरून व तिरपे प्रकाशन वापरून खनिजाचे सापेक्ष प्रणमन ठरविले जाते. सूक्ष्मदर्शकाच्या मंचाखाली उजव्या किंवा डाव्या बाजूने पुठ्ठ्याचा तुकडा किंचित सरकवून तिरपे प्रकाशन मिळविले जाते. अशावेळी सूक्ष्मदर्शकाने दिसणाऱ्या एकूण क्षेत्राच्या जवळजवळ अर्ध्या भागातच उजेड आणि उरलेल्या अर्ध्या भागात जवळजवळ अंधार असतो. मंचाखालचे संघनित्र (प्रकाश एकत्रित करून विशिष्ट दिशेने टाकण्यासाठी वापरले जाणारे भिंग) काढून टाकून खनिजाच्या एखाद्या कणावर संकेंद्रण (केंद्रीकरण, फोकसिंग) केले, तर त्या कणाच्या एका बाजूची कडा प्रकाशित दिसेल व दुसऱ्या बाजूच्या कडेशी काळोख दिसेल. ज्या बाजूने पुठ्ठ्याचा तुकडा सरकविला असेल त्याच्या विरुद्ध बाजूची कडा प्रकाशित असली म्हणजे खनिजाच्या कणाचा प्रणमनांक द्रवापेक्षा अधिक असतो. ज्या बाजूने पुठ्ठ्याचा तुकडा सरकविला असेल त्याच बाजूची कडा प्रकाशित असली म्हणजे खनिजाच्या कणाचा प्रणमनांक द्रवापेक्षा कमी असतो (आ. २).
(२) खनिजांच्या चुऱ्यातील कण पुष्कळ वेळा मध्यभागी फुगीर व कडेशी अधिक पातळ असतात.
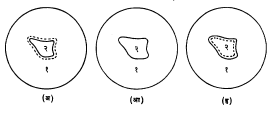
त्यांच्यासाठी पुढील पद्धती वापरतात : या पद्धतीत अधिक उच्च वर्धनक्षमतेची भिंगे वापरली जातात. मंचाखालचे संघनित्र काढून टाकले किंवा खाली केले जाते. कनीनिका पटलाचे (छिद्र लहान-मोठे करण्याची सोय असलेल्या पटलाचे) छिद्र बारीक करून प्रकाश अंधुक केला जातो. एखाद्या कणावर संकेंद्रण केले जाते, नंतर सूक्ष्म समायोजक (जुळविणारे) मळसूत्र फिरवून सूक्ष्मदर्शकाची नळी वेगाने वर उचलली व खाली केली जाते. नळी वरखाली होत असताना प्रकाशाची एक सूक्ष्म रेषा खनिजाच्या कणाच्या कडांपासून आत आलेली वा बाहेर गेलेली दिसते (आ.३). नळी वर उचलताना प्रकाशाची पांढरी रेषा खनिजात शिरली, तर खनिजाचा प्रणमनांक शेजारच्या द्रवापेक्षा अधिक असतो. नळी खाली करताना तशीच रेषा खनिजात शिरली, तर त्याचा प्रणमनांक शेजारच्या द्रवापेक्षा कमी असतो.
बेके पद्धती : खनिजाच्या कणाची कडा सरळ उभी असली म्हणजे खनिज व त्याच्याशी संपर्क येणारा द्रव यांच्या संपर्काचे समतल सरळ उभे असले म्हणजे ही पद्धत वापरता येते. पण सामान्यत: ती पातळ चकत्यांतील खनिजांसाठी वापरली जाते. अशा चकत्यांतील खनिजांची जाडी इतकी अल्प असते की, खनिजांच्या कडा व दोन खनिजांमधील किंवा एखादे खनिज आणि चकती चिकटविण्यासाठी वापरलेले कॅनडा बाल्सम यांच्या संपर्काचे समतल उभे असते. या पद्धतीने एखाद्या खनिजाचा प्रणमनांक त्याच्या लगतच्या खनिजापेक्षा किंवा कॅनडा बाल्समापेक्षा कमी अथवा जास्त आहे एवढेच कळते. पण तेवढी माहितीही उपयुक्त ठरते. उदा., कित्येक खडकांत क्वॉर्ट्झ व ऑर्थोक्लेज ही दोन्ही खनिजे असतात व त्यांचे पुष्कळ तुकडे अगदी सारखेच दिसतात. पण क्वॉर्ट्झाचा प्रणमनांक कॅनडा बाल्समापेक्षा अधिक व ऑर्थोक्लेजाचा निश्चित कमी असल्यामुळे बेके यांची पद्धती वापरून त्यांच्यात अनायासे भेद करता येतो. चकत्यांमधील काही खनिजे सहज ओळखता येतात. त्यांचा व एखाद्या अज्ञात खनिजाचा संपर्क आलेला असेल, तर बेके पद्धती वापरून अज्ञान खनिजाचा प्रणमनांक ज्ञात खनिजापेक्षा कमी किंवा अधिक आहे, हे कळते आणि त्या माहितीचा उपयोग अज्ञात खनिज ओळखण्यासाठी होतो.
बेके पद्धतीत कनीनिका पटलाचे छिद्र बारीक करून प्रकाश अंधुक केला जातो व अधिक उच्च वर्धनक्षमतेची भिंगे वापरली जातात. मंचाखालचे संघनित्र काढून टाकले किंवा खाली केले जाते. ज्यांच्या प्रणमनांकांची तुलना करावयाची त्यांच्या संपर्काच्या रेषेवर संकेंद्रण केले जाते. नंतर सूक्ष्म समायोजक मळसूत्र फिरवून सूक्ष्मदर्शकाची नळी वरखाली केली जाते. नळी वरखाली होत असताना एक सूक्ष्म पांढरी रेषा संपर्काच्या सांध्यापासून एका किंवा दुसऱ्या बाजूच्या पदार्थात गेलेली दिसते. नळी वर उचलताना प्रकाशाची पांढरी रेषा ज्या पदार्थात शिरलेली दिसते त्याचा प्रणमनांक अधिक उच्च असतो.
अपस्करण : वर्णपटातील निरनिराळ्या रंगांच्या प्रकाशाच्या प्रणमनाचे मान निरनिराळे असते. तांबड्या टोकावरील रंगांपेक्षा जांभळ्या टोकाकडील रंगांचे प्रणमन अधिक असल्यामुळे तांबड्या किरणांचे अपगमन (सरकणे) कमी व जांभळ्या किरणांचे त्यांच्याहून अधिक असते. तांबड्या आणि जांभळ्या रंगांच्या प्रणमनांकांमधील फरकाला अपस्करण म्हणतात. प्रत्येक खनिजामुळे सामान्यत: थोडे तरी अपस्करण घडून येते, पण कित्येकांत ते पुष्कळ असते. सर्वांत कमी अपस्करणता असलेले खनिज म्हणजे फ्ल्युओरस्पार (०.००८६८) व सर्वांत जास्त म्हणजे हिरा (०.०५७४१) होय. एखाद्या लोलकातून बाहेर पडणाऱ्या किरणांसारखे अनेक तेजस्वी किरण पैलू पाडलेल्या हिऱ्यातून बाहेर पडलेले दिसतात ते त्याच्या उच्च अपस्करणामुळेच. हिऱ्याला अशा खुबीने पैलू पाडलेले असतात की, त्याच्यातून अधिकात अधिक अपस्कारित किरण बाहेर पडावेत. प्ल्युओरस्पाराला तसेच पैलू पाडले तरी त्याचे स्फटिक निस्तेज, सफेद दिसतात.
वर उल्लेख केलेल्या व साधा प्रकाश वापरून काढलेल्या पद्धतींनी खनिजांचे प्रणमनांक स्थूल मानाने कळतात. सामान्य परीक्षणात खनिज ओळखून काढणे हाच हेतू असतो व त्यासाठी वरील पद्धतींनी मिळणारे प्रणमनांकाचे मूल्य पुरेसे होते. परंतु एखाद्या खनिजाच्या गुणधर्मांचे अचूक मापन करावयाचे असेल आणि त्याचा यथातथ्य प्रणमनांक ठरवावयाचा असेल, तर काही खास पद्धती वापरतात. उदा., एकवर्णी प्रकाश देणारा दिवा वापरून खनिजाचे निरीक्षण केले जाते. खनिजाचा प्रणमनांक सामान्यत: सोडियम दीपाच्या पिवळ्या प्रकाशाच्या संदर्भाने दिला जातो.
खनिजांचे प्रणमन काढताना पुढील गोष्टी लक्षात ठेवाव्या लागातात. (१) अस्फटिकी पदार्थांत व घनीय स्फटिकांत एकच प्रणमन असते. ते ठरविण्यासाठी त्याचे कोणतेही कण किंवा छेद चालतात, (२) घनीय स्फटिकांखेरीज इतर स्फटिकांत द्विप्रणमन असते. प्रणमनाने निर्माण झालेल्या दोन किरणांच्या प्रणमनाचे मापन करण्यासाठी काही विवक्षित स्थिती असलेले कण किंवा विवक्षित दिशांनी घेतलेले छेद वापरावे लागतात. तसे छेद निरीक्षणासाठी घेतलेल्या चुऱ्यात किंवा चकत्यांत असतीलच असे नाही. अशा खनिजांच्या कणांची पाहणी करून प्रणमनाचे स्थूल मूल्य मिळत असते. अचूक मापनासाठी विविक्षित कण किंवा छेद मुद्दाम मिळवून वापरावे लागतात.
समदिक् पदार्थ : कोणत्याही वायूतून, द्रवातून किंवा काचेतून प्रकाश जात असताना त्या पदार्थातील कोणतीही दिशा ही प्रकाशाची कंपनदिशा असू शकते. घनीय स्फटिकातील सर्व दिशा समान व एकमेकींशी तुल्य असतात. त्यांच्यातील कोणतीही दिशा ही प्रकाशाची कंपनदिशा असू शकते. वायू, द्रव, काच आणि घनीय स्फटिक हे सर्व पदार्थ एक प्रणमनी असतात. त्यांचे प्रणमन दिशानिरपेक्ष असते. कोणत्याही एका पदार्थातील सर्व दिशांस ते सारखेच असते. या सर्व पदार्थांना समदिक् म्हणतात.
असमदिक् पदार्थ : घनीय स्फटिकांखेरीज इतर कुठल्याही समूहातील स्फटिकातून जाणाऱ्या प्रकाशाचा वेग म्हणजे प्रकाशाच्या प्रसारणाचे मान सर्वत्र सारखे असत नाही व निरनिराळ्या दिशांत निरनिराळे असते, म्हणून त्यांना असमदिक् पदार्थ म्हणतात. त्यांच्यातून प्रसारित होणाऱ्या किरणांचे द्विप्रणमन होते म्हणजे प्रत्येक किरणापासून दोन किरण निर्माण होतात व त्या किरणांच्या कंपनदिशा एकमेकींस लंब असतात. घनीयखेरीज इतर सर्व स्फटिक द्विप्रणमनी असतात. अशा पदार्थांतील कोणत्याही दिशा कंपनाच्या दिशा असू शकत नाहीत, तर स्फटिकातील काही विशिष्ट दिशांतच कंपन होते. कंपनाच्या दिशांचे व स्फटिकांच्या अक्षांचे निश्चित संबंध असतात.
असमदिक् पदार्थाचे एकाक्षीय आणि द्वि-अक्षीय असे दोन विभाग आहेत. एकाक्षीय पदार्थांत चतुष्कोणीय व षट्कोणीय स्फटिकांचा व द्वि-अक्षीय पदार्थांत समचतुर्भुजी, एकनताक्ष व त्रिनताक्ष स्फटिकांचा समावेश होतो [→ स्फटिकविज्ञान].
रंगबदल : (प्लीओक्रोइझम). काही द्विप्रणमनी खनिजांचे (उदा., कृष्णाभ्रक, तोरमल्ली) c अक्षाला समांतर असणारे छेद सूक्ष्मदर्शकाखाली ध्रुवित प्रकाशात तपासले असता असे दिसते की, खनिज ठेवावयाचा मंच फिरविला असता या खनिजांचा रंग बदलतो. हे बदल तीव्रता किंवा रंगाचा प्रकार असा दोन्ही प्रकारचा असू शकतो. अशा खनिजांना रंगबदली खनिजे म्हणतात. खनिजांतील विशिष्ट स्फटिक अक्षांच्या दिशेने प्रवास करणाऱ्या प्रकाशकिरणांपैकी सर्व किंवा काही विशिष्ट तरंगलांबीच्या किरणांचे शोषण करण्याच्या गुणामुळे रंगबदल घडून येतो [→ नैकवर्णता].
एकाक्षीय पदार्थ : यांच्या द्विप्रणमनाने निर्माण झालेल्या दोन किरणांपैकी एका किरणाचे कंपन सर्व दिशांत सारखेच सुकर असते व त्याच्या प्रसारणाचा वेग सर्वत्र सारखा असतो. त्याला सामान्य किरण म्हणतात व तो O (ओ) या चिन्हाने दर्शवितात. प्रणमनाने निर्माण झालेल्या दुसऱ्या किरणाला असामान्य किरण म्हणतात व तो E या चिन्हाने दर्शवितात. तो स्फटिकातील निरनिराळ्या दिशांस निरनिराळ्या वेगांनी जातो, पण स्फटिकाच्या c अक्षाच्या दिशेस त्याचा व सामान्य किरणाचा वेग सारखाच असतो. त्या दिशेने द्विप्रणमन होत नाही, म्हणून c अक्षाला समदिक्तेचा अक्ष किंवा प्रकाशीय अक्ष म्हणतात. चतुष्कोणीय व षट्कोणीय स्फटिकांत एकच प्रकाशीय अक्ष असतो, म्हणून त्यांना एकाक्षीय स्फटिक म्हणतात. प्रकाशीय अक्षांची दिशा ही स्फटिकाच्या c अक्षाची दिशा असते.
एकाक्षीय स्फटिकांचे दोन प्रकार आहेत. एका प्रकारात c अक्षाची दिशा ही असामान्य किरणाच्या सर्वांत अधिक सुकर कंपनाची दिशा असते. अशांना ॠण (-) स्फटिक म्हणतात. दुसऱ्या प्रकारात c अक्षाची दिशा ही असामान्य किरणाच्या सर्वांत कमी सुकर कंपनाची दिशा असते. अशांना धन (+) स्फटिक म्हणतात.
द्वि-अक्षीय स्फटिक : याच्या प्रणमनाने निर्माण झालेल्या दोन्ही किरणांच्या प्रणमनाचे मान अर्थात त्यांच्या प्रसारणाचा वेग ही दिशापरत्वे बदलत असतात पण स्फटिकात दोन दिशा अशा असतात की, ज्यांस अनुसरुन दोघांचा वेग सारखाच असतो आणि द्विप्रणमन होत नाही. म्हणजे या स्फटिकात दोन प्रकाशीय अक्ष असतात म्हणून द्वि-अक्षीय म्हणतात. त्या दोन अक्षांमधील कोन खनिजाच्या जातिपरत्वे निरनिराळा असतो व अक्षांमधील कोनाच्या मूल्यावरुन खनिज ओळखण्यास मदत होते. त्याचे मूल्य अगदी कमी १° ते २° वा फार जास्त ८०° किंवा अधिक असू शकते. सामान्यत: त्या दोन अक्षांमधील एक कोन लघू व दुसरा विशाल असतो. त्या कोनांच्या दुभाजक रेखांपैकी एक रेखा ही त्या स्फटिकातील शीघ्रतम कंपनाची व दुसरी मंदतम कंपनाची दिशा असते. लघुकोन दुभाजकाची दिशा ही मंदतम कंपनाची दिशा असेल, तर त्या स्फटिकास धन (+) व लघुकोन विभाजकाची दिशा शीघ्रतम कंपनाची दिशा असेल, तर त्या स्फटिकास ॠण (-) स्फटिक म्हणातात.
विलोपन : ध्रुवण सूक्ष्मदर्शकाखाली खडकांच्या किंवा खनिजांच्या पातळ छेदांची पाहाणी करताना असे दिसते की, जात्य निकोलात बहुतेक खनिजांच्या छेदांत नानाविध रंग दिसतात. मुळात ते खनिज (उदा., क्वॉर्ट्झ, फेल्स्पार) रंगहीन असले, तरीही त्याच्या छेदात हे रंग दिसतात. मात्र मंच उभ्या अक्षाभोवती गोल फिरवला असता खनिजाचे हे रंग काही विशिष्ट स्थितींत नाहीसे होऊन ते खनिज पूर्णपणे अंधारमय वा काळे दिसते. जात्य निकोलात पाहणी करताना मंचाच्या एका पूर्ण फेरीत प्रत्येक खनिजाचा छेद चार वेळा काळा होतो अशा स्थितीला विलोपन म्हणतात.
जात्य निकोलात दिसणारे खनिजांचे रंग असमदिक् खनिजांच्या छेदातून भिन्न वेगाने प्रवास करणाऱ्या दोन प्रकाशकिरणांच्या व्यतिकरणामुळे (किरण एकमेकांवर पडल्यामुळे) निर्माण झालेले असतात. सर्व द्विप्रणमनी खनिजे असमदिक् असल्यामुळे अशा खनिजांच्या छेदांतच व्यतिकरण रंग दिसतात. समदिक् खनिजांमध्ये प्रकाशाचे द्विप्रणमन होत नसल्यामुळे व्यतिकरण होत नाही. अशा खनिजांच्या छेदांत खालच्या ध्रुवकातून आलेले प्रकाशकिरण त्यांच्या कंपनदिशेत कोणताही बदल न करता खनिजातून पार जातात. पुढे विश्लेषकापाशी हे किरण आल्यावर विश्लेषकातील कंपनदिशा किरणांच्या कंपनदिशेशी काटकोनात असल्यामुळे हे किरण तेथे पूर्णपणे अडवले जातात. परिणामी समदिक् खनिजाचा छेद काळा दिसतो. मंच फिरविताना हे छेद सर्वकाळ विलोपन स्थितीत राहतात. असमदिक् खनिजांपैकी चतुष्कोणी व षट्कोणी म्हणजे एकाक्षीय खनिजांच्या c अक्षाला लंब दिशेत कापलेल्या छेदामध्येही द्विप्रणमन होत नसल्यामुळे असे छेद संपूर्ण मंचाच्या फेरीत सर्वकाळ विलोपन स्थितीत राहतात.
असमदिक् खनिजांच्या c अक्षाला लंब दिशा सोडून इतर दिशांत कापलेल्या सर्व छेदांत जात्य निरनिराळे व्यतिकरण रंग दिसतात. मंचाच्या संपूर्ण फेरीत चार वेळा हे छेद विलोपन स्थितीमध्ये येतात. मंच फिरविण्याचा कोन मोजला तर असे दिसते की, पहिल्या विलोपन स्थितीपासून पुढची प्रत्येक विलोपन स्थिती ९० अंश कोनाच्या अंतराने येते.
खनिजाचा छेद जेव्हा विलोपन स्थितीत असतो तेव्हा त्या छेदातील दोन प्रकारच्या (सामान्य व
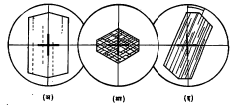
असामान्य) प्रकाशकिरणांच्या कंपनदिशा दोन्ही ध्रुवकांपैकी कोणत्या ना कोणत्या ध्रुवकाच्या कंपनदिशेला समांतर व काटकोनात अशा असतात. त्यामुळे खालच्या ध्रुवकातून येणारे ध्रुवित प्रकाशकिरण खनिजाच्या छेदातून प्रवास करताना त्यांच्याशी समांतर दिशा असणाऱ्या – सामान्य किंवा असामान्य – अशा एका प्रकाशकिरणाच्या रुपात खनिजातून पार जातात. त्यांच्या कंपनदिशेत कोणताही बदल न होता ते विश्लेषकापाशी आल्यावर विश्लेषकातील कंपनदिशा त्यांच्या कंपनदिशेशी काटकोनात असल्यामुळे तेथे हे किरण अडवले जाऊन खनिजाचा छेद काळा दिसतो.
खनिजाचा छेद विलोपन स्थितीत असताना त्या खनिजाची स्फटिकरुपात्मक विशिष्ट दिशा (उदा., प्रमुख पाटन, प्रचिनाच्या लांब कडांच्या स्वरुपात दिसून येणारी c अक्षाची दिशा इ.) उभ्या किंवा आडव्या लंघक तंतूंना (अचूक संकेंद्रण करण्यासाठी एकमेकांना काटकोनात असणाऱ्या सूक्ष्मदर्शकातील तंतूंना) म्हणजेच खालच्या आणि वरच्या ध्रुवकांच्या कंपनदिशांना समांतर असेल, तेव्हा त्या स्थितीला सरळ विलोपन म्हणतात. त्याच्या उलट स्फटिकरुपाची महत्त्वाची कड किंवा पाटन दिशा लंघक तंतूशी काही कोन करीत असेल तेव्हा त्या स्थितीला तिर्यक् विलोपन म्हणतात. विलोपन स्थितीत खनिजाचा छेद असताना त्याच्यात दिसणाऱ्या दोन गटांच्या पाटनातील कोन (उदा., प्रचिनाकार पाटन) लंघक रेषांनी दुभागला असल्यास त्याला सममित विलोपन म्हणतात (आ. ४). तिर्यक् विलोपनाचा कोन ते खनिज ओळखण्याच्या दृष्टिने उपयोगी पडतो. उदा., हॉर्नब्लेंडाच्या a व c अक्षप्रतलांना समांतर (010) छेदाच्या विलोपनाचा कोन १२° ते ३०° पर्यंत असतो, तर ऑजाइटाच्या अशा छेदांच्या विलोपनाचा कोन ४५° असतो.
सर्व समदिक् म्हणजे घनीय खनिजे व नैसर्गिक काच जात्य निकोलात मंचाच्या संपूर्ण फेरीत सर्वकाळ विलोपन स्थितीत राहतात, त्याचप्रमाणे चतुष्कोणी आणि षट्कोणी खनिजांचे c अक्षाला लंब असणारे छेदही सर्वकाळ विलोपन स्थितीत राहतात. चतुष्कोणी आणि षट्कोणी खनिजांचे इतर दिशांत असणारे छेद व समचतुर्भुजी खनिजांचे त्यांच्या कोणत्याही स्फटिक अक्षाला समांतर असणारे छेद सरळ विलोपन दाखवितात. एकनताक्ष खनिजांच्या b अक्षाला समांतर असणाऱ्या (ऑर्थो) छेदातही सरळ विलोपन दिसते. एकनताक्ष खनिजांचे (010) प्रतलाला समांतर छेद, त्रिनताक्ष खनिजांचे बहुतेक सर्व छेद तिर्यक् विलोपन दाखवितात. खनिजनिश्चितीसाठी ही माहिती उपयुक्त ठरते.
व्यतिकरण रंग : असमदिक् खनिजांच्या छेदांचे जात्य निकोलात परीक्षण करताना छेदातील प्रकाशकिरणांच्या कंपनदिशा ध्रुवक वा विश्लेषकाच्या कंपनदिशांना समांतर असतील तेव्हा अशा स्थितीतील छेद विलोपन दाखवतो. पण मंच फिरवल्यावर छेदातील कंपनदिशा ध्रुवक आणि विश्लेषकातील कंपनदिशांशी काही कोन करतात. अशा स्थितीतील छेदात निरनिराळ्या रंगछटा दिसतात. जेव्हा खनिजाच्या छेदातील कंपनदिशांचा खालच्या व वरच्या ध्रुवकांतील कंपनदिशांशी ४५° कोन होतो, त्या स्थितीत या रंगाची तीव्रता सर्वांत जास्त असते. मंच आणखी पुढे फिरविल्यास हे रंग मंद होऊ लागून पुन्हा छेदातील कंपनदिशा ध्रुवकांच्या कंपनदिशांना समांतर झाल्या की, छेदाची विलोपन स्थिती येते. द्विप्रणमनी खनिजांच्या सामान्य व असामान्य किरणांच्या परस्पर व्यतिकरणामुळे हे रंग निर्माण होत असल्यामुळे यांना व्यतिकरण रंग तसेच ध्रुवण रंग असेही म्हणतात. हे रंग मंद करडा, फिकट पिवळा यांपासून तो भडक नारिंगी, लाल, निळा, हिरवा याप्रमाणे वाढत गेलेले दिसतात. या रंगांच्या विशिष्ट क्रमाने वाढत गेलेल्या चढत्या श्रेणीला न्यूटन रंगश्रेणी म्हणतात (पहा शेजारील सारणी). या श्रेणीतील सर्वांत खालचा रंग अत्यंत मंद, धूसर करडा असतो. रंगांच्या चढत्या पायऱ्यांनुसार श्रेणीचे विभाग पाडले आहेत. त्यांना कोटी म्हणतात. पहिल्या कोटीचे रंग फिके व मंद असून दुसऱ्या व तिसऱ्या कोटींचे रंग सर्वांत भडक व तीव्र असतात. चौथ्या कोटीपासून पुढचे रंग पुन्हा फिकट व पांढरट होतात. प्रत्येक कोटीतील शेवटचा रंग लाल किंवा लालाची छटा असलेला असा असतो. सर्वसामान्य खडकांच्या प्रमाणभूत जाडीच्या छेदातील खनिजांचे व्यतिकरण रंग पहिल्या तीन कोटींचे असतात.
व्यतिकरण रंग हे प्रामुख्याने खनिजाचे द्विप्रणमन मूल्य, खनिजाच्या छेदाची जाडी व छेदाची दिशा या तीन घटकांवर अवलंबून असतात.
द्विप्रणमनी खनिजांच्या छेदातून प्रवास करताना सामान्य आणि असामान्य किरणांचा वेग निरनिराळा असतो आणि छेदातून दोन्ही किरण बाहेर पडतात तेव्हा त्यांच्यातील एक किरण तरंगलांबीच्या कलेच्या (एखाद्या संदर्भाच्या सापेक्ष असणाऱ्या अवस्थेच्या) बाबतीत दुसऱ्या किरणाच्या मागे पडलेला असतो. दोन किरणांच्या कलेत पडलेल्या या अंतराला विलंबन म्हणतात. या विलंबनामुळेच विश्लेषकातून प्रवास करताना दोन किरणांचे व्यतिकरण होऊन रंगनिर्मिती होते.
|
न्यूटन रंगश्रेणी : |
||
|
पहिली कोटी |
गर्द काळसर करडा |
|
|
दुसरी कोटी |
जांभळा |
भडक व तीव्र रंग |
|
तिसरी कोटी |
निळा |
|
|
चौथी व वरच्या कोटी |
फिकट हिरवट व फिकट गुलाबी रंगांच्या छटा |
फिकट रंग |
दोन किरणांच्या कलेत पडणाऱ्या या अंतराची म्हणजे विलंबनाची तुलना धावण्याच्या शर्यतीत भाग घेणाऱ्या दोन स्पर्धकांत पडणाऱ्या अंतराशी करता येईल. शर्यतीत एकाच स्थानापासून आणि एकाच क्षणी धावण्यास सुरुवात करणाऱ्या दोन स्पर्धकांच्या वेगांत फरक असेल, तर थोड्याच वेळात त्या दोघांत अंतर पडू लागेल. हे अंतर त्या दोन स्पर्धकांच्या धावण्याच्या वेगांतील फरक आणि एकूण शर्यतीचा पल्ला या दोन घटकांवर अवलंबून राहील. जितका पल्ला मोठा तितके दोघांत पडणारे अंतर जास्त. तसेच पल्ला ठराविक असेल, तर दोघांच्या वेगांतील फरक जितका जास्त तितके अंतर जास्त पडेल. खनिजात घडून येणाऱ्या प्रकाशकिरणांच्या विलंबनाच्या बाबतीत वेगांतील फरक म्हणजे दोन किरणांच्या प्रणमनांकांतील फरक व शर्यतीचा पल्ला म्हणजे छेदाची जाडी असे म्हणता येईल, त्यामुळे घडून येणारे विलंबन वि = जा (प्र१-प्र२) या सूत्राने देता येते. या सूत्रात वि = विलंबन, जा = छेदाची जाडी व प्र१, प्र२ हे त्या खनिजाचे दोन किरणांचे प्रणमनांक होत.
खनिजाच्या छेदाची स्फटिक अक्षांच्या संदर्भातील दिशा वेगवेगळी असल्यासही व्यतिकरण रंगात फरक पडतो. क्वॉर्ट्झ, तोरमल्ली, झिर्कॉन यांसारख्या एकाक्षीय खनिजांचे c अक्षाला लंब दिशेत कापलेले छेद घेतल्यास त्यांच्यात द्विप्रणमन होत नसल्यामुळे व्यतिकरण होत नाही व हे छेद जात्य निकोलात मंचाच्या संपूर्ण फेरीत नेहमी विलोपन स्थितीत राहतात. त्याच्या उलट या खनिजाच्या उभ्या म्हणजे c अक्षाला समांतर असणाऱ्या छेदातून जाणाऱ्या सामान्य व असामान्य किरणांच्या वेगांत सर्वांत जास्त फरक असल्याने अशा छेदात सर्वांत जास्त कोटीचे व्यतिकरण रंग दिसतात. सर्वसामान्य प्रमाणभूत काचपट्टिकांतील छेदाची जाडी ०.०३ मिमी. असते. त्यामुळे विविध खनिजांत दिसणारे व्यतिकरण रंग त्या खनिजांच्या द्विप्रणमनांक मूल्यांवर आणि छेदाच्या दिशेवरच अवलंबून राहतात.
व्यतिकरण रंग दोन प्रकाशकिरणांच्या परस्पर सापेक्ष विलंबनावर अवलंबून असतात. हे विलंबन मोजता येते. विलंबनाचे एकक अत्यंत सूक्ष्म म्हणजे प्रकाशाच्या तरंगलांबीशी तुल्य असे μ μ (एक दशलक्षांश मिमी.) हे वापरतात. विलंबनाचे मूल्य विशिष्ट व्यतिकरण रंगाच्या छटेत सांगता येते. उदा., २७० µ µ विलंबनामुळे प्रथम कोटीचा फिकट पिवळा रंग मिळतो. छेदाची जाडी माहीत असल्यास विलंबन मूल्यावरुन त्या खनिजाच्या द्विप्रणमनाचे मूल्य काढता येते. खनिजनिश्चितीच्या कामात व्यतिकरण रंग उपयुक्त ठरतात.
व्यतिकरण आकृती : ध्रुवण सूक्ष्मदर्शकाखाली खनिजांचे परीक्षण करताना उच्च वर्धन शक्तीचे वस्तुभिंग
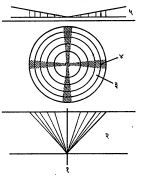
वापरून व खालून येणारा प्रकाश संघनित्राने केंद्राभिमुखी करुन जात्य निकोलात खनिजांचे छेद पाहिले असता त्यांच्यात काही विशिष्ट आकृती तयार झालेल्या दिसतात. त्यांना व्यतिकरण आकृती म्हणतात. मंचाखाली असणारे साहाय्यक संघनित्र वापरले म्हणजे खालून येणाऱ्या प्रकाशकिरणांचा खनिजाच्या छेदाकडे केंद्रित होणारा शंकू तयार होतो. खनिजाच्या छेदाची जाडी जरी सर्वत्र सारखी असली, तरी खालून येणारे किरण शंकूसारखे तिरके येत असल्यामुळे जितके किरण जास्त तिरके तितका त्यांना अधिक जाडीच्या छेदातून प्रवास करावा लागतो. त्यामुळे छेदाच्या मध्यापासून चोहोबाजूंना छेदाची जाडी पाचरीसारखी वाढावी असा परिणाम घडून येतो (आ. ५) आणि मध्यापासून कडेपर्यंत प्रकाशकिरणांचे विलंबन क्रमाक्रमाने वाढत जाते त्यानुसार व्यतिकरण रंगही वाढत जातात. मंचावर एखादा एकाक्षीय खनिजाचा c अक्षाला लंब दिशेत कापलेला (आधार तलानुसारी) छेद ठेवून पाहिल्यास खालून येणाऱ्या शंक्वाकृती किरणांपैकी मध्यभागातून येणारे किरण छेदाला लंब दिशेने येत असल्यामुळे त्यांच्यात द्विप्रणमन होत नाही. त्यामुळे छेदाचा मध्यभाग काळा दिसतो. पण जे किरण तिरके येतात, त्यांचे मात्र सामान्य आणि असामान्य किरणांत विभाजन होऊन व्यतिकरण घडून येते. हे व्यतिकरण मध्याशी म्हणजे प्रकाशीय अक्षाच्या दिशेने शून्य असून जो जो मध्यापासून दूर कडेला जावे तो तो वाढत गेलेले दिसते. लंघक तंतूंना समांतर कंपन दिशा असणारे किरण छेदातून बाहेर पडल्यावर विश्लेषकापाशी अडवले जातात त्यामुळे लंघक
तंतूंना समांतर बाहू असणारी अशी विलोपन फुली तयार होते. इतर क्षेत्रात मात्र कंपनदिशा लंघक तंतूंशी काही कोन करतात तेथे व्यतिकरण रंगांची एककेंद्री (एकाच केंद्राभोवती असणारी) वलये दिसतात. या वलयांतील रंगांची कोटी मध्यापासून कडेला वाढत गेलेली असते. मंचाच्या संपूर्ण फेरीत ही विलोपन फुली व सभोवतीची रंगीत वलये यांच्या स्थानांत बदल होत नाही.
सूक्ष्मदर्शकाने दिसणाऱ्या नेहमीच्या प्रतिमेपेक्षा वेगळ्या पातळीवर व्यतिकरण आकृती तयार होते. त्यामुळे ती पाहण्यासाठी नेत्रभिंग काढून पाहणे किंवा सूक्ष्मदर्शकाच्या नळीत नेत्रभिंगाच्या खाली बर्ट्रंड भिंग नावाचे विशेष भिंग बसविलेले असते, त्याचा वापर करणे आवश्यक ठरते. नेत्रभिंग काढून दिसणारी व्यतिकरण आकृती स्पष्ट, रेखीव पण लहान दिसते. बर्ट्रंड भिंगाचा उपयोग करुन दिसणारी व्यतिकरण आकृती मोठी, पण काहीशी अरेखीव दिसते.
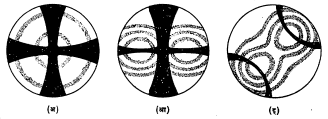
द्विप्रणमनी खनिजांचा कोणत्याही दिशेत कापलेला छेद घेतला, तरी त्याच्यात कसली ना कसली तरी व्यतिकरण आकृती दिसतेच. परंतु या अनेक प्रकारच्या छेदांपैकी खनिजांचे जे छेद प्रकाशीय अक्षाला लंब असतील अशी किंवा द्वि-अक्षीय खनिजांमध्ये लघुद्विभाजक अक्षाला लंब असतील अशा छेदात दिसणाऱ्या व्यतिकरण आकृती त्या त्या खनिजांची माहिती मिळविण्यासाठी विशेष उपयुक्त ठरतात. प्रत्येक व्यतिकरण आकृतीत एककेंद्री रंगीत वलये आणि त्यांना छेदून जाणारे छायेसारखे काळे छायापथ (आयसोगायर) दिसतात, हे छायापथ कधी काटकोनी फुलीप्रमाणे तर कधी दोन अपास्तीय [हायपरबोलिक → अपास्त] वक्रांच्या आकाराचे असतात (आ. ६).
केंद्रित एकाक्षीय व्यतिकरण आकृतीत छायापथांची फुली दिसते. केंद्रीत द्वि-अक्षीय व्यतिकरण आकृतीत सूक्ष्मदर्शकाच्या दृश्यक्षेत्रामध्ये दोन्ही प्रकाशीय अक्षांची टोके असतात. खनिजाच्या छेदाच्या मध्याशी लघुद्विभाजक अक्षाचा बिंदू असून त्याच्या दोन्ही बाजूंना समान अंतरावर प्रकाशीय अक्षांची टोके बाहेर आलेली दिसतात. मंच फिरविताना प्रकाशीय अक्ष छेदातून बाहेर पडण्याचे बिंदू केंद्राशी असावेत, अशा प्रकारे त्यांच्याभोवती अपास्तीय आकाराचे छायापथ फिरत राहतात. मंचाच्या फेरीत एका विशिष्ट स्थितीत दोन्ही छायापथांची मिळून एक फुली होते. ही फुली सदृश: एकाक्षीय व्यतिकरण फुलीसारखी दिसत असली, तरी मंच जरा मागे-पुढे फिरविला की, ही फुली मोडून दोन्ही छायापथ एकमेकांपासून सुटे होऊन त्यांचे अपास्तीय वक्र तयार होतात [आ. ६ (इ)].
व्यतिकरण आकृतींच्या साहाय्याने एकाक्षीय आणि द्वि-अक्षीय खनिजांची प्रकाशीय चिन्हे ठरविणे, तसेच त्यांच्या छेदांतील स्फटिक अक्षांच्या दिशा व त्यांचे प्रकाशीय कंपनदिशांशी असणारे संबंध इ. माहिती मिळविता येते. खनिज निश्चित करण्याच्या कामी या माहितीचा विशेष उपयोग होतो.
खनिज निदान किंवा खनिज अभिज्ञान : म्हणजे खनिज ओळखणे. खनिजांचे गुणधर्म देणाऱ्या सारण्या तयार करण्यात आलेल्या आहेत. त्या सारण्यांत सामान्यत: धातवीय व अधातवीय चमक असणाऱ्या खनिजांचे दोन प्रमुख विभाग केलेले असतात. नंतर कसाचा रंग लक्षात घेऊन त्या विभागांचे उपविभाग केलेले असतात. प्रत्येक उपविभागात उत्तरोत्तर अधिक कठिनता असणाऱ्या खनिजांचे नावे दिलेली असतात व त्या नावांसमोर खनिजांचे रंग, ठेवण, विशिष्ट गुरुत्व इ. गुणधर्म दिलेले असतात. कठिनता, विशिष्ट गुरुत्व यांसारख्या एकेका गुणधर्मावर आधारलेल्या सारयाही असतात. खनिजाचा एखादा नवा नमुना हाती आल्यावर त्याच्या भौतिक गुणधर्मांच्या साहाय्याने व कधीकधी फुंकनळी कसोट्या वापरुन सामान्य खनिजे ओळखता येतात. सूक्ष्मदर्शकाने दिसणाऱ्या खनिजांच्या गुणधर्मांवर आधारलेल्या सारण्याही उपलब्ध आहेत व अधिक काटेकोर माहितीसाठी त्या वापरल्या जातात. क्ष-किरणांच्या उपयोगावर आधारलेल्या सारण्याही क्वचितच लागतात व त्याही उपलब्ध आहेत.
क्रमिक सहजनन खनिजविज्ञान : या विभागामध्ये खनिजाच्या क्रमिक सहजननाचा म्हणजे निरनिराळ्या खडकांत एकत्र आढळणाऱ्या किंवा साहचर्य असणाऱ्या खनिजांचा व त्यांच्या स्फटिकीभवनाच्या क्रमाचा विचार करण्यात येतो. क्रमिक सहजननाचा अभ्यास हा लहान आकारमानाच्या म्हणजे खडकाच्या हात नमुन्यातील खनिजांचा अगदी मर्यादित, तर मोठ्या प्रादेशिक अशा संपूर्ण धातुक निक्षेपाचा अगदी व्यापक असा असू शकतो. व्यापक अभ्यासासाठी निक्षेपाच्या संपूर्ण क्षेत्रातील अनेक ठिकाणचे प्रातिनिधिक नमुने काळजीपूर्वक गोळा करावे लागतात. या पाहणीमध्ये निक्षेपात आणि त्याच्या सभोवार असणाऱ्या खडकांत असणाऱ्या स्तरण, घड्या, विभंग (भेगा) यांसारख्या संरचनांचे विश्लेषणही करण्यात येते.
शिलारसाचे स्फटिकीभवन होऊन तयार होणाऱ्या निरनिराळ्या खनिज जातींच्या स्फटिकीभवनाचा क्रम, खनिज व धातुक शिरेमध्ये असलेल्या खनिजांच्या निर्मितीचा क्रम क्रमिक सहजननात ठरविण्यात येतो. सर्वांत अगोदर तयार झालेले खनिज प्रथम व क्रमाक्रमाने नंतर तयार झालेली खनिजे त्या अनुक्रमाने पुढेपुढे मांडीत जाऊन सर्वांत शेवटी तयार झालेले खनिज शेवटी लिहून यादी तयार करतात. मात्र अशा प्रकारची यादी करताना अगदी अचूक क्रम ठरविणे हे नेहमीच सोपे नसते. प्रथम तयार झालेल्या काही खनिजांचे विघटन, पुनर्स्फटिकीभवन, प्रतिष्ठापन वगैरे होऊन नंतर काही नवीन खनिजांच्या जाती तयार होतात. यामुळे क्रम ठरविण्यात चूक होण्याची शक्यता असते. हल्ली प्रयोगशाळेत निरनिराळ्या रासायनिक संघटनांच्या शिलारसांपासून कृत्रिम रीतीने खनिजे संश्लेषित करुन क्रमिक सहजननाचा अभ्यास करतात.
खनिजांच्या वयनाची (घटकांचे आकारमान, निक्षेपण व मांडणी यांची, पोताची) पाहणी क्रमिक सहजननाची माहिती मिळविण्यासाठी उपयोगी पडते. मात्र कधीकधी वयनाच्या चुकीच्या विश्लेषणामुळे चुकीचे क्रम ठरण्याची शक्यता असते. उदा., एकमेकांच्या सान्निध्यात दोन भिन्न आकारमानांची खनिजे असल्यास त्यांतील मोठे खनिज सामान्यत: अगोदर तयार झालेले असते, पण असे असेलच असे नाही. कित्येकदा एकाच वेळेस स्फटिकीभूत होणाऱ्या दोन संयुगांच्या वाढीचा वेग भिन्न असल्यामुळे एक मोठे व दुसरे लहान असणे शक्य असते. मात्र एखादे पूर्णाकृती खनिज दुसऱ्या एखाद्या अंशाकृती किंवा अनाकृती खनिजात समाविष्ट असेल, तर पूर्णाकृती खनिज लहान असले तरी अगोदर तयार झालेले असते.
खनिजांच्या क्रमिक सहजननाचा विचार हा सामान्यत: काळाचा सापेक्ष विचार करुन करण्यात येतो. दोन खनिजे तयार होण्यामधील निरपेक्ष काळ सामान्यत: माहीत नसतो. सर्वांत प्रथम व सर्वांत शेवटी तयार होणाऱ्या खनिजांत प्रत्यक्ष किती वेळ गेला हे माहीत नसते. अगदी आवश्यक असल्यास कधीकधी निरपेक्ष काळही किरणोत्सर्गी (कण वा किरण बाहेर टाकणाऱ्या पदार्थाच्या गुणधर्माचा उपयोग करणाऱ्या) पद्धतींनी काढता येतो. परंतु निरपेक्ष काळ माहीत नसूनही फक्त सापेक्ष काळाचा विचार करुन केलेला क्रमिक सहजननाचा अभ्यास, निरनिराळ्या दाब व तापमानाच्या परिस्थितींत निरनिराळे ॠणायन व धनायन कसे वागतात हे खनिजाचे भूरसायन समजून घेण्यास उपयोगी पडतो. बऱ्याच वेळा ज्या द्रवातून खनिजे तयार होतात त्याबद्दल इतकी सविस्तर माहिती मिळते की, ही खनिजे प्रयोगशाळेत योग्य अशा रासायनिक संघटनाच्या रसापासून नैसर्गिक स्फटिकीभवनाची पुनरावृत्ती करुन स्फटिकीभवनाच्या त्याच नैसर्गिक क्रमाने तयार करता येतात. क्रमिक सहजनन खनिजविज्ञान व खनिज रसायनशास्त्र यांच्यात अगदी घनिष्ट संबंध आहेत.
प्रायोगिक खनिजविज्ञान : खनिजे कशी तयार होतात हे समजून घेण्यासाठी पूर्वी केवळ नैसर्गिक खडकांची उघड्या क्षेत्रात जागच्या जागी किंवा प्रयोगशाळेत पाहणी करीत असत. पण हल्ली खनिजे ज्या जटिल प्रक्रियांनी तयार होतात, त्या समजावून घेण्यासाठी प्रायोगिक पद्धतींचा उपयोग करतात. खनिजांचे संश्लेषण, प्रावस्था संतुलनाचे (विशिष्ट दाब व तापमानाच्या परिस्थितींत एकत्र स्थिर राहू शकणारे द्रव, घन व वायुरुप घटक यांचे) अध्ययन, भूवैज्ञानिक प्रक्रिया आणि परिस्थिती कृत्रिम रीतीने प्रयोगशाळांत निर्माण करणे दाब, तापमान इत्यादींच्या निरनिराळ्या परिस्थितींत खनिजांचे गुणधर्म कसे असतात किंवा बदलतात ते पाहणे, यांसारख्या गोष्टींचा समावेश प्रायोगिक खनिजविज्ञानात होतो.
बहुतेक सर्वसामान्य खनिजे व पुष्कळशी दुर्मिळ खनिजे कुठल्या ना कुठल्या कृत्रिम पद्धतीने बनविण्यात आली आहेत. केवळ एकेकटी खनिजे स्वतंत्रपणे संश्लेषित केल्यास खडकांतील खनिजे कशी तयार होतात, हे समजण्यास त्याचा अगदी थोडाच उपयोग होतो. मात्र तांत्रिक व औद्योगिक दृष्ट्या उपयोगी पदार्थ बनविण्यासाठी त्यांचा फार उपयोग होतो. निसर्गात आढळणारे खडक तयार करणाऱ्या भूरासायनिक समुहाची साधी प्रतिकृती तयार करुन तिच्यामधील प्रावस्था संतुलनाचे अध्ययन प्रयोगशाळांत करुन खनिजे कशी तयार होतात, याबद्दल बरीच मूलभूत माहिती मिळते. शिलारसासारख्या रसातून तयार होणाऱ्या पदार्थांचे स्थैर्य हे त्या रसात असणाऱ्या घटकांवर अवलंबून असल्यामुळे पुष्कळ घटक असणाऱ्या रासायनिक समुहांनी युक्त अशा रसांचे अन्वेषण (संशोधन) करणे फार उपयोगी असते.
या प्रकारचे अगदी सुरुवातीचे अन्वेषण इ. स. १८९६ मध्ये जे. एच्. व्हांट हॉफ यांनी साध्या मिठाच्या विद्रावावर सामान्य दाबतापमानास केले व त्याचा उपयोग त्यांनी श्टासफुर्ट येथील जिप्समादी लवणांचे निक्षेप कसे तयार झाले असावेत, हे ठरविण्यासाठी केला. प्रायोगिक खनिजविज्ञानाचे पद्धतशीर अन्वेषण कार्य अमेरिकेतील वॉशिंग्टन येथील भूभौतिक प्रयोगशाळा करीत आहे. १९१३ साली बोएन यांनी प्लॅजिओक्लेज फेल्स्पारांच्या दोन घटकांच्या समुहांचे आणि त्यांच्या घन विद्रावणाच्या प्रक्रियेचे अन्वेषण केल्यानंतर पुढे अनेक घटक असणाऱ्या समुहातील निरनिराळ्या प्रावस्थांच्या संतुलनाचे संबंध उच्च दाब आणि तापमानास कसे असतात, त्याचे अन्वेषण होऊ लागले. यावरुन बोएन यांनी विक्रियेचे मूलतत्व प्रसिद्ध केले. १९३१ साली आर्. डब्ल्यू. गोरानसन यांनी सजल सिलिकेटी समुहाचे उच्च दाब आणि तापमानास अन्वेषण केले. त्यावरुन या परिस्थितीमध्ये (१) तप्त अशा रस-समुहामध्ये कित्येक टक्के पाणी मिसळू शकते व (२) या परिस्थितीतील खनिजांचे वितळबिंदू या समुहाइतकेच परंतु निर्जल असणाऱ्या समुहातील खनिजांच्या वितळबिंदूंपेक्षा बरेच कमी असतात, हे दिसून आले. १९४९ साली बोएन व टटल यांनी अगोदरच्या निर्जल रासायनिक समुहांच्या अन्वेषणाच्या धर्तीवर जलतापीय पद्धतींचे अन्वेषण सुरु केले. अलीकडेच डी. टी. ग्रिग्झ व सी. जी. केनेडी यांनी पन्नास हजार वातावरणीय दाब सु. १,०००° से. तापमान या परिस्थितीत वापरता येणारी यंत्रणा प्रयोगशाळेत वापरुन तिच्यामध्ये निरनिराळ्या खनिजांचे स्थैर्य कसे असते, त्याची पाहणी सुरु केली आहे. या पाहणीवरुन ज्या तापमानास पुष्कळसे निर्जल रासायनिक समूह कित्येक महिने ठेवले असताना त्यांच्यात थोडीसुद्धा विक्रिया घडून येत नाही, अशा काही अल्प शतकांच्या तापमानास पाणी किंवा बाष्पनशील (सहज उडून जाणाऱ्या) द्रव्याच्या सान्निध्यात व उच्च दाबास खनिजातील रासायनिक विक्रिया अगदी झपाट्याने घडून येतात, असे दिसून आले आहे. या माहितीमुळे या काळापर्यंत शक्य नसलेल्या अनेक घन विद्रावांचे अन्वेषण करणे शक्य झाले आहे. सिलिकेटांच्या अध्ययनाबरोबर कार्बोनेटे आणि सल्फाइडे यांचेही सविस्तर अध्ययन सुरु झाले आहे. तसेच प्रावस्था संतुलनाच्या पाहणी व्यतिरिक्त इतर प्रकारांनी भूवैज्ञानिक तापमानाचे अन्वेषण प्रायोगिक पद्धतींनी सुरु झाले आहे. तापमान, दाब, रासायनिक संघटन इत्यादींच्या निरनिराळ्या परिस्थितींतील खनिजे, त्यांची मिश्रणे यांच्या गुणधर्माचे अध्ययन तांत्रिकी तसेच भूवैज्ञानिक दृष्टीने महत्त्वपूर्ण असे आहे.
पहा : खाणकाम धातुक रत्ने रुपांतरित खडक स्फटिकविज्ञान.
संदर्भ : 1. Dana, E. S. Ford, W. E., Ed., Textbook of Mineralogy Bombay, 1962.
2. Deer. W. A. Howie, R. A. Zussman, J. Introduction to the Rock Forming Minerals, London, 1967.
3. Hurlbut, C. S., Ed., Dana’s Manual of Mineralogy, New York, 1959.
4. Kerr, P. F. Optical Mineralogy, New York, 1959.
5. Kraus, E. H. Hunt, W. F., Mineralogy, New York, 1959.
6. Mason, B. Berry, L. G. Elements of Mineralogy, San Francisco, 1968.
7. Nininger, R. D. Minerals of Atomic Energy, New York, 1956.
8. Read, H. H. Rutley’s Elementery Mineralogy, London, 1956.
9. Sinha, R. K. A Treatise on Industrial Minerals of India, Bombay, 1967.
10. Wahlstrom, E. E. Optical Crystallography, New York, 1966.
11. Webster, R. Gems-Their Sources, Description and Identification, London, 1970.
12. Winchell, A. N. Winchell, H. Elements of Optical Mineralogy, New Delhi, 1968.
केळकर, क. वा. आगस्ते, र. पां. सोवनी, प्र. वि.
“