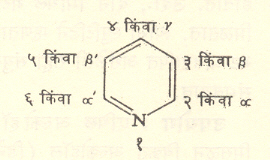
पिरिडीन : एक क्षारकधर्मी (अम्लाशी विक्रिया करून लवण बनविण्याचा गुण असलेले) कार्बनी संयुग. रेणुसूत्र (रेणुमध्ये असलेल्या अणूचे प्रकार व संख्या व्यक्त करणारे सूत्र) C5H¬5N. याच्या संरचनेत (रेणूतील अणू एकमेकांस जोडले जाण्याच्या पध्दतीत) पाच कार्बन अणू व एक नायट्रोजन अणू यांचे बनलेले एकंदर सहाअणूंचे असंतृप्त (व्दिबंध अथवा त्रिबंध असलेले) वलय असते.
पिरिडीन आणि त्याच्या वर्गाची इतर संयुगे या सर्वांना मिळून पिरिडीन क्षारके म्हणतात.
उपस्थिती : दगडी कोळशाच्या डांबरात [→ डांबर] व हाडांच्या भंजक ऊर्ध्वपातनाने (बंद भांड्यात घेऊन उच्च तापमानाने मूळ रेणूचे तुकडे करून, मिळणारे पदार्थ जमविण्याच्या क्रियेने) मिळणाऱ्या तेलात पिरिडीन व त्याची समजातीय (याच वर्गाची) संयुगे असतात.
ब६ जीवनसत्त्व व निकोटिनामाइड या नैसर्गिक पदार्थांत तसेच डाळिंब, हेमलॉक, पोफळ, तंबाखू इत्यादींमधील अल्कलॉइडांमध्ये [→ अल्कलॉइडे] पिरिडीन संरचनेचा गाभा आहे.
इतिहास : टी. अँडरसन यांनी १८४६–५७ या काळात हाडांच्या ऊर्ध्वपातनाने मिळणाऱ्या तेलापासून व डांबरापासून प्रथम २–मिथिल पिरिडीन (α –पिकोलीन) आणि नंतर पिरिडीन व इतर क्षारके लवकरच वेगळी केली. या क्षारकांचे अस्तित्व ⇨ शेल तेल, अशुध्द ॲमिल अल्कोहॉल, खनिज तेल इत्यादींमध्येही असते हे नंतर कळून आले. संश्लेषणाने (कृत्रिम रीतीने) पिरिडीन व इतर क्षारके बनविण्याचे मार्ग आज उपलब्ध आहेत.
निर्मिती : दगडी कोळशाच्या कार्बनीकरणाने मिळणाऱ्या डांबराचे [→ डांबर] ऊर्ध्वपातन केले म्हणजे सु. २१०० से. पर्यंत ऊर्ध्वपातन होणाऱ्या अंशाचे (हलके तेल) व सु. २७०० से. पर्यंतच्या अंशाचे (मध्यम तेल) प्रथम दाहक (कॉस्टिक) सोड्याने निष्कर्षण (वेगळी) करून त्यातील अम्ले व फिनॉले काढून टाकतात. नंतर राहिलेल्या तेलात सल्फ्यूरिक अम्लाचा जलीय विद्राव मिसळतात. त्यामुळे पिरिडीन व त्याच्या क्षारकांची सल्फेटे बनून ती पाण्यात विरघळतात. जलीय थर वेगळा करुन दाहक सोडा किंवा अमोनिया यांची विक्रिया केली म्हणजे पिरिडीन व क्षारके मुक्त होतात. मिळणाऱ्या मिश्रणात सु. ३५–४० % पिरिडीन, १०% २–मिथिल पिरिडीन व उरलेला भाग इतर पिरिडीन क्षारके यांचा असतो. यामधून खंडश: ऊर्ध्वपातन करून (ऊर्ध्वपातन होताना वेगवेगळ्या तापमानांस मिळणारे अंश वेगवेगळे जमवून) पिरिडीन, २–मिथिल पिरिडीन (२–पिकोलीन), ३–मिथिल पिरिडीन (३–पिकोलीन), ४–मिथिल पिरिडीन (४–पिकोलीन) व २, ६–डायमिथिल पिरिडीन (२, ६–ल्युटिडीन) ही क्षारके वेगळी करतात.
काही महत्वा्वच्या संश्लेषण विक्रिया : मिथिल अल्कोहॉल, फॉर्माल्डिहाइड व अँसिटाल्डिहाइड ही बाष्परुपात घेऊन त्यात अमोनिया मिसळतात व मिश्रण सिलिका-अँल्युमिना उत्प्रेरकाच्या (विक्रिया जलद अथवा कमी तापमानास घडावी म्हणून वापरलेल्या व विक्रियेनंतर रासायनिक दृष्यात् मूळ स्वरुपात कायम राहणाऱ्या पदार्थांच्या) उपस्थितीत, ५००० से. तापमानास तापवितात. त्यामुळे जे विक्रिया मिश्रण मिळते त्याचे खंडश: ऊर्ध्वपातन केले म्हणजे पिरिडीन (३५ %) व ३-मिथिल पिरिडीन (३-पिकोलीन, २७%) ही संयुगे मिळतात. सिलिका-अँल्युमिना व थोरिया हा उत्प्रेरक वापरला आणि अँसिटाल्डिहाइड व अमोनिया यांचे मिश्रण ४५०० से. तापमानास त्य़ावरुन प्रवाहित केले, तर २-पिकोलीन व ४-पिकोलीन ही संयुगे मिळतात.
पॅराल्डिहाइड व जलीय अमोनिया यांच्यापासून २००० – २५०० से. तापमानास विक्रिया घडवून २-मिथिल ५-एथिल पिरिडीन हे एक महत्वागकचे संयुग बनविता येते.
ए. हांटश यांनी सिध्द केलेल्या एका संश्लेषण पध्दतीने, विक्रिया मिश्रणात फेरफार केला म्हणजे पिरिडीनाची अनेक समजातीय संयुगे बनविता येतात. उदा., एथिल अँसिटोअँसिटेटाचे २ रेणू व अँसिटाल्डिहाइड १ रेणू या प्रमाणात घेऊन अमोनियाच्या उपस्थितीत विक्रिया घडविली, तर तीन टप्प्यांत ती पूर्ण होते आणि सूत्र २ मध्ये दाखविलेले संयुग बनते. नायट्रीक अम्लाने याचे ऑक्सिडीकरण [→ ऑक्सिडीभवन] केले म्हणजे सूत्र ३ मध्ये दाखविलेले संयुग मिळते व त्यापासून २, ४, ६-ट्रायमिथिल पिरिडीन (२, ४, ६ – कॉलिडीन) हे महत्वायाचे संयुग बनविता येते.
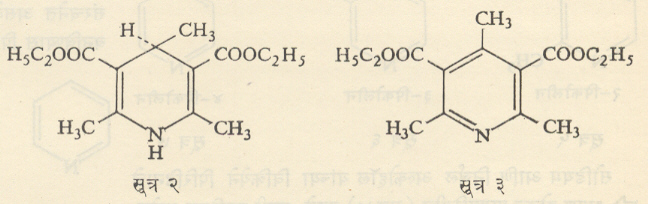
अँसिटाल्डिहाइडाऐवजी दुसरी आल्डिहाइडे वापरली, तर पिरिडीन वलयातील ४ या स्थानी गट बसविता येतात.
याचप्रमाणे बीटा डायकीटो एस्टराच्या जागी बीटा डायकीटोने वापरता येतात. तसेच बीटा डायकीटो एस्टराचे २ रेणू वापरण्याऐवजी आल्डिहाइडाचे २ रेणू आणि डायकीटोनाचा एक रेणू, असा फरक करुनही विक्रिया घडवून आणता येते आणि वेगवेगळी पिरिडीन क्षारक वर्गाची संयुगे बनविता येतात.
पिरिडिनामध्ये विषमवलयी (वलयात कार्बन अणूबरोबर इतर अणूंचा समावेश असलेली) संरचना आहे हे सुचित करण्याच्या दृष्टीने पुढील संश्लेषण पध्दतीला (सूत्र ४) महत्त्व आहे. या पध्दतीने प्रथम पायरिडीन हे संयुग बनते व त्यापासून पिरिडीन मिळते.
गुणधर्म : वर्णहीन, दुर्गंधी, तिखट रुचीचा द्रव. वितळबिंदू – ४१.५० से., उकळबिंदू ११५.५० से., आर्द्रताशोषक (पाणी शोषण करणारे). पाण्यात व कार्बनी विद्रावकांत विरघळते. हायड्रोक्लोरीक अम्लाच्या विक्रियेने C5H5N.HCl व सल्यूकळरिक अम्लाच्या विक्रियेने (C5H5N)2H2SO4 ही स्फटिकी लवणे मिळतात.
|
Br·CH2·CH2·CH2·Br + |
2KCN |
→NC·CH2·CH2·CH2·CN + |
2KBr |
|
ट्रायमिथिलीन डायब्रोमाइड |
पोटॅशियम सायनाइड |
ट्रायमिथिलीन डायसायनाइड |
पोटॅशियम ब्रोमाइड |
|
NC·CH2·CH2·CH2·CN + |
8H |
→H2N·CH2·CH2·CH2·CH2·CH 2·NH2 |
|
ट्रायमिथिलीन डायसायनाइड |
हायड्रोजन |
पेंटामिथिलीनडायअमाइन |

मिथिल आयोडाइडाबरोबर (CH3I) समावेशक (अणू वा अणुगट रेणूमध्ये सामावले जाऊन होणारी) विक्रिया होऊन C5H5N.CH3 I पिरिडीन मिथआयोडाइड किंवा मिथिल पिरिडीनियम आयोडाइड हे संयुग बनते. ते ३००० से. पर्यंत तापविले, तर २–पिकोलीन आणि ४–पिकोलीन ही संयुगे बनतात (सूत्रे ५ व ७).

सोडीयम आणि निर्जल अल्कोहॉल यांच्या विक्रियेने पिरिडिनाचे ⇨ क्षपण होऊन पायपरिडीन (सूत्र ४) बनते. पाणी उपस्थित असेल, तर मात्र नायट्रोजन अणू अमोनियाच्या रूपाने निघून जातो व ग्लटार डाय आल्डिहाइड (OHC–CH2–CH2–CH2–CHO) बनते. हॅलोजनांच्या विक्रिया कष्टसाध्य आहेत. उदा., ३००० से. तापमानास विक्रिया केली म्हणजे ३ – ब्रोमोपिरिडीन (बीटा ब्रोमोपिरिडीन) मिळते.
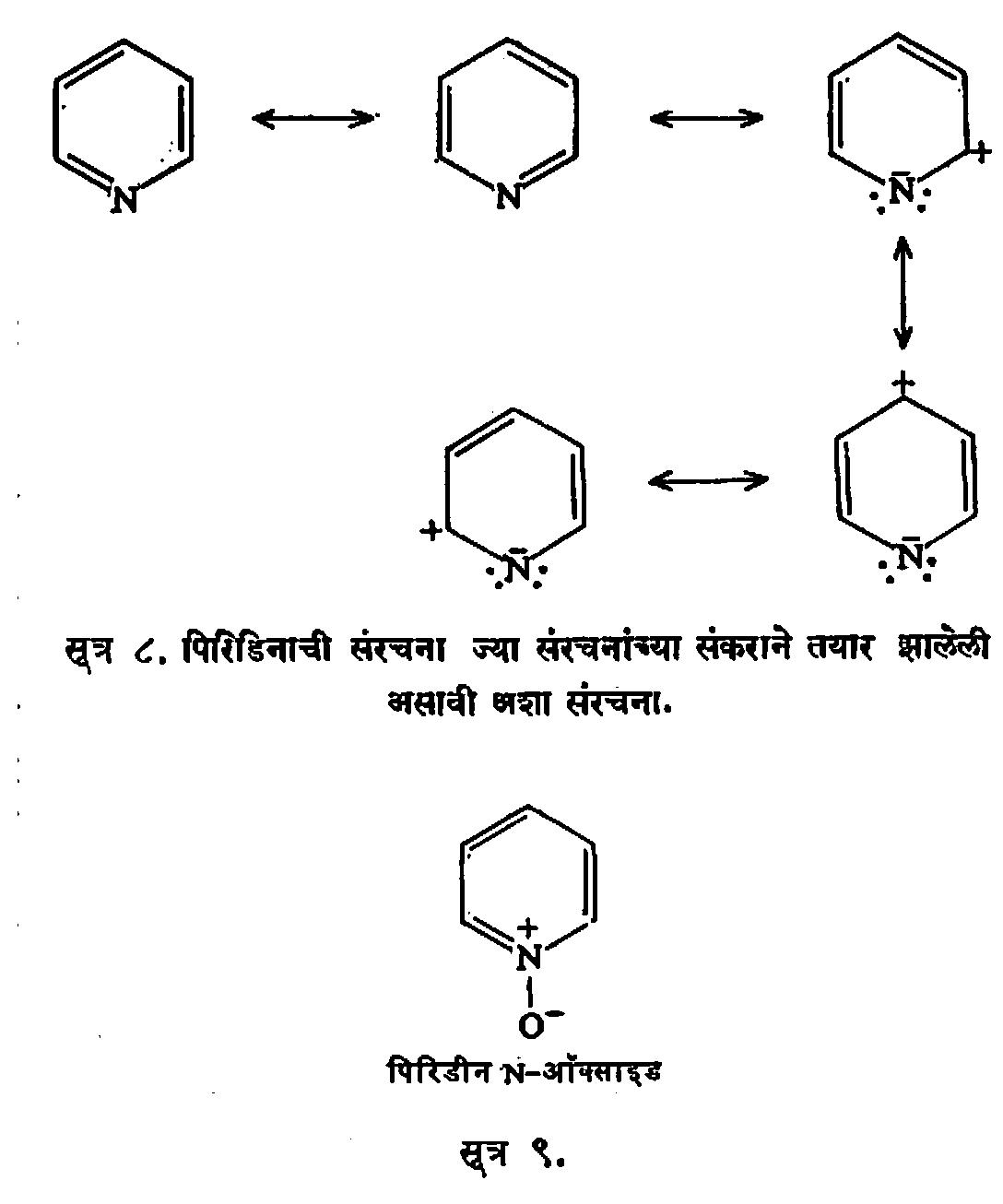
बेंझिनावर सल्फ्यूरिक अम्लाची विक्रिया जशी सुलभतेने होते तशी पिरिडिनावर होत नाही. संहत (विद्रावात जास्त प्रमाण असलेल्या) सल्फ्यूरिक अम्लाबरोबर ३५०० से. तापमानास पिरिडीन तापविले, तरच पिरिडीन–३–सल्फॉनिक अम्ल बनते. पिरिडीन बेंझिनापेक्षा जास्त स्थिर आहे. पिरिडीनाची संरचना सूत्र ८ मध्ये दर्शविलेल्या संरचनांच्या संकराने झाली असली पाहिजे, असा यावरून निष्कर्ष निघतो.
परबेंझॉइक अम्लाबरोबर विक्रिया होऊन पिरिडिनाचे N–ऑक्साइड बनते. यावर विक्रिया करून अनेक पिरिडीन अनुजात (पिरिडिनापासून तयार होणारी इतर संयुगे) मिळविता येतात. उदा., फॉस्फरस पेंटाक्लोराइडाच्या विक्रियेने २–क्लोरोपिरिडीन बनते. नायट्रीकरण केल्याने प्रथम २–व ४–नायट्रोपिरिडीन ऑक्साइडे बनतात. त्यांवर फॉस्फर ट्राय क्लोराइडाची विक्रिया केली म्हणजे २ – व ४ – नायट्रोपिरिडिने मिळतात.
पिरिडिनाची संयुगे : (एकाच वर्गातील संयुगांच्या श्रेणीतील संयुगे, अशा दोन संयुगांच्या रेणुसूत्रांत CH2 चा फरक असतो). पिरिडीन वलयात एक अणू अथवा गट प्रतिष्ठापित केल्यास (रेणूतील मूळचा अणू अथवा गट काढून त्या जागी दुसरा अणू अथवा गट बसविल्यास) तीन निरनिराळ्या संरचना होतात. उदा., मिथिल गटामुळे २ – मिथिल पिरिडीन किंवा आल्फा पिकोलीन, ३ – मिथिल पिरिडीन किंवा बीटा पिकोलीन व ४ – मिथिल पिरिडीन किंवा गॅमा पिकोलीन. दोन समान गट प्रतिष्ठापित केल्यास सहा भिन्न संरचना होतात. उदा., दोन मिथिल गटांमुळे ६ संयुगे मिळतात. त्यांना ल्युटिडिने म्हणतात. तीन मिथिल गट प्रतिष्ठापित असलेली सहा संयुगे–कॉलिडिने–संभवतात.
उपयोग : एथिल अल्को हॉलात पिरिडीन मिसळून विकृत अल्कोहॉल (डिनेचर्ड स्पिरिट) बनवितात. त्यामुळे ते विद्रावक म्हणून (पदार्थ विरघळविण्यासाठी) वापरता येते, पण मादक पेय (दारू) म्हणून पिता येत नाही. रासायनिक विक्रिया घडविण्यासाठी एक माध्यम म्हणून पिरिडीन उपयोगी पडते. आर्द्रतामापनासाठी वापरतात त्या प्रसिध्द कार्ल-फिशर विक्रियाकारकात पिरिडिनाचा अंतर्भाव असतो.
अनेक स्टरॉइडे व सल्फा औषधे, तसेच २ – ॲमिनोपिरिडीन हे औषधी संयुग बनविण्यासाठी पिरिडीन उपयोगी पडते. स्टिअरिल मिथिल एथिल पिरिडीनियम क्लोराइड व कार्बनाची लांब साखळी संरचनेत असलेली यासारखी वस्त्रोद्योगात उपयोगी पडणारी संयुगे बनविण्यास पिरिडीन लागते.
२–पिकोलीन हे विद्रावक म्हणून आणि रंजकद्रव्ये, कीटकनाशके, औषधी व वस्त्रोद्योगात उपयोगी पडणारी संयुगे बनविण्यासाठी माध्यमिक द्रव्य म्हणून उपयोगी पडते. ३–पिकोलिनापासून निकोटिनिक अम्ल हे महत्वाचे संयुग बनवितात. ४–पिकोलिनाचा उपयोग आयसोनियाझीड हे क्षयरोग प्रतिकारी औषधी संयुग बनविण्यासाठी करतात. पायपरिडिनापासून पीपीडी म्हणजेच पायपरिडीनियम पेंटामिथिलीन डायथायोकार्बामेट हे रबर उद्योगात उपयुक्त असलेले प्रभावी प्रवेशक [व्हल्कनीकरण त्वरेने घडविणारे → रबर] बनविले जाते. कॉलिडिने ॲथ्रक्किनोनाच्या उत्पादनात विद्रावके म्हणून उपयोगी पडतात.
संदर्भ : 1. Faith, W. L. Keyes, D. B. Clark, R. L. Industrial Chemistry, London, 1957.
2. Fieser, L. F. Fieser, M. Organic Chemistry, Bombay, 1962.
3. Kilner, E. Samuel, D. M. Applied Organic Chemistry, London, 1960.
केळकर, गो. रा. सुर्यवंशी, वि. ल.
“