दर्शके : ज्या द्रव्याचा विद्राव क्षारकीय (अम्लाशी विक्रिया झाल्यास लवणे देणाऱ्या पदार्थांच्या बेसिक) माध्यमातून अम्लीय माध्यमात जाताना तसेच अम्लीय माध्यामातून क्षारकीय माध्यमात जाताना रंग बदलतो, त्याला दर्शक असे म्हणतात. दर्शकाच्या रंगात होणाऱ्या रंगबदलामुळे विद्रावाची अम्लीय अथवा क्षारीय स्थिती समजू शकते. दर्शकांचा हा रंगबदल विद्रावातील हायड्रोजन आयनांच्या संहतीशी (हायड्रोजनाच्या विद्युत् भारित अणूंच्या म्हणजे आयनांच्या प्रमाणाशी) म्हणजेच विद्रावाच्या pH मूल्याशी [⟶ पीएच मूल्य]संबधित असतो. हायड्रोजन आयन संहतीच्या ठराविक कक्षेसाठी ठराविक दर्शकाचा उपयोग होतो. या कक्षेमध्ये हायड्रोनियम आणि हायड्रॉक्साइड आयनांच्या संहतीप्रमाणे दर्शके रंग बदलतात. ⇨ अनुमापनासाठी किंवा pH मूल्य ठरविण्यासाठी दर्शकांचा उपयोग केला जातो. दर्शकामुळे होणारा रंगबदल गडद असावा यासाठी त्याचे काही थेंब पुरेसे होतात. मापी विश्लेषण करताना चंबूमधील विद्रावात दर्शकाचे २—३ थेंब टाकतात. उदासिनीकरण (अम्लीय वा क्षारकीय गुणधर्म नाहीसा होण्याची क्रिया) पूर्ण होण्याच्या वेळी मोजनळीमधून पडणाऱ्या विद्रावाच्या अर्ध्या थेंबामुळेही दर्शक आपला रंग बदलतो. या रंग बदलण्याच्या अवस्थेला अंतिम बिंदू म्हणतात म्हणून कोणत्याही अनुमापनात अंतिम बिंदू ठरविण्यासाठी दर्शके वापरतात. सर्वसाधारणपणे वापरण्यात येणारी दर्शके दुर्बल कार्बनी अम्ले अथवा दुर्बल कार्बनी क्षारक असतात. (ज्या अम्लांचे वा क्षारकांचे जलीय विद्रावात पूर्णपणे आयनीभवन होते ते प्रबल आणि ज्यांचे आयनीभवन अल्प प्रमाणात होते ते दुर्बल होत आयनीभवन म्हणजे आयनांत—विद्युत् भारित अणू, रेणू वा अणुगटांत—रुपांतर होणे).
निवड : जेव्हा अनुमापन करताना क्षारकामध्ये सममूल्य अम्ल घातले जाते त्या वेळी दर्शकात सहज रीतीने दिसण्याजोगा रंगबदल झाला पाहिजे. या ठिकाणी सममूल्य याचा अर्थ क्षारक विद्रावात जितका क्षारक असेल तितका संपूर्णपणे उदासीन करण्यास लागणारे अम्लाचे वजन असा आहे, म्हणजेच अंतिम बिंदूच्या वेळी विद्रावाचे जे pH मूल्य असते त्या वेळी रंगबदल होते. यासाठी योग्य दर्शकाची निवड करण्याकरिता या विद्रावाचे आधी pH मूल्य मोजतात आणि जे दर्शक या सीमारेषेशी pH मूल्य बदलतात त्या दर्शकांची निवड करतात. या कामासाठी pH तक्त्यांचा चांगला उपयोग होतो.
उपपत्ती : एफ्. डब्ल्यू. ओस्टव्हाल्ट यांनी दर्शकासंबंधी मांडलेली उपपत्ती पुढीलप्रमाणे आहे. विद्रावाचे pH बदलल्यानंतर दर्शकाच्या रंगात का बदल होतो याचे स्पष्टीकरण या उपपत्तीमुळे होते. या उपपत्तीप्रमाणे दर्शके ही दुर्बल अम्ले अथवा दुर्बल क्षारक असतात आणि दर्शकांचे रंग आयन स्वरूपात व रेणूच्या स्वरूपात निरनिराळे असतात. म्हणून या उपपत्तीनुसार फिनॉलप्थॅलिनासारख्या दुर्बल अम्लाचे वर्तन पुढीलप्रमाणे सांगता येईल.
HPh ⇌ H+ + Ph−
रंगविरहित नीलातिरक्त (मॅजेंटा)
विद्रावात अम्ल विद्राव घातल्यामुळे हायड्रोजन आयनांची संहती वाढते. त्यामुळे दर्शकाचे विगमन (रेणूतील आयन सुटे होणे) कमी होते आणि त्यामुळे दर्शक रंगहीन होते. याउलट क्षारक घातल्यामुळे हायड्रोजन आयन हायड्रॉक्साइडामुळे बाजूला काढले जातात आणि दर्शकाचे विगमन जास्त होऊन गुलाबी रंग येतो.
याचप्रमाणे मिथिल ऑरेंजसारख्या दुर्बल क्षारक असलेल्या दर्शकाची वर्तणूकही स्पष्ट करता येईल.
MeOH ⇌ Me+ + OH−
पिवळा नारिंगी
क्षारक घातल्यामुळे हायड्रॉक्साइड आयनांची संहती वाढते आणि त्यामुळे दर्शकाचे विगमन कमी होऊन पिवळा रंग येतो. अम्ल घातल्यामुळे हायड्रॉक्साइड आयन बाजूला काढले जातात व त्यामुळे दर्शकाचे विगमन जास्त होऊन नारिंगी रंग येतो परंतु हे स्पष्टीकरणही अपूर्ण आहे कारण कार्बनी रसायनाच्या रंगात जेव्हा बदल होतो तेव्हा तो त्याच्या रेणूतील अणूंच्या रचनेतही बदल झाल्याचे सुचवितो. आता असेही सिद्ध झाले आहे की, प्रथम दर्शकांचा व्युत्क्रमी (उलटसुलट अशा दोन्ही दिशांनी होणारा) चलसमघटक (ज्या रेणूतील अणुरचना बदलू शकते अशा) रूपांत बदल होतो व त्याचा रंग मूळ दर्शकाहून वेगळा असतो. या दुसऱ्या रूपाचे आयनीभवन होते व त्यापासून वेगळ्या रंगाचे आयन तयार होतात. उदा., फिनॉलप्थॅलीन :
HPh ⇌ HPh* ⇌ H+ + Ph−
रंगविरहित रंगीत चलसमघटक रूप नीलातिरक्त
कक्षा : दर्शकाची उपयुक्त कक्षा pH च्या दोन परिमाणांपुरती मर्यादित असते, परंतु विद्रावाचे pH १ ते १४ पर्यंत असू शकते. म्हणून निरनिराळ्या pH कक्षांमध्ये रंगबदल दर्शविणारी निरनिराळी दर्शके आवश्यक असतात. काही दर्शके, त्यांच्या उपयुक्त pH कक्षा व रंगांत होणारे बदल पुढे दिलेल्या तक्त्यावरून लक्षात येतील.
प्रकार: विवर्ण दर्शक : ही दोन दर्शके किंवा दर्शक आणि रंजक यांचे रंगहीन मिश्रण असते. अंतिम बिंदूला हे मिश्रण असते. अंतिम बिंदूला हे मिश्रण स्वतःच्या रंगाचा पूरक रंग दर्शविते. उदा.,
मिथिल रेड ०·१२५ + मिथिलीन ब्ल्यू ०·०८२५
पृष्ठशोषण दर्शक : (पृष्ठभागी ज्यांचे शोषण होते असे). काही कार्बनी संयुगांच्या अवक्षेपावर (न विरघळणाऱ्या साक्यावर) पृष्ठशोषण होते. त्यामुळे अवक्षेपाच्या पृष्ठभागावर रंगबदल होतो. उदा., क्लोराइडाच्या सिल्व्हर नायट्रेटाबरोबरच्या अनुमापनात फ्ल्युओरेसीन पृष्ठशोषण दर्शक म्हणून वापरतात. तसेच सिल्व्हर क्लोराइडाच्या साक्यावर ऱ्होडामाइन पृष्ठशोषित होते.
बाह्य दर्शक : ही दर्शके ज्याचे अनुमापन करावयाचे त्या विद्रावात घातली जात नाहीत. चिनी मातीच्या झिलई असलेल्या फरशीवर त्याचे थेंब ठेवले जातात व अनुमापन चालू असताना मधूनमधून अनुमापित विद्रावात एखाद्या काचदांडीचे टोक बुडवून त्याच टोकाने दर्शकाच्या थेंबाला स्पर्श केला जातो. या स्पर्शित थेंबातील रंगबदलावरून अंतिम बिंदू सूचित होते. या प्रकारच्या दर्शकास बाह्य दर्शक असे म्हणतात. उदा., पोटॅशियम डायक्रोमेटाच्या लोहाबरोबरच्या अनुमापनासाठी पोटॅशियम फेरिसायनाइडाचा उपयोग बाह्य दर्शक म्हणून केला जातो.
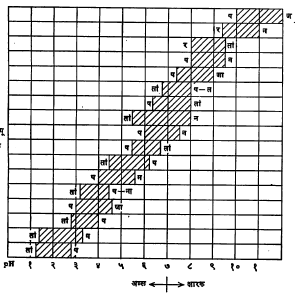
ॲलिझरीन यलो थायमॉलप्थॅलीन फिनॉलप्थॅलीन थायमॉल ब्ल्यू क्रेसॉल पर्पल न्यूट्रल रेड फिनॉल रेड लिटमस ब्रोमोथायमॉल ब्ल्यू क्लोरोफिनॉल रेड मिथिल रेड ब्रोमोक्रेसॉल ग्रीन मिथिल ऑरेंज ब्रोमोफिनॉल ब्ल्यू मिथिल यलो ट्रीपिओलीन ०० थायमॉल ब्ल्यू
आंतर्दर्शक : अनुमापन करावयाच्या विद्रावात जे दर्शक घातले जाते आणि अनुमापन केले जाते त्याला आंतर्दर्शक म्हणतात. उदा., फिनॉलप्थॅलीन अम्लात रंगहीन व क्षारकात नीलातिरक्त रंगावरून अंतिम बिंदू सूचित होतो.
उदासिनीकरण दर्शक : हा आंतर्दर्शकाचाच एक उपप्रकार आहे. हा सौम्य अम्लधर्मी अथवा सौम्य क्षारकधर्मी कार्बनी रंग असतो. अम्ल व क्षारक विद्रावांत त्याचे रंग वेगवेगळे असतात. उदा., मिथिल ऑरेंजला क्षारकात पिवळा व अम्लात नारिंगी रंग येतो.
अनुस्फुरक दर्शक: काही पदार्थ विशिष्ट तरंग लांबीच्या प्रकाशाचे शोषण करून निराळ्या, बहुशः अधिक, तरंगलांबीचे प्रकाशतरंग बाहेर टाकतात, याला अनुस्फुरण म्हणतात. ज्या पदार्थांच्या अनुस्फुरणात pH मूल्यातील बदलानुसार बदल होतात त्यांना अनुस्फुरक दर्शक म्हणतात व त्यांचा उपयोग pH मूल्य, तसेच अनुमापनातील अंतिम बिंदू ठरविण्यासाठी करता येतो. या प्रकारची दर्शके गडद रंगाच्या अथवा मलिन विद्रावांसाठीही वापरता येतात. या प्रकारची दर्शके सामान्यतः दुर्बल अम्ले किंवा क्षारके असून त्यांची अम्लीय वा क्षारीय रूपे तीव्र अनुस्फुरक असतात. आल्फानॅप्थिल अमाइन हे असे अनुस्फुरक दर्शक आहे.
मालिन्यदर्शक : काही निर्बल अम्ले आणि काही निर्बल क्षारक अविद्राव्य असतात परंतु त्यांची लवणे विद्राव्य असतात. अशी द्रव्ये दर्शक म्हणून वापरता येतात. जसजसा pH मध्ये बदल होतो तसतसा लवणाचा अवक्षेप दृश्य किंवा अदृश्य होतो. pH च्या मर्यादित कक्षेतही हा अवक्षेप दृश्य किंवा अदृश्य करता येतो. ठराविक pH मूल्य असताना विद्युत् उदासीनता किंवा शून्य विद्युत् वर्चस् (विद्युत् पातळी) निर्माण होऊन साका दिसू लागतो. यावरून अंतिम बिंदू किंवा pH मूल्य ठरविता येते.
ऑक्सिडीभवन–क्षपण दर्शक : अनुमापन चालू असताना अंतिम बिंदूजवळ विद्युत् वर्चसामध्ये बदल होत असताना ज्या पदार्थाचे ⇨ ऑक्सिडीभवन वा ⇨ क्षपण होताना जो रंगबदल दर्शवितो त्याला ऑक्सिडीभवन क्षपण दर्शक असे म्हणतात. ऑक्सिडीभवन अवस्थेमध्ये बदल होत असताना एका निश्चित अवस्थेत हा रंगबदल होतो. डायफिनिल बेंझिडीन हे अशा दर्शकाचे एक उदाहरण आहे.
सर्वकामी दर्शक : हे अनेक निवडक दर्शकांचे मिश्रण असते. त्यामुळे एकेका दर्शकापेक्षा हे दर्शक pH च्या व्यापक कक्षेसाठी उपयोगी पडते. कोणत्याही विद्रावासाठी कोणते दर्शक वापरावे लागेल हे ठरविण्यासाठी त्या विद्रावाचे pH मूल्य माहीत असावे लागते. यासाठी सर्वकामी दर्शक उपयोगी पडते. सर्वकामी दर्शकातील मिश्रणात २ ते १० पर्यंत प्रत्येक pH साठी ठराविक निराळा रंग दाखविणारी दर्शके निवडतात. विद्रावात सर्वकामी दर्शक घातल्यामुळे जो रंग येतो त्याची तुलना pH माहीत असलेल्या रंगाबरोबर केली जाते. हे दर्शक अनुमापनासाठी वापरीत नाहीत, तर pH ठरविण्यासाठी वापरतात. या दर्शकातील घटक (सर्व वजने ग्रॅममध्ये) : मिथिल ऑरेंज ०·१, मिथिल रेड ०·४, ब्रोमोथायमॉल ब्ल्यू ०·४, आल्फानॅप्थॉलप्थॅलीन ०·३२, फिनॉलप्थॅलीन ०·५ व क्रेसॉलप्थॅलीन १·६, १०० मिलि. ७०% अल्कोहॉलामध्ये विद्राव केल्यावर सर्वकामी दर्शक तयार होतो. याचा एक थेंब १० मिलि. विद्रावात घातल्यास निरनिराळ्या pH ला पुढीलप्रमाणे रंग येतात (पहिला आकडा pH मूल्य दर्शवितो) : ३·० लाल, ४·० नारिंगी लाल, ५·० पिवळट नारिंगी, ६·५ पिवळा, ८·० हिरवा, ८·५ निळसर हिरवा, ९·० हिरवट निळा, १०·० निळा, ११·० जांभळा, १२·० लालसर जांभळा. ते योग्य प्रमाणात मिथिल ऑरेंजमध्ये मिसळले, तर रंगबदल पिवळट हिरवा करडा नीलातिरक्त असा होतो. करड्या रंगामुळे (pH ३·८) अंतिम बिंदू आला असल्याचे समजते. कार्बोनेट बाय कार्बोनेट अनुमापनासाठी फिनॉलप्थॅलीन या दर्शकाऐवजी थायमॉल ब्ल्यू व क्रेसॉल रेड यांचे योग्य प्रमाणात केलेले मिश्रण वापरले, तर pH ८·३ असता पिवळ्यामधून जांभळ्यात रंगबदल होतो.
प्रच्छदित व मिश्र दर्शक : काही वेळा दर्शकाच्या रंगात होणारा बदल अधिक स्पष्ट आणि pH च्या छोट्याशा कक्षेत असणे आवश्यक असते. उदा., फॉस्फोरिक अम्लाचे द्विक्षारकीय अवस्थेपर्यंत (सममूल्य बिंदू pH ८·७) अनुमापन करावयाचे झाल्यास छोट्या pH कक्षेत रंगबदल होणारे दर्शक हवे असते. त्याचप्रमाणे कार्बोनेटाचे बायकार्बोनेट अवस्थेपर्यंत (सममूल्य बिंदू pH ८·३) अनुमापन करण्यासाठीही दर्शकाची अडचण भासते. अशा वेळी ‘प्रच्छादित’ वा ‘मिश्र’ प्रकारची दर्शके वापरणे इष्ट असते. याकरिता दर्शकामध्ये एखादा निष्क्रिय रंजक योग्य प्रमाणात मिसळून प्रच्छादित दर्शकाने वा दोन दर्शकांचे मिश्रण योग्य प्रमाणात मिसळून मिश्र दर्शकाने अनुमापन करावे लागते. दर्शकाचे हे दोन रंग एकमेकांस पूरक असल्याने अंतिम बिंदू अधिक अचूकपणे ठरविता येतो. अंतिम बिंदू हा मध्यम करड्या रंगामुळे ओळखता येतो. निष्क्रिय रंजकाच्या पार्श्वभूमीवर वा त्याच्यामधून दर्शकाच्या रंगात होणाऱ्या बदलाचे निरीक्षण करता येते. यामुळे एका रंगापासून त्याच्या पूरक रंगात होणारा बदल ओळखता येतो. उदा., निळा रंजक अंतिम बिंदूच्या वेळी तांबड्यापासून पिवळ्याकडे होणाऱ्या रंगबदलाचे प्रच्छादन करेल कारण तांबड्याबरोबर तो जांभळा रंग देईल, तर पिवळ्याबरोबर हिरवा देईल. अंतिम बिंदू मध्यम करड्या रंगाने दिसेल. मिथिल ऑरेंज हे दर्शक वापरताना क्षारक अवस्थेतून अम्ल अवस्थेत बदल होतो तेव्हा पिवळ्या रंगाचा तांबड्या रंगात बदल होतो. हा रंगबदल नेमका केव्हा होतो हे ठरविणे कठीण असते (pH ४·४ ते ३·१). याकरिता त्याच्याबरोबर इंडिगो कॅरमीन किंवा झायलीन सायनॉल एफ. एफ. यांच्यापैकी एक निष्क्रिय रंजक वापरतात. यामध्ये क्षारक अवस्थेतून अम्ल अवस्थेत जाताना हिरवा–करडा–नीलातिरक्त असा रंगबदल होतो. करडी अवस्था ३·८ असताना येते.
अकार्बनी दर्शक: काही धातवीय लवणांच्या विद्रावांचा उपयोग अनुमापनात दर्शक म्हणून केला जातो. उदा., पोटॅशियम क्रोमेट, पोटॅशियम फेरोसायनाइड.
दर्शक कागद : दर्शकाच्या विद्रावात गालन पत्र किंवा खास बनविलेला कागद बुडवितात, सुकवितात व त्याच्या लहान लहान पट्ट्या तयार करतात. अशा पट्ट्यांचा उपयोग द्रवाची अम्लता वा क्षारकता त्याचप्रमाणे निरनिराळी pH मूल्ये ठरविण्यासाठी करण्यात येतो. उदा., लिटमस कागद.
|
काही महत्त्वाची दर्शके, त्यांची pH कक्षा व रंगबदल. |
|||
|
दर्शकाचे नाव |
पीएच कक्षा |
रंगबदल (अम्लाकडून क्षारकाकडे) |
|
|
मिथिल व्हायोलेट |
०–२, ५–६ |
पिवळा ते निळसर जांभळा ते जांभळा |
|
|
मेटा–क्रेसॉल पर्पल |
१·२–२·८ |
} |
तांबडा ते पिवळा ते जांभळा (पर्पल) |
|
|
७·३–९·० |
||
|
थायमॉल ब्ल्यू |
१·२–२·८ |
} |
तांबडा ते पिवळा ते निळा |
|
|
८·०–९·६ |
||
|
ट्रोपिओलीन OO |
|
|
|
|
(ऑरेंज IV) |
१·४–३·० |
तांबडा ते पिवळा |
|
|
ब्रोमोफिनॉल ब्ल्यू |
३·०–४·६ |
पिवळा ते निळा |
|
|
मिथिल ऑरेंज |
२·८–४·० |
नारिंगी ते पिवळा |
|
|
ब्रोमोक्रेसॉल ग्रीन |
३·८–५·४ |
पिवळा ते निळा |
|
|
मिथिल रेड |
२·४–६·३ |
तांबडा ते पिवळा |
|
|
क्लोरोफिनॉल रेड |
५·०–६·८ |
पिवळा ते तांबडा |
|
|
ब्रोमोक्रेसॉल पर्पल |
५·२–६·८ |
पिवळा ते जांभळट |
|
|
ब्रोमोथायमॉल ब्ल्यू |
६·०–७·६ |
पिवळा ते निळा |
|
|
फिनॉल रेड |
६·८–८·४ |
पिवळा ते तांबडा |
|
|
दर्शकाचे नाव |
पीएच कक्षा |
रंगबदल (अम्लाकडून क्षारकाकडे) |
|
|
क्रेसॉल रेड |
२·०–३·० |
} |
नारिंगी ते उदी ते तांबडा |
|
|
७·२–८·८ |
||
|
ऑर्थो–क्रेसॉलप्थॅलीन |
८·२–९·८ |
रंगहीन ते तांबडा |
|
|
फिनॉलप्थॅलीन |
८·४–१०·० |
रंगहीन ते गुलाबी (पिंक) |
|
|
थायमॉलप्थॅलीन |
१०·०–११·० |
रंगहीन ते तांबडा |
|
|
ॲलिझरीन यलो |
|
|
|
|
जीजी |
१०·०–१२·० |
पिवळा ते लिलिॲक |
|
|
मॅलॅकाइट ग्रीन |
११·४–१३·० |
हिरवा ते रंगहीन |
|
|
मिथिल ऑरेंज + |
|
|
|
|
झायलीन सायनॉल |
|
|
|
|
एफ. एफ. |
३·८–४·१ |
जांभळा ते हिरवा |
|
|
ब्रोमोक्रेसॉल ग्रीन + |
|
|
|
|
मिथिल ऑरेंज |
४·३ |
नारिंगी ते निळा–हिरवा |
|
|
ब्रोमोक्रेसॉल ग्रीन + |
|
|
|
|
क्लोरोफिनॉल रेड |
६·१ |
फिकट हिरवा ते निळा जांभळा |
|
|
मिथिल रेड + |
|
|
|
|
मिथिलीन ब्ल्यू |
५.३ |
तांबडा–जांभळा ते हिरवा |
|
|
फिनॉलप्थॅलीन+ |
|
|
|
|
मिथिलीन ग्रीन |
८.८ |
हिरवा ते जांभळा |
|
|
फिनॉलप्थॅलीन + |
|
|
|
|
आल्फानॅप्थॉलप्थॅलीन |
८.९ |
फिकट गुलाबी ते जांभळा |
|
|
फिनॉलप्थॅलीन + |
|
|
|
|
थायमॉल ब्ल्यू |
९.० |
पिवळा ते जांभळा |
|
|
फिनॉलप्थॅलीन + |
|
|
|
|
थायमॉलप्थॅलीन |
९·९ |
रंगहीन ते जांभळा |
|
उपयोग : उदासिनीकरण क्रियेचा अंतिम बिंदू दर्शविण्यासाठी, एखाद्या विद्रावाचे pH मूल्य दर्शविण्यासाठी, ऑक्सिडीभवन–क्षपण विक्रिया, अवक्षेपण विक्रिया तसेच रसायनशास्त्रातील इतर विक्रियांचे नियंत्रण इत्यादींसाठी दर्शकांचा उपयोग करण्यात येतो.
पहा : अनुमापन.
संदर्भ : 1. Parks, G. D. Mellor’s Modern Inorganic Chemistry, London, 1961.
2. Sneed, M. C. Maynard, J. L. General Inorganic Chemistry, New York, 1942.
क्षीरसागर, अनुपमा मिठारी, भू. चिं.
“