फॉर्माल्डिहाइड : अलिफॅटिक आल्डिहाइड श्रेणीतील [⟶ आल्डिहाइडे] सर्वांत साधे व पहिले संयुग. याला ‘मिथेनाल’ असेही म्हणतात. संरचना HCH = O. नेहमीच्या तापमानास हे वायुरूप असून मुख्यतः याचे जलीय विद्राव व्यवहारात वापरले जातात. त्यात काही प्रमाणात मिथिल अल्कोहॉल परिरक्षक म्हणून मिसळलेले असते म्हणजे त्यामुळे फॉर्माल्डिहाइडाचे बहुवारिकीकरण [अनेक साध्या रेणूंच्या संयोगाद्वारे जटिल रेणू बनण्याची प्रक्रिया ⟶ बहुवारिकीरण] होणे टळते. हे विद्राव फॉर्मॅलीन, फॉर्माल (४०% फॉर्माल्डिहाइड, ८% मिथिल अल्कोहॉल व ५२% पाणी) या नावांनीही ओळखले जातात.
इतिहास : इ. स. १८५९ मध्ये ए. एम्. बूटल्येरॉव्ह यांनी मिथिलीन डाय-ॲसिटेटाचे जलीय विच्छेदन केले (पाण्याच्या साहाय्याने रेणूचे तुकडे केले) तेव्हा अपेक्षित मिथिलीन ग्लायकॉल या संयुगाऐवजी फॉर्माल्डिहाइड बनले. ही गोष्ट त्यांच्या लक्षात आली नव्हती, तरी या संयुगाचे हे आद्य संश्लेषण (कृत्रिम रीतीने झालेली निर्मिती) होय. त्यानंतर १७६८ मध्ये ए. डब्ल्यू. फोन होफमान यांनी प्लॅटिनम उत्प्रेरक (प्रत्यक्ष विक्रियेत भाग न घेता तिचा वेग बदलणारा पदार्थ) वापरून मिथिल अल्कोहॉलाचे ऑक्सिडीकरण [⟶ ऑक्सिडीभवन] करून हे तयार केले. याच्या उत्पादनासाठी योग्य अशी, तांबे उत्प्रेरक असलेली, एक पद्धत १८८६ मध्ये ओ. लो यांनी व चांदी हे उत्प्रेरक असलेली ओ. ब्लँक यांनी १९१० मध्ये शोधून काढली. खनिज तेल उद्योगातील वायूपासून फॉर्माल्डिहाइड बनविण्याच्या प्रक्रियाही उपलब्ध आहेत. त्या १९२५ मध्ये जॉन सी. वॉकर यांनी केलेल्या संशोधनावर आधारित आहेत.
फॉर्माल्डिहाइडाचे व्यापारी उत्पादन प्रथम जर्मनीत १८८८ मध्ये सुरू झाले. त्यानंतर अमेरिकेत १९०१ मध्ये व भारतात १९२९ मध्ये त्याचे उत्पादन होऊ लागले. १९१० मध्ये फिनॉलिक रेझिने [⟶ प्लॅस्टिक व उच्च बहुवारिके] प्रचारात आल्यापासून त्याचे उत्पादन वाढू लागले.
उत्पादन : मिथिल अल्कोहॉलाचे बाष्पावस्थेत हवेच्या साहाय्याने ऑक्सिडीकरण घडवून फॉर्माल्डिहाइडाचे व्यापारी उत्पादन केले जाते. त्यासाठी मिथिल अल्कोहॉल व हवा शुद्ध असावी लागतात अन्यथा उत्प्रेरकावर अनिष्ट परिणाम होतो.
शुद्ध मिथिल अल्कोहॉलाचे बाष्प व हवा यांचे मिश्रण (३०-३५% मिथिल अल्कोहॉल) तापवून उत्प्रेरकाच्या थरावरून प्रवाहित केले जाते. उत्प्रेरक म्हणून तांब्यापेक्षा चांदी जास्त कार्यक्षम ठरली आहे. विक्रियेचे तापमान ४५०° – ६५०° से. दरम्यान राखतात आणि विक्रियेनंतर मिळणाऱ्या बाष्पमिश्रणातील फॉर्माल्डिहाइड आणि उरलेले मिथिल अल्कोहॉल विरघळवून काढून घेतात सु. ३०-३६ % फॉर्माल्डिहाइड, २०–२४ % पाणी व बाकीचे मिथिल अल्कोहॉल असलेले मिश्रण मिळते. विभाजन स्तंभाचा (मिश्रणातील कमी व जास्त उकळबिंदू असलेले घटक सावकाशपणे वेगळे करणाऱ्या उपकरणाचा) उपयोग करून त्यापासून ३७% फॉर्माल्डिहाइड व परिरक्षक म्हणून आवश्यक तेवढे मिथिल अल्कोहॉल असलेला विद्राव वेगळा काढतात.
लोह, मॉलिब्डेनम किंवा व्हॅनेडियम यांच्या ऑक्साइडांची मिश्रणेही उत्प्रेरक म्हणून उपयोगी पडतात. ती वापरताना वरील प्रक्रियेत लागते त्यापेक्षा हवेचे प्रमाण ५ ते १० पटींनी जास्त असावे लागते व विक्रिया तापमान ३००° – ४५०° से. ठेवतात. या प्रक्रियेने वापरलेल्या बहुतेक सर्व मिथिल अल्कोहॉलाचे ऑक्सिडीकरण घडून येते व त्यामुळे उत्पादित मिश्रणात मिथिल अल्कोहॉलाचे प्रमाण अत्यल्प असते.
ब्युटेन, प्रोपेन, मिथेन (नैसर्गिक इंधन वायू) या हायड्रोकार्बनांचे दाबाखाली हवेने अथवा ऑक्सीजनाने ऑक्सिडीकरण केले असता फॉर्माल्डिहाइड व त्याबरोबर मिथिल अल्कोहॉल, ॲसिटाल्डिहाइड, प्रोपिल अल्कोहॉल, प्रोपिऑनाल्डिहाइड व कार्बनी अम्ले इत्यादींचे मिश्रण मिळते. त्यापासून फॉर्माल्डिहाइड वेगळे करावे लागते. एका प्रक्रियेत ब्युटेन वायू प्रथम तापवून तो दर चौ. सेंमी. ला २१ ते २८ किग्रॅ. दाब असलेल्या हवा व वाफ यांच्या ४००° से. तापमानाच्या मिश्रणात समाविष्ट करतात. विक्रियेने जे मिश्रण मिळते त्यातून फॉर्माल्डिहाइड वेगळे काढतात. १०० किग्रॅ. ब्युटेनापासून सु. १५ किग्रॅ. फॉर्माल्डिहाइड मिळते. त्याचबरोबर ॲसिटाल्डिहाइड, ॲसिटोन, मिथिल अल्कोहॉल, प्रोपिल अल्कोहॉल, ब्युटिल अल्कोहॉल व कार्बनी अम्ले ही मिळतात.
नैसर्गिक वायूपासून ४३०°–४८०° से. तापमान, ७-२० वातावरणांइतका दाब (वातावरणाच्या दाबाच्या ७-२० पट दाब) आणि ॲल्युमिनियम फॉस्फेट व धातूंची ऑक्साइडे यांची मिश्रणे ही प्रवेगके (विक्रियेची गती वाढविणारे पदार्थ) म्हणून वापरली असता २०-३० टक्के फॉर्माल्डिहाइड व ३०-६० टक्के मिथिल अल्कोहॉल यांचे मिश्रण मिळविता येते.
गुणधर्म : फॉर्माल्डिहाइड हा एक वर्णहीन, तिखट किंवा उग्र वासाचा आणि डोळे, नाक व घसा यांतील श्लेष्मकलेचा (बुळबुळीत अस्तराचा) क्षोभ करणारा वायू आहे. कमी तापमानास ते द्रवरूप बनते. त्याचा गोठणबिंदू -११८° से. व उकळबिंदू -१९·२°से. आहे. फॉर्माल्डिहाइड ज्वालाग्राही असून हवा व ऑक्सिजन यांबरोबर त्याचे स्फोटक मिश्रण बनते. पाणी व अल्कोहॉल यांसारख्या ध्रुवीय विद्रावकांत (ज्यांच्या रेणूंमध्ये धन व ऋण विद्युत् भार कायमचे अलग असतात अथवा धन व ऋण विद्युत् भारांची केंद्रे एकाच ठिकाणी नसतात अशा विरघळविणाऱ्या पदार्थात) ते पूर्णपणे आणि ॲसिटोन, बेंझीन, क्लोरोफॉर्म, ईथर इत्यादींमध्ये थोड्या प्रमाणात विरघळते. जलीय विद्रावात त्याचे मोनोहायड्रेट, मिथिलीन ग्लायकॉल आणि कमी रेणुभारांची बहुवारिकी हायड्रेटे यांचे समतोल मिश्रण असते. याच्या व्यापारी विद्रावात सु. १५ टक्क्यांपर्यंत मिथिल अल्कोहॉल मिसळलेले असते. त्यामुळे त्याची अविद्राव्य बहुवारिके बनत नाहीत. फॉर्माल्डिहाइड अत्यंत विक्रियाशील आहे. ते रासायनिक संयुगांच्या बहुतेक सर्व वर्गांशी विक्रिया करू शकते.
फॉर्माल्डिहाइडाचा जलीय विद्राव शुष्क होईपर्यंत आटविला असता पॅराफॉर्माल्डिहाइड (CH2O)n·H2O हे अनेक बहुवारिकांचे मिश्रण तयार होते. यात n चे मूल्य ६ ते ५० असते व तापविल्याने यापासून पुन्हा फॉर्माल्डिहाइड मिळते.
संहत (पाण्यापासून विद्रावातील प्रमाण जास्त असलेल्या) सल्फ्यूरिक अम्लाच्या विक्रियेने पॉलिऑक्सिमिथिलीन (CH2O)n ·H2O (n = १०० पेक्षा जास्त) हे पांढरे व पाण्यात अविद्राव्य (न विरघळणारे) बहुवारिके बनते. तापविल्याने यापासूनही फॉर्माल्डिहाइड तयार होते.
फॉर्माल्डिहाइडाचा जलीय विद्राव (६० टक्के) थोड्या सल्फ्यूरिक अम्लाबरोबर मिसळून ऊर्ध्वपातन (मिश्रण तापवून व बनणारे बाष्पमिश्रण थंड करून घटक अलग मिळविण्याची क्रिया) केले म्हणजे ट्रायऑक्सिमिथिलीन (CH2O)3 हे ६१°–६२° से. वितळबिंदू असलेले संयुग बनते [⟶ आल्डिहाइडे]. हे कार्बनी विद्रावकांत विरघळते. निर्जल फॉर्माल्डिहाइड बनविण्यासाठी हे उपयोगी पडते.
कॅल्शियम हायड्रॉक्साइडासारख्या दुर्बल (पाण्यातील विद्रावात OH–आयन-विद्युत् भारित अणुगट-कमी प्रमाणात निर्माण होतात अशा) क्षारांच्या (अम्लाशी विक्रिया झाल्यास लवणे देणाऱ्या पदार्थांच्या) उपस्थितीत फॉर्माल्डिहाइडापासून C6H12O6 या सूत्राच्या शर्करांचे मिश्रण बनते. त्याला ‘फॉर्मोज’ किंवा ‘आल्फा ॲक्रोज’ म्हणतात.
प्रबल क्षारांच्या उपस्थितीत बेंझाल्डिहाइडावर फॉर्माल्डिहाइडाची विक्रिया होऊन बेंझिल अल्कोहॉल व सोडियम फॉर्मेट ही संयुगे तयार होतात [⟶ आल्डिहाइडे].
ज्या आल्डिहाइडांमध्ये आल्फा (α) स्थानी हायड्रोजनाचा एक अणू असेल, त्यांच्यावर फॉर्माल्डिहाइडाची विक्रिया होते व βहायड्रॉक्सी आल्डिहाइडे बनतात. तसेच फॉर्माल्डिहाइड अतिरिक्त असेल, तर या β हायड्रॉक्सी आल्डिहाइडावरही विक्रिया होऊन अखेर प्रतिष्ठापित ट्रायमिथिलीन ग्लायकॉल हे मध्यस्थ म्हणजे अंतिम संयुग मिळण्याच्या मार्गातील एक टप्पा असलेले संयुग बनते.
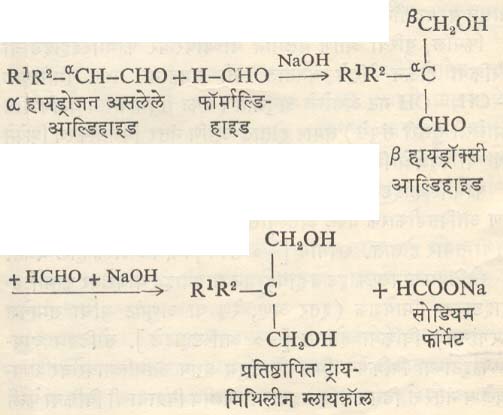
आल्फा स्थानी दोन हायड्रोजन अणू असलेल्या आल्डिहाइडापासून क्रमाक्रमाने विक्रिया घडून शेवटी ट्रिसहायड्रॉक्सिमिथिल संयुग बनते. ॲसिटाल्डिहाइडापासून (तीन आल्फा हायड्रोजन अणू असलेले एक आल्डिहाइड) पॅराआल्डिहाइडाचे जलीय संधारण (सूक्ष्म व लोंबकळते कण व पाणी यांचे मिश्रण) आणि कॅल्शियम ऑक्साइडाची पूड वापरून विक्रिया केल्यास पेंटा-इरिथ्रिटॉल हे महत्त्वाचे संयुग बनविता येते. याचे टेट्रानायट्रेट एक स्फोटक द्रव्य म्हणून प्रसिद्ध आहे. ॲसिटाल्डिहाइड व फॉर्माल्डिहाइड यांच्यामधील विक्रियेने बीटा हायड्रॉक्सी प्रोपिऑनाल्डिहाइड हे संयुग बनते त्याचे निर्जलीकरण करून ॲक्रोलीइन तयार करण्याची एक कृती ज्ञात आहे. रेझिने, औषधिद्रव्ये इत्यादींमध्ये ॲक्रोलीइन वापरले जाते.
विक्रियाशील (ज्यात सहजपणे रासायनिक बदल होऊ शकेल असा) हायड्रोजन अणू असलेल्या कीटोनावर फॉर्माल्डिहाइड आणि एखादे द्वितीयक अमाइन हायड्रोक्लोराइड [⟶ अमाइने] यांची मिळून विक्रिया, लवमात्र हायड्रोक्लोरिक अम्लाच्या उपस्थितीत घडते व एक मध्यस्थ संयुग बनते याला कार्ल मॅनिश या जर्मन रसायनशास्त्रज्ञांच्या नावावरून ‘मॅनिश लवण’ म्हणतात. याचे विघटन केल्यास α βअसंतृप्त कीटोन मिळते. ही मॅनिश विक्रिया संश्लेषणाच्या दृष्टीने महत्त्वाची आहे.
अम्ल उत्प्रेरकाने ओलेफिनांवर [⟶ ॲलिफॅटिक संयुगे] विक्रिया होऊन १ : ३ ग्लायकॉल आणि १ : ३ डायऑक्झेन या वर्गाच्या संयुगांचे मिश्रण मिळते. अमोनियाबरोबर विक्रिया होऊन फॉर्माल्डिहाइडापासून हेक्झामिथिलीन टेट्रामाइन हे एक महत्त्वाचे संयुग मिळते. त्याचा उपयोग औषधांत आणि सायक्लोनाइट हे स्फोटक द्रव्य, रेझिने, प्लॅस्टिके इ. बनविण्यासाठी केला जातो.
अमोनियम क्लोराइडवर (नवसागरावर) फॉर्माल्डिहाइडाच्या जलीय विद्रावाची विक्रिया केली असता मिथिल अमाइन हायड्रोक्लोराइड CN3N+H3CI– बनते. पॅराफॉर्माल्डिहाइड वापरले असता विक्रिया उच्च तापमानास घडविता येते आणि ट्रायमिथिल अमाइन हायड्रोक्लोराइड (CH3)3 ·N+HCI– तयार होते. ग्रीन्यार विक्रियाकारकांच्या [व्हिक्तॉर ग्रीन्यार यांनी शोध लावल्याने त्यांच्या नावाने ओळखण्यात येणाऱ्या विक्रिया घडविण्यास साहाय्य करणाऱ्या संयुगांच्या ⟶ ग्रीन्यार विक्रिया] विक्रियेने फॉर्माल्डिहाइडापासून प्राथमिक अल्कोहॉले मिळतात [⟶ आल्डिहाइडे].
फॉर्माल्डिहाइड किंवा पॅराफॉर्माल्डिहाइड आणि हायड्रोक्लोरिक अम्ल यांची झिंक क्लोराइड वापरून विक्रिया केली असता ⇨ ॲरोमॅटिक संयुगांतील हायड्रोजनाची क्लोरोमिथिल –CH2-CI या गटाने प्रतिष्ठापन (जागा घेतली जाण्याची क्रिया) करता येते. उदा., बेंझिनापासून या पद्धतीने बेंझिल क्लोराइड (C6H5CH2CI) बनविता येते.
फिनॉल, यूरिया आणि मेलॅमीन यांच्याबरोबर फॉर्माल्डिहाइडाची विक्रिया होऊन रेझिने बनतात. ती बनताना प्रथम मिथिलाल –CH2-OH गट असलेले अनुजात (एका संयुगापासून बनविण्यात आलेली दुसरी संयुगे) तयार होतात आणि नंतर निर्जलीकरण क्रियेने त्यांच्या रेणूंमध्ये मिथिलीन –CH2 बंध निर्माण होतात.
फॉर्माल्डिहाइडाच्या नियंत्रित ऑक्सिडीकरणाने फॉर्मिक अम्ल बनते पण ऑक्सिडीकारक प्रबल असल्यास त्यापासून कार्बन मोनॉक्साइड व पाणी तयार होतात. क्षपणाने [⟶ क्षपण] मिथिल अल्कोहॉल बनते.
सोडियम बायसल्फाइड व हायड्रोजन सायनाइड यांबरोबर फॉर्माल्डिहाइडाच्या समावेशक (इतर अणू, रेणू वा अणुगट यांचा समावेश करणाऱ्या) विक्रिया होतात [⟶ आल्डिहाइडे]. सोडियम बायसल्फाइटाच्या विक्रियेने मिळणारे संयुग प्रथम ॲनिलिनाबरोबर तापविले व नंतर सोडियम सायनाइडाच्या जलीय विद्रावाची विक्रिया केली असता फिनिल ॲमिनो ॲसिटोनायट्राइल (C6H5NH-CH2CN) मिळते. त्याचे जलीय विच्छेदन करून फिनिल ग्लायसीन (C6H5-NH-CH2-COOH) हे निळीच्या संश्लेषणातील महत्त्वाचे संयुग बनविता येते.
फॉर्माल्डिहाइडाचे व्यापारी विद्राव : अमेरिकेच्या संयुक्त संस्थानांच्या औषधिकोशानुसार तयार केलेल्या फॉर्माल्डिहाइडाच्या जलीय विद्रावात कमीत कमी ३७ टक्के (वजनी) फॉर्माल्डिहाइड असून ६ ते १५ टक्के मिथिल अल्कोहॉल परिरक्षक म्हणून मिसळलेले असते. हे स्वच्छ व जवळजवळ वर्णहीन असून त्याला फॉर्माल्डिहाइडाचा वास येतो. त्याची अम्लता, फॉर्मिक अम्लाच्या ( H·COOH ) रूपाने ०·०१ ते ०·०३ असून pH मूल्य २·८ ते ४ असते [⟶ पीएच मूल्य]. फॉर्माल्डिहाइडाचे प्रमाण ४५ ते ५० टक्के आणि मिथिल अल्कोहॉलाचे प्रमाण कमी असलेले विद्रावही उपलब्ध आहेत.
मिथिल अल्कोहॉल, n – प्रोपेनॉल, n – ब्युंटेनॉल व आयसोब्युटेनॉल यांमधील याचे विद्रावही मिळतात. ज्या उपयोगात अल्कोहॉल उपस्थित असावे व पाण्याचे प्रमाण अत्यल्प असावे अशी अपेक्षा असते, त्याकरिता हे उपयोगी पडतात.
उपयोग: उत्पादनापैकी निम्याहून अधिक फॉर्माल्डिहाइड फिनॉल, यूरिया, मेलॅमीन इत्यादींची रेझिने त्याचप्रमाणे ॲनिलीन, ॲरोमॅटिक हायड्रोकार्बने, कीटोने, यूरेथेने इत्यादींपासून बनणारी रेझिने यांसाठी वापरले जाते. वस्त्रोद्योगातील अनेक प्रक्रियांत उदा., वस्त्र चुण्या न पडणारे, न आटणारे व ज्वलनरोधी व्हावे म्हणून करावयाच्या संस्कारांत [⟶ कापडावरील अंतिम संस्करण] आणि पॉलिव्हिनिल अल्कोहॉल व प्रथिने यांचे तंतू बनविण्याच्या प्रक्रियांत फॉर्माल्डिहाइड उपयोगी पडते. कागदाच्या उत्पादनात ओल्या कागदाला पुरेशी बळकटी यावी आणि पृष्ठभागावर लेप दिलेले कागद पुरेसे जलरोधी व्हावेत यांसाठी फॉर्माल्डिहाइड आणि त्याचे अनुजात वापरले जातात. कातडी कमावण्यासाठी उपयोगी पडणारे संश्लिष्ट (कृत्रिम रीतीने बनविलेले) पदार्थ बनविण्यासाठी चर्मोद्योगात आणि विकासक (अदृश्य प्रतिमा दृश्य करण्यासाठी वापरावयाची) संयुगे बनविण्यासाठी छायाचित्रणात फॉर्माल्डिहाइड अनेक ठिकाणी उपयोगी पडते. एथिलीन ग्लायकॉल, हेक्झामिथिलीन टेट्रामाइन (हेक्झॅमीन, यूरोट्रोपिन), पेंटा-इरिथ्रिटॉल, फिनिल ग्लायसीन, मिथिलीन बिस् क्लोरोफिनॉल इ. महत्त्वाच्या पदार्थांच्या संश्लेषणात फॉर्माल्डिहाइड हे एक महत्त्वाचे विक्रियाकारक आहे. यांशिवाय अनेक ऑक्सिकरणरोधके (ऑक्सिडीकरणास विरोध करणारे पदार्थ), रंग, विद्युत् विलेपन साहाय्यके, रबर धंद्यातील प्रवेगक [⟶ रबर ], पृष्ठक्रियाकारके [⟶ पृष्ठक्रियाकारके], आसंजके (चिकटणारे पदार्थ) इत्यादींच्या उत्पादनात ते वापरले जाते. कृषी उद्योगात बीजे व गहू, बार्ली यांसारखी धान्ये यांचे रोगापासून संरक्षण व्हावे म्हणून त्यांवर फॉर्माल्डिहाइडाचा संस्कार करतात. वस्तुसंग्रहालयात प्राणिज नमुने टिकविण्यासाठी तसेच जमिनीच्या निर्जंतुकीकरणासाठीही ते वापरले जाते.
हाताळणी : (वापरताना घ्यावयाची काळजी). डोळे, नाक व घसा यांना फॉर्माल्डिहाइड क्षोभकारक आहे. तसेच त्याचा कातडीशी संपर्क आल्यास त्वक्शोथ (कातडीची दाहयुक्त सूज) संभवतो. यापासून संरक्षण व्हावे म्हणून ते बंद पात्रात वापरले जाईल अशी योजना केलेली असते. ती शक्य नसेल, तर हवेमध्ये त्याचे प्रमाण फार वाढू नये म्हणून हवा खेळती ठेवण्यासाठी पंखे असावे लागतात. तापमान २५° से. आणि ७६० मिमी. वातावरणीय दाब असताना १ लक्ष भाग हवेत १ भाग म्हणजेच १ लिटर हवेत फॉर्माल्डिहाइडाचे प्रमाण ०·०१२ मिग्रॅ.पेक्षा जास्त नसेल, तर अशा हवेचा दररोज ८ तास संपर्क बाधक होत नाही. त्वचेशी संपर्क टाळण्यासाठी जलरोधी मोजे वापरणे किंवा लॅनोलिनासारख्या जलरोधी पदार्थाचे त्वचेस लेपन करणे आवश्यक असते. फॉर्माल्डिहाइड त्वचेस लागल्यास तो भाग साबणाच्या पाण्याने ताबडतोब धुतात. पॅराफॉर्माल्डिहाइड वापरताना तोंडावर मुखवटा वापरावा लागतो आणि संपर्क झाल्यास ते भाग प्रथम अमोनिया व नंतर पाण्याने धुणे आवश्यक असते. पोटात गेल्यास पाणी पाजून ते शक्य तितके विरल करतात व डॉक्टरांची मदत घेतात.
भारतीय उत्पादन : इ. स.१९२९ मध्ये किर्लोस्करवाडीच्या इंडस्ट्रियल केमिकल वर्क्स या कारखान्याने फॉर्माल्डिहाइडाचे उत्पादन सुरू केले. १९२९ ते १९३३ या काळात तेथील उत्पादन दरसाल १२० टन होते. त्यानंतर मुंबई सरकारने मिथिल अल्कोहॉलावर अबकारी कर बसविल्याने हा कारखाना बंद पडला. दुसऱ्या महायुद्धकाली भद्रावतीच्या आयर्न अँड स्टील कंपनीने हा कारखाना विकत घेतला व १९४६ पर्यंत उत्पादन केले. तेथे १९४३-४४ मध्ये सर्वाधिक उत्पादन (सु. ५१,८०० किग्रॅ.) झाले. पुढे तेही बंद पडले. त्यानंतर फॉर्माल्डिहाइडाची गरज आयात करून भागवावी लागत होती. ‘सिंद्री फर्टिलायझर अँड केमिकल्स लि.’ ह्या कंपनीने १९५७ पासून मोठ्या प्रमाणावर फॉर्माल्डिहाइडाची निर्मिती करण्याचे योजिले होते. फॉर्माल्डिहाइडाचे विद्राव किंवा बहुवारिके मोठ्या प्रमाणावर आयात केली जातात.
पहा : आल्डिहाइडे.
संदर्भ : 1. C. S. I. R. The Wealth of India, Industrial Products, Part IV, New Delhi, 1957.
2. Faith, W. L. and others, Industrial Chemicals, New York, 1965.
3. Walker, J. F. Formeldehyde, London, 1964.
गाळकर, ना. तु.
“