ॲस्कॉर्बिक अम्ल : सुत्र C6H8O6. प्रकाशीय सक्रियतेनुसार (एकाच प्रतलात कंप पावणाऱ्या म्हणजे ध्रुवित प्रकाशाच्या कंपनाचे प्रतल फिरविण्याच्या क्षमतेनुसार) ॲस्कॉर्बिक अम्लाचे एल-ॲस्कॉर्बिक अम्ल (प्रतल डाव्या बाजूस फिरविणारे) व डी-ॲस्कॉर्बिक अम्ल (प्रतल उजव्या बाजूस फिरविणारे) असे दोन प्रकार आहेत. एल-ॲस्कॉर्बिक अम्ल म्हणजे क जीवनसत्त्व होय. त्याशिवाय ते रेडॉक्सान, सेलीन इ. नावांनीही बाजारात विकले जाते. डी- ॲस्कॉर्बिक अम्लाची जैव सक्रियता (प्राण्याच्या शरीरातील क्रियांच्या दृष्टीने क्रियाशीलता) एल- ॲस्कॉर्बिक अम्लापेक्षा फार कमी असल्याने त्याला फारसे महत्त्व नाही. पुढील वर्णन एल-ॲस्कॉर्बिक अम्लाचे (क जीवनसत्त्वाचे) आहे.
शुद्ध ॲस्कॉर्बिक अम्ल गंधहीन पांढरे स्फटिकरूप असून पाण्यात मोठ्या प्रमाणात विरघळते, तर कित्येक कार्बनी विद्रावांत ते जवळजवळ अविद्राव्य राहते (विरघळत नाही). अल्कोहॉलामध्ये शेकडा दोन प्रमाणात विरघळते. त्याचा द्रवांक (वितळबिंदू) १९००—१९२० से. असून या तापमानाला त्याचे विघटनही (संयुगांचे तुकडे पडून घटक द्रव्ये वेगळी होणे) होते. हेक्सोजापेक्षा त्याच्यात क्षपणशक्ती [→क्षपण] अधिक असते.
स्कर्व्ही नावाचा, क जीवनसत्त्वाच्या त्रुटीमुळे होणारा, रोग फार वर्षांपासून ज्ञात आहे. विशेषत्वे खलाशांमध्ये त्याचे प्रमाण अधिक आढळून येत असे. १५९३ साली हॉकिन्झ यांनी हा आजार मोसंबी व संत्री यांच्या रसांनी बरा करता येतो हे दाखविले. तेव्हापासून गेली ३५० वर्षे स्कर्व्हीवर विशिष्ट ताज्या फळांचा रस औषध म्हणून प्रचलित आहे. १९२८ साली कोबी व तांबडी मिरी यांच्यापासून सेंट-ड्यर्ड्यी यांनी वेगळ्या केलेल्या पदार्थास हॅक्सुरॉनिक अम्ल हे नाव दिले. १९३२ साली वॉ व किंग यांनी कागदी लिंबापासून क जीवनसत्त्व शुद्धावस्थेत वेगळे केले व हेक्सुरॉनिक अम्ल व क जीवनसत्त्व हे दोन्ही पदार्थ एकच असल्याचे दाखविले. हार्थ व हीर्स्ट यांनी १९३३ मध्ये या पदार्थाचे रासायनिक सूत्र ठरविले. याच साली हार्थ व सेंट-ड्यर्ड्यी यांच्या सूचनेनुसार स्कर्व्ही हा रोग बरा करण्याच्या त्याच्या गुणावरून त्याला अस्कॉर्बिक अम्ल हे नाव देण्यात आले. वर्षभरातच निसर्गात मिळणाऱ्या ॲस्कॉर्बिक अम्लाबरहुकूम ते संश्लेषणाने (कृत्रिम रीतीने) बनविता येऊ
लागले.
या पदार्थाचे रासायनिक सूत्र पुढीलप्रमाणे आहे :
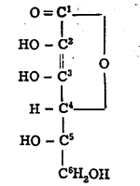
कार्बनी अम्लांची अम्लता सामान्यतः त्यांतील संरचनेतील COOH या कार्बॉक्सी गटाच्या विगमनाने (गटातील अणू वेगळे होऊन आयन बनण्यामुळे) निमार्ण झालेल्या H+ मुळे (हायड्रोजनाच्या अणूतील इलेक्ट्रॉन निघून गेल्यावर राहिलेल्या धनभारित कणामुळे) असते. ॲस्कॉर्बिक अम्ल COOH गट नाही, परंतु त्यातील C3 या अणूस जोडलेला OH गट ईनॉलरूप [→चलसमघटकता] असल्यामुळे त्यापासून H+ बनतो व त्यामुळे हे संयुग अम्लधर्मी आहे.
वाढत्या तापमानाबरोबर व pH मूल्याबरोबर [→पीएच मूल्य] ॲस्कॉर्बिक अम्लाचे ऑक्सिडीभवनही वाढते व त्यामुळे ॲस्कॉर्बिक अम्लाचे स्थैर्य घटत जाते. खाद्य पदार्थ साठविताना अगर तयार करताना योग्य ती दक्षता न घेतल्यास वरील कारणाने त्यातील ॲस्कॉर्बिक अम्लाचा बराचसा भाग नाहीसा होतो, हे लक्षात ठेवले पाहिजे. फळांचे रस टिकविण्याकरिता ते डब्यात बंद करण्यापूर्वी नायट्रोजन किंवा कार्बन डाय-ऑक्साइड यांच्या साहाय्याने डब्यातील हवा (ऑक्सिजन) काळजीपूर्वक संपूर्णपणे बाहेर काढणे जरूर असते.
ॲस्कॉर्बिक अम्लाच्या क्षपणाच्या गुणधर्माचा उपयोग रासायनिक पद्धतीने पदार्थातील त्याचे प्रमाण ठरविण्याकरिता करतात. याकरिता अनेक क्षपणशील रंगांचा उपयोग होऊ शकतो. क्षपणाच्या क्रियेने या रंगीत पदार्थाचे रूपांतर वर्णहीन पदार्थात होते. त्यामुळे क्रियेची पूर्णावस्था सहज दिसू शकते. वापरलेल्या रंगाचा रेणूभार व त्यास वर्णहीन करण्याकरिता लागलेल्या ॲस्कॉर्बिक अम्लयुक्त पदार्थाचे वजन यावरून त्या पदार्थातील ॲस्कॉर्बिक अम्लाचे प्रमाण आकडेमोडीने ठरविता येते. २, ६— डायक्लोरो फिनॉल इंडोफिनॉल या रंगीत पदार्थाचा या कामी विशेषत्वे उपयोग केला जातो.
लिंबे, संत्री, द्राक्षे, स्ट्रॉबेरी, केळी, पीच, अननस, सफरचंद, डोंगरी आवळे या फळांत आणि टोमॅटो, बटाटे, ओला वाटाणा, कोबी, बीट, गाजर, शेवग्याच्या शेंगा यांसारख्या नित्य वापरल्या जाणाऱ्या भाज्यांत ॲस्कॉर्बिक अम्लाचे प्रमाण भरपूर असते.
काही प्राणी आपल्या गरजेप्रमाणे आपल्या शरीरात स्वतःच याचे उत्पादन करू शकतात. परंतु मनुष्य व गिनी पिग यांच्या ठिकाणी ही शक्ती नसल्याने त्यांना ॲस्कॉर्बिक अम्लाचा पुरवठा अन्नातून व्हावा लागतो. दूध तापविल्याने किंवा निर्जंतुक करण्याने त्यातील ॲस्कॉर्बिक अम्ल नष्ट होते म्हणून लहान मुलांना दुधाबरोबर ॲस्कॉर्बिक अम्लाचा बाहेरून पुरवठा करणे अत्यावश्यक असते. ॲस्कॉर्बिक अम्लाचे ०.०५ मिग्रॅ. म्हणजे एक आंतरराष्ट्रीय एकक समजले जाते.
ॲस्कॉर्बिक अम्ल कमी पडल्यास मनुष्याचे वजन घटते. थकवा वाटू लागतो, हाडे ठिसूळ होतात, सांधे दुखू लागतात व सुजतात, हिरड्यांना सूज येते व सौम्य स्पर्शानेही त्यातून रक्त येऊ लागते. तीव्र अभावामुळे दात अकाली पडू लागतात. सेवन केलेल्या अन्नाचे शरीरास लागणाऱ्या पोषक घटकामध्ये रूपांतर करण्याच्या प्रक्रियेत होणाऱ्या क्षपण व ऑक्सिडीकरण या महत्त्वाच्या विक्रियांत ॲस्कॉर्बिक अम्ल सहभागी होते.
प्राण्यांच्या शरीरात ॲस्किडीकरणामुळे त्याचे रूपांतर डी हायड्रो ॲस्कॉर्बिक अम्लात व त्याच्या क्षपणामुळे परत मूळ ॲस्कॉर्बिक अम्लात सहज होत असले पाहिजे.

ऑक्सिडीकरणाने ज्यांचा नाश होऊ शकेल अशा रेणूंमध्ये हायड्रोजनअणू असलेल्या पदार्थांचे रक्षण करण्यासाठी प्रति-ऑक्सिडीकारक (ऑक्सिडीकरणास विरोध करणारे द्रव्य) म्हणून या अम्लाचा उपयोग होतो. टायरोसीन चपयापचामध्ये (प्राण्यांच्या शरीरात सतत होणाऱ्या भौतिक-रासायनिक घडामोडींमध्ये) किंवा फॉलिक अम्लाचे फॉलिनिक अम्लात रूपांतर करण्याचा विक्रियेत त्याची मदत होत असली पाहिजे.
ब्रिटिश शास्त्रज्ञांच्या मते रोजच्या आहारात ३० मिग्रॅ. पेक्षा जास्त ॲस्कॉर्बिक अम्ल असणे जरूर नाही व इष्टही नाही. मात्र फूड अँड न्यूट्रिशन रिसर्च कौन्सिलची शिफारस अशी आहे की १ ते ३ महिन्यांच्या मुलास रोज ३० मिग्रॅ., मोठ्या माणसास ७५ मिग्रॅ. तर बाळंतिणीस रोज १५० मिग्रॅ. इतक्या ॲस्कॉर्बिक अम्लाची आवश्यकता असते.
उत्पादन पद्धती : मोठ्या प्रमाणात तयार करण्यात आलेले हेच पहिले जीवनसत्त्व होय. याच्या उत्पादनाच्या प्रक्रियेस ग्लुकोजापासून सुरुवात केली जाते. या प्रक्रियेतील रासायनिक क्रियांचे काही महत्त्वाचे टप्पे खालीलप्रमाणे देता येतील : ग्लुकोज → सॉर्बिटॉल → एल-सॉर्बोज → डायॲसिटोन एल-सॉर्बोज → डायॲसिटोन २—कीटो एल-ग्युलॉनिक अम्ल → २—कीटो एल-ग्युलॉनिक अम्ल → एल- ॲस्कॉर्बिक अम्ल.
पहा : जीवनसत्त्वे.
संदर्भ : Sebrell, W. H. Harris, R. S., Ed. Vitamins: Chemistry, Physiology, Pathology, Methods,London, 1967.
शिंगटे, रा. धों.
“