ॲमिनो अम्ले : ज्यांच्यात एक किंवा अधिक क्षारकीय (अम्लांशी विक्रिया झाल्यास लवणे देणारा) ॲमिनो गट (-NH2) व एक किंवा अधिक कार्बॉक्सी गट (-COOH) आहेत, अशा कार्बनी संयुगांना ‘ॲमिनो अम्ले’ म्हणतात. प्रथिनांचे घटक म्हणून आढळणारी व इतर बहुतेक सर्व नैसर्गिक ॲमिनो अम्ले ही आल्फा ॲमिनो अम्ले आहेत. म्हणजे त्यांमध्ये ॲमिनो व कार्बॉक्सी गट एकाच कार्बन अणूला जोडलेले असून त्या अणूचा तिसरा बंध बहुधा हायड्रोजनाने व उरलेला चौथा बंध हा विविध प्रकारच्या गटांनी (R) तृप्त झालेला असतो. सर्वांत
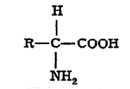
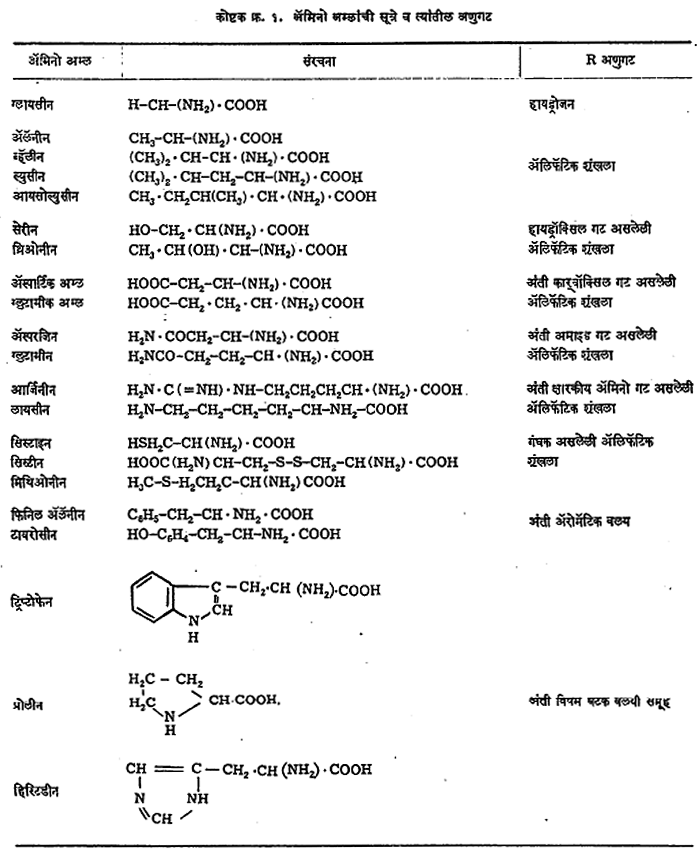
साध्या अशा ग्लायसीन या ॲमिनो अम्लातील R हा हायड्रोजनाचा अणू असतो. इतर सर्व ॲमिनो अम्लांत R हा कार्बनी गट असतो. उदा., ॲलॅनिनामध्ये तो मिथिल (-CH3) गट असतो, तर ग्लुटामिक अम्लात अंती कार्बॉक्सी गट असणारी ॲलिफॅटिक (-CH2.CH2.COOH) शृंखला असते. ऐंशीहून अधिक अशा नैसर्गिक ॲमिनो अम्लांपैकी सु. २० ॲमिनो अम्ले प्रथिनांचे घटक समूह आहेत असे आढळते.
सजीव ऊतकामध्ये (समान कार्य व रचना असणाऱ्या पेशींच्या समूहामध्ये) ॲमिनो अम्ले बहुधा संयोगित (एकमेकांस जोडलेल्या स्थितीत) असून ती पेप्टाइडांच्या स्वरूपात असतात. पेप्टाइडामध्ये एक अम्लाचा ॲमिनो गट दुसऱ्या अम्लाच्या कार्बॉक्सी गटाशी जोडलेला असतो. पेप्टाइडी बंध बनताना पाण्याचा एक रेणू मुक्त होतो, तर तोच बंध तुटताना पाण्याचा एक रेणू मिळवावा लागतो. अशा प्रकारे ॲमिनो अम्ले एकमेकांशी संयोग पावून बऱ्याच लांबीच्या शृंखला बनवू शकतात. प्रथिनांमध्ये पेप्टाइडी बंध असलेले ५० ते कित्येक हजार ॲमिनो अम्लांचे अवशेष असतात.
ॲमिनो अम्लांपासून पेप्टाइड निर्मितीसाठी पुष्कळशा ऊर्जेची आवश्यकता असते. बहुतेक संयोगित ॲमिनो अम्ले निसर्गात प्रथिनांच्या
रूपात असतात परंतु लहान लहान पेप्टाइडेसुद्धा निसर्गात सापडतात व ती क्रियाशील (विक्रिया करण्यास योग्य) असतात.
मुक्त ॲमिनो अम्लांची उपस्थिती : उच्च जिवंत प्राण्यांच्या कोशिकांत (शरीरातील सूक्ष्म घटकांत, पेशींत) व शरीरांतील द्रवात मुक्त ॲमिनो अम्ले सापडतात. त्यांपैकी अमोनियाचे ग्रहण व देवाणघेवाण होण्यास आवश्यक असलेली ग्लुटामिक अम्ल, ॲस्पार्टिक अम्ल व त्यांची अमाइडे ही जरा जास्त प्रमाणात आढळतात. कोशिकासमूहात ॲमिनो अम्लांचे व प्रथिनांचे संश्लेषण (घटक रेणू एकत्र आणून रासायनिक पदार्थ बनविणे) सतत चालू असते तथापि प्रत्यक्षात ओल्या कोशिकासमूहात मुक्त ॲमिनो अम्ले अगदी कमी प्रमाणात म्हणजे काही मि.ग्रॅ.इतकीच असतात. याचे कारण एखादे ॲमिनो अम्ल वाजवीपेक्षा अधिक प्रमाणात तयार झाल्यास ते अम्ल स्वतःच्याच जैव संश्लेषणास प्रतिबंध करते. प्रथिनांच्या घटकांत असणाऱ्या ॲमिनो अम्लांखेरीज इतर ॲमिनो अम्लेही निसर्गात मुक्त स्वरूपात आढळतात. त्यांपैकी काही प्रथिनांच्या चयापचयास (शरीरात सतत घडणाऱ्या रासायनिक भौतिक घडामोडीत) उत्पन्न झालेली असतात. उदा., गॅमा ॲमिनो ब्युटिरिक अम्ल (HOOC-CH2-CH2-CH2-NH2) हे ग्लुटामिक अम्लातील एक कार्बॉक्सिल गट निघून गेल्यामुळे बनते तर ऑर्निथीन [H2N (CH2)3-CH (NH2).COOH] व होमोसेरीन [HOCH2-CH2-CH(NH2).COOH] यांसारखी ॲमिनो अम्ले प्रथिनांतील अम्लांच्या संश्लेषणाच्या प्रक्रियेतील पूर्वगामी (एखादे संयुग तयार होण्यापूर्वी उत्पन्न होणारी) असतात.
भौतिक गुणधर्म : सर्व ॲमिनो अम्ले पाण्यात सहज विरघळतात, अल्कोहॉलांमध्ये अल्प प्रमाणात विरघळतात किंवा विरघळत नाहीत व ईथरांमध्ये विरघळत नाहीत. कमी संहतीच्या (एकक घनफळातील दिलेल्या पदार्थाच्या प्रमाणाच्या) अम्लात व क्षारकात (अम्लाशी विक्रिया करून लवणे देणाऱ्या पदार्थात) विरघळून लवणे मिळतात.
ग्लायसिनाशिवाय इतर सर्व ॲमिनो अम्ले प्रकाशीय गुणधर्म दाखवितात. प्रकाशीय वलन (विशिष्ट पातळीत कंपन पावणारा प्रकाश, म्हणजे ध्रुवित प्रकाश, पदार्थातून गेल्यास प्रकाशाची कंपन पातळी डावीकडे वा उजवीकडे वळणे) हा ॲमिनो अम्लाचा महत्त्वाचा गुणधर्म आहे. ॲमिनो अम्ले ही ध्रुवित प्रकाशाची कंपन पातळी डावीकडे वळवणारी, उजवीकडे वळवणारी किंवा रॅसेमिक म्हणजे दोन्ही प्रकारांचे मिश्रण असणारी आहेत. ॲमिनो अम्लाचे प्रकाशीय वलन, हे ज्यामध्ये त्यांचे विद्राव करतात, त्या विद्रावाच्या pH मूल्यावर (अम्लता वा क्षारकीयता दर्शविणारे मूल्य, →पीएच मूल्य) व विद्रावकावर (विरघळविणाऱ्या पदार्थावर) अवलंबून असते. त्याचप्रमाणे हे वलन विद्रावाच्या तपमानावर व वापरालेल्या प्रकाशावर अवलंबून असते. सोडियम-D प्रकाश तरंगलांबीचा म्हणजे ५,८९० अँगस्ट्रॉम (१ अँगस्ट्रॉम =१०-८ सेंमी.) तरंगलांबीचा प्रकाश वापरल्यास वलन [α]D असे दर्शविले जाते. ॲमिनो अम्लांच्या प्रकाशीय वलनांची तुलना करताना ही वलने एकाच विद्रावकामधील सममूल्या विद्रावाची (एक लिटर विद्रावात विक्रियाशील पदार्थाचा एक ग्रॅम रेणुभार असलेल्या विद्रावाची) एकाच तपमानाला घेऊन तुलना करतात. विद्रावामधील ॲमिनो अम्लांची संहती वाढविल्यास प्रकाशीय वलन विशिष्ट मर्यादेपर्यंत वाढते. रासायनिक दृष्ट्या उदासीन लवणे घालून काही वेळा प्रकाशीय वलन (डावीकडे वळविणाऱ्याचे उजवीकडे वळविणाऱ्याकडे) बदलता येते. क्षारकाबरोबर, दाबाखाली अम्लाबरोबर वा विशिष्ट परिस्थितीत ॲसिटिक ॲनहायड्राइडाबरोबर ॲमिनो अम्ले तापविल्यास ती रॅसेमिक होतात [→ध्रुवणमिति प्रकाशकी].
ॲमिनो अम्लांमध्ये अम्लीय व क्षारकीय समूह असतात व त्यांची अम्लांबरोबर किंवा क्षारकांबरोबर विक्रिया झाल्यास लवणे मिळतात. म्हणून ॲमिनो अम्ले ही उभयधर्मी संयुगे आहेत. ही अम्ले विद्रावकात विरघळविल्यास त्यांच्या रेणूंचे लहान लहान तुकडे होऊन दोन किंवा अनेक रेणू तयार होतात. तसेच हे फुटून झालेले रेणू एकत्र येऊन मूळ अम्ल तयार होते, यासच विगमन असे म्हणतात. विगमन विक्रियेत समतोल निर्माण झाल्यावर रूपांतरित रेणू व अरूपांतरित रेणू यांच्या गुणोत्तरास विगमन स्थिरांक असे म्हणतात.
उभयधर्मी अम्लांची अम्लीय व क्षारकीय शक्ती वेगवेगळी असते. शुद्ध ॲमिनो अम्लाचा पाण्यातील विद्राव विद्युत् दृष्ट्या उदासीन असतो. अशा विद्रावातील अम्ल व क्षारक समूहाची शक्ती ज्या pH मूल्याला सारखी असते त्या pH मूल्याला समविद्युत् भारबिंदू (विद्युत् भारांच्या दृष्टीने उदासीन अवस्था) असतो. या वेळी विद्रावात उभयधर्मी आयनाची (विद्युत् भारित अणू, रेणू व अणुगट यांची) संख्या जास्तीत जास्त असते तर धनविद्युत् भारित व ऋणविद्युत् भारित आयनांची संख्या कमी असते. समविद्युत् भारबिंदू हा विगमन-स्थिरांकावरून काढला जातो.
सर्वसामान्य तपमानास ॲमिनो अम्ले शुभ्र स्फटिक रूपात आढळतात. इतर कार्बनी संयुगांच्या मानाने त्यांचे वितळबिंदू उच्च आहेत. बहुतेक सर्व ॲमिनो अम्लांचे वितळबिंदूच्या आसपास अपघटन (घटक द्रव्ये सुटी
होणे) होते. सर्वसामान्यतः २००० से. वर त्यांचे वितळबिंदू आहेत.
ॲमिनो अम्ले चवीने गोड वा कडू किंवा काही चवहीनही असतात. पाण्याच्या साहाय्याने १,२००० से. ला प्रथिनांचे विच्छेदन केल्यास त्यांमधील घटक ॲमिनो अम्ले मुक्त होतात. मात्र या ट्रिप्टोफेन या अम्लाचा विनाश होतो.
त्रिमितीय संरचना : ग्लायसिनाखेरीज इतर सर्व नैसर्गिक ॲमिनो अम्लांत आल्फा कार्बन अणू हे असममितीचे (ज्याला चार वेगवेगळे अणू वा अणुगट जोडले आहेत असे) केंद्र असते, कारण हा कार्बन अणू चार भिन्न अणूंना अथवा गटांना जोडलेला असतो. त्यामुळे या अम्लांचे प्रत्येकी दोन प्रकाशीय समघटक [→समघटकता] संभवतात. त्यांपैकी एक दुसऱ्याचे आरशात पडलेले प्रतिबिंब होईल अशा तर्हेचे असते. एका रूपाच्या योगाने ध्रुवित प्रकाशाच्या प्रतलाचे वलन घड्याळाचे काटे फिरतात त्याप्रमाणे (अनुघटी) व दुसऱ्याने तितकेच परंतु विरुद्ध दिशेने (प्रतिघटी) होते.
अनुघटी वलन असणाऱ्या संयुगाला दक्षिणवलनी व प्रतिघटी वलन असणाऱ्यास वामवलनी असे म्हणतात व हे गुणधर्म दर्शविण्याकरिता दक्षिणवलनासाठी d अथवा (+) व वामवलनासाठी l किंवा (-) ही चिन्हे वापरतात. जसे (+) लॅक्टिक अम्ल किंवा d-लॅक्टिक अम्ल म्हणजे दक्षिणवलनी लॅक्टिक अम्ल प्रकार होय.
दक्षिणवलनी व वामवलनी (बिंब-प्रतिबिबंरूप) त्रिमितीय संरचना ज्या आकृतींनी दाखवितात त्यांना विन्यास (मांडणी) म्हणतात. हे परस्पर-सापेक्ष असतात. त्यांपैकी कोणत्याही एकास दक्षिणवलनी मानले (अथवा वामवलनी मानले), तर त्याचा प्रतिबिंबरूप विन्यास वामवलनी (अथवा दक्षिणवलनी) होईल.
रासायनिक पुरावा उपलब्ध असेल, तर या दोन विन्यासांपैकी कोणता विन्यास दक्षिणवलनी अथवा वामवलनी संयुगाचा आहे हे ठरविता येते. या तऱ्हेने निश्चित झालेल्या रूपांना त्या संयुगाचा ‘निरपेक्ष विन्यास’ म्हणतात. हे विन्यास D व L ही उपपदे संयुगाच्या नावापूर्वी लावून दर्शवितात. कोणत्या निरपेक्ष विन्यासास D व कोणत्या विन्यासास L हे उपपद लावावयाचे, याविषयी संकेत पुढीलप्रमाणे आहेत.
ज्या दक्षिण अथवा वामवलनी संयुगाचा विन्यास (१) मधील D-ग्लिसराल्डिहाइडाच्या विन्यासाशी जुळता आढळतो त्याचा निरपेक्ष विन्यास D हे उपपद लावून व (२) मधील L-ग्लिसराल्डिहाइडाच्या विन्यासाशी जमणारा असेल त्याला L हे उपपद लावून दर्शवितात.

(१) व (२) यांमधील विन्यासांशी तुलना करताना ह्या त्रिमितीय मांडणीचे प्रक्षेप (घनाकारी पदार्थाचे कागदाच्या पातळीत प्रमाणबद्ध चित्र) आहेत व त्यामध्ये असममित कार्बन अणू कागदाच्या प्रतलात असून CHO व CH2OH यांना जोडणारे बंध कागदाच्या प्रतलाखाली आणि H व OH यांना जोडणारे बंध कागदाच्या प्रतलावर आपणाकडे येत आहेत, अशा तऱ्हेने संयुग धरले आहे असे समजावयाचे.
एखाद्या संयुगाची या विन्यासांशी तुलना करताना त्यातील असममित कार्बन अणू अशा तऱ्हेने धरावा की, त्याला जोडलेल्या गटांपैकी सर्वांत अधिक ऑक्सिडीकरण [→ऑक्सिडीभवन] झालेला गट शिरोभागी व सर्वांत कमी ऑक्सिडीकरण झालेला गट तळभागी यावा व त्यांना जोडणारे बंध असममित कार्बन अणूच्या खालच्या प्रतलात जावे व राहिलेले दोन बंध प्रतलाच्या वर आपणाकडे यावे. अशा तऱ्हेने योजना केल्यावर OH गट (किंवा तत्सम गट) जर आपल्या उजव्या हातास आला, तर तो निरपेक्ष विन्यास दक्षिण होतो व तो D या उपपदाने दाखविला जातो. याच्या उलट OH (अथवा तत्सम गट) डाव्या हातास आला, तर तो विन्यास वाम किंवा L होय.
ॲमिनो अम्लांकरिता संदर्भ विन्यास OH ऐवजी NH2, CHO ऐवजी COOH हा गट व CH2OH ऐवजी उरलेला R हा गट वरील विन्यासात घातल्याने मिळतात.

निरपेक्ष विन्यास आणि प्रकाशीय वलन यांचा परस्परसंबंध जोडता येत नाही. दक्षिण विन्यास असलेले संयुग दक्षिणवलनी असेल किंवा वामवलनीही असेल.
प्रथिनांच्या जैव संश्लेषणात L-प्रतिबिंब रूपच लागते. काही सूक्ष्मजंतूंच्या कोशिकांच्या भित्तींमध्ये D-ॲलॅनीन व D-ग्लुटामिक अम्ल ही सापडतात. थ्रिओनीन, आयसोल्युसीन, हायड्रॉक्सीप्रोलीन, हायड्रॉक्सी-लायसीन आणि सिस्टीन ह्या ॲमिनो अम्लांत आल्फा कार्बन अणूच्या असममितीच्या केंद्राव्यतिरिक्त आणखी दुसरे असममित केंद्रही असते [→त्रिमितीय रसायनशास्त्र].
आयनी स्थिती : ॲमिनो अम्लातील कार्बॉक्सी गट व NH2 गट या दोहोंचे विगमन होते. कार्बॉक्सी गट विद्रावकाला एक प्रोटॉन देऊन धनायन (ऋणभारिंत परंतु धनाग्राकडे जाणारा) होतो, तर NH2 आयन गट विद्रावकापासून एक प्रोटॉन घेऊन ऋणायन (धनभारित परंतु ऋणाग्राकडे जाणारा आयन) बनतो.
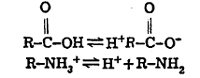
कार्बॉक्सी गटाचा विगमन स्थिरांक K1 व ॲमिनो गटाचा K2 या चिन्हांनी दर्शविले, तर त्यांचे अम्लता-स्थिरांक अनुक्रमे pK1 व pK2 हे पुढील समीकरणांवरून निश्चित करता येतात.
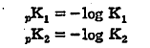
समविद्युत् भार बिंदूला ॲमिनो अम्ले द्विध्रुवी (धन व ऋण अशा दोन्ही रीतींनी भारित असलेल्या) आयन स्वरूपात आढळतात. तीव्र अम्ल विद्रावात ॲमिनो अम्लाचा रेणू ऋणायन बनतो, पण पुरेसा क्षारीय विद्राव मिसळला तर तोच धनायन स्वरूपात जातो.
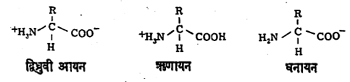
कार्बॉक्सी गटाचे अर्धे विगमन २ ते ३ pH मध्ये होते, तर ॲमिनो गटाचे अर्धे विगमन १० pH जवळ होते यावरून ॲमिनो अम्ले ही ४ ते ९ pH च्या दरम्यान द्विध्रुवीस्थितीत असतात.
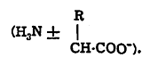
ॲमिनो अम्लांचे आयनीभवन होत असल्यामुळे त्यांची लवणे तयार करता येतात.
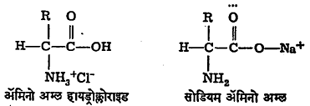
पृथक्करण व निश्चिती : ॲमिनो अम्लांची उपस्थिती, पुढे कोष्टक क्र. २ मध्ये दाखविल्याप्रमाणे, रासायनिक रंग-विक्रियांनी कळते. निनहायड्रिनाचा उपयोग ॲमिनो अम्लांची उपस्थिती व निश्चित प्रमाण काढण्यासाठी करतात.
१-फ्ल्यूरो-२, ४-डायनायट्रो बेंझिनामुळे ॲमिनो अम्लांचे ॲरिलीकरण होते व त्याचा प्रथिनांची रचना कशी आहे हे शोधण्यासाठी फार उपयोग होतो.
ॲमिनो अम्ले मुक्त स्वरूपात मिळविण्यासाठी प्रथिनाचे अम्लीय किंवा क्षारकीय विद्रावात जलीय विच्छेदन (पाण्याच्या विक्रियेने घटकद्रव्ये वेगळी करणे) करतात. जलीय विच्छेदनाने मिळालेल्या विद्रावापासून कोणतेही एखादे ॲमिनो अम्ल शुद्ध स्वरूपात वेगळे करता येते. ॲस्पार्टिक अम्ल वेगळे करताना त्या विद्रावात प्रथम कॅल्शियम हायड्रॉक्साइड अतिरिक्त (वाजवीपेक्षा जास्त) प्रमाणात टाकून कॅल्शियम ॲस्पार्टेट मिळवितात. त्यात अल्कोहॉल मिसळल्यावर ॲस्पार्टिक अम्लाचा अवक्षेप (साका) मिळतो. ॲमिनो अम्लांचे विश्लेषण (घटक ओळखणे व प्रमाण ठरविणे) आयन-विनियम वर्णलेखाने [→वर्णलेखन] फारच चांगले होते. ऋणायन-विनिमय करणारे सल्फोनेटेड पॉलिस्टायरीन-रेझीन हे आयन-विनिमयाच्या स्तंभात भरल्यावर ॲमिनो अम्लांच्या विद्रावाचे मिश्रण pH मूल्य तीन असताना त्याच्यावर ओततात. ऋणायनी ॲमिनो अम्ले स्तंभातील -SO3–Na+ यापासून सोडियम आयन दूर करतात आणि स्थिर विद्युत् प्रेरणेने ती स्तंभाशी बद्ध होतात. जी ॲमिनो अम्ले अधिक क्षारकीय असतात ती अधिक दृढतेने बद्ध होतात व जी अल्प क्षारकीय असतात ती शिथिलतेने बद्ध होतात. नंतर उभय-प्रतिरोधी (अम्ल व क्षारकाला विरोध करणाऱ्या) विद्रावाचे pH व आयनिक शक्ती क्रमशः व सावकाश वाढवून त्याने स्तंभ धुतात. यालाच ‘स्तंभ विकसित करणे’ असेही म्हणतात. या प्रक्रियेमुळे ॲमिनो अम्लांची लवण-बंधने (अम्ल व लवण यांना एकत्रित ठेवणारे बंध) ढिली होतात. अशा रीतीने स्तंभ विकसित करताना, अम्लधर्मी ॲमिनो अम्ले (ग्लुटामिक व ॲस्पार्टिक अम्ले) ही रेझिनापासून सहजगत्या प्रथम निराळी होतात. त्यानंतर उदासीन ॲमिनो अम्ले व शेवटी क्षारकीय ॲमिनो अम्ले वेगळी होतात.
ह्या पद्धतीने (रेझिनांचा उपयोग करून आणि पृष्ठशोषण व आयन-विनिमय घडवून) प्रथिनांतील सर्व ॲमिनो अम्लांचे पृथक्करण करता येते. ॲमिनो अम्ले जसजशी स्तंभापासून धुतली जातात तसतशी ती एका स्वयंचलित विभाजक (एकामागून एक घटक निराळा करणाऱ्या) संग्राहकामध्ये निरनिराळी संग्रहित केली जातात. ती वेगवेगळी मिळाल्यावर वैयक्तिक ॲमिनो अम्लाची निनहायड्रिनाबरोबर विक्रिया करून त्याला येणाऱ्या रंगाची तीव्रता मोजतात. ॲमिनो अम्लांचे असे पृथक्करण करणारी स्वयंचलित उपकरणे उपलब्ध आहेत.
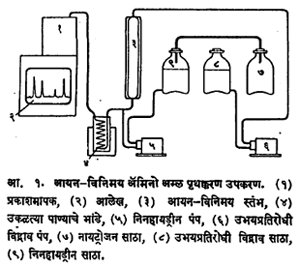
या उपकरणांत आयन-विनिमयाच्या स्तंभावर ॲमिनो अम्ले आपोआप वेगळी होऊन ती निरनिराळी मिळतात. त्यांच्यात निनहायड्रीन टाकले जाते व रंग तयार होण्याकरिता उष्णता दिली जाते. रंगाच्या तीव्रतेची नोंद होऊन ती आलेखित केली जाते. या सर्व प्रक्रिया त्या उपकरणाने क्रमवार होतात. वर्णलेखावरील विशिष्ट स्थानावरून कोणतेही अम्ल ओळखता येते आणि त्याचे परिमाणात्मक (वजनी प्रमाणाच्या दृष्टीने) मापन प्रत्येक वक्ररेषेच्या खाली येणाऱ्या जागेच्या क्षेत्रफळावरून करता येते.
वर्णलेखन : कागद-वर्णलेखन पद्धतीनेही ॲमिनो अम्लांचे पृथक्करण करतात. निरनिराळ्या ॲमिनो अम्लांच्या जीवज व जलयुक्त अवस्थेमधील पृथक्करण हे विभाजन गुणकातील फरकावर आधारित असते. वर्णलेख एकाच विद्रावाने विकसित केल्यास ॲमिनो अम्लांचे पृथक्करण स्पष्टपणे दिसून येत नाही, म्हणून द्विमितीय (दोन दिशांनी दाखविणाऱ्या) वर्णलेखनाचा उपयोग करतात. या पद्धतीत प्रथम एका विद्रावाने वर्णलेख विकसित करतात व मग ९० अंशाने वर्णलेख फिरवून दूसऱ्या विद्रावकाने तो विकसित करतात. नमुन्यादाखल एक द्विमितीय वर्णलेख आ. २ मध्ये दाखविलेला आहे.
वर्णलेखावर निनहायड्रिनाचा फवारा मारल्याने प्रत्येक ॲमिनो अम्लाची उपस्थिती जांभळ्या ठिपक्यांवरून निश्चित कळते. हे ठिपके असलेला लेखाचा भाग कापून व तो धुवून मिळालेल्या विद्रावाच्या रंगाच्या तीव्रतेवरून ॲमिनो अम्लाचे प्रमाण निश्चित करतात.
प्रत्येक ॲमिनो अम्लावर विशिष्ट pH ला ठराविक विद्युत् वर्चस् (विद्युत् स्थिती) असते व निरनिराळ्या pH ला निरनिराळे वर्चस् असते. या विद्युत् वर्चसांच्या फरकाचा उपयोग करून ॲमिनो अम्लांचे विद्युत् स्थानांतर करता येते. अम्ले वेगवेगळी केली जाऊन त्यांचे मापनही करता येते.
ॲमिनो अम्लांचे मापन व्हॅन-स्लाइक पद्धतीनेही करतात. यात ॲमिनो अम्लाचा ॲमिनोगट व नायट्रस अम्ल यांची विक्रिया होऊन नायट्रोजन वायू मिळतो. त्याच्या घनफळावरून ॲमिनो अम्लाचे प्रमाण कळते. सूक्ष्मजीवशास्त्रीय मापन हे सर्व साध्या ॲमिनो अम्लांकरिता उपयोगी पडते. एखाद्या सूक्ष्मजीवाच्या वाढीसाठी विशिष्ट अम्लाची आवश्यकता असते. या प्रकृतिगुणाचा उपयोग त्या ॲमिनो अम्लाच्या मापनासाठी करतात. ॲमिनो अम्लाच्या मापनासाठी तो सूक्ष्मजीव ॲमिनो अम्लविरहित निर्जंतुक माध्यमात सोडतात. नंतर मोजावयाच्या पदार्थाचा ज्ञात भाग त्यात मिसळतात. सूक्ष्मजीवाच्या वाढीवरून ॲमिनो अम्लाचे प्रमाण कळते.
काही एंझाइमे (सजीवांमध्ये रासायनिक विक्रिया घडवून आणण्यास मदत करणारे प्रथिनयुक्त पदार्थ) एखाद्या विशिष्ट ॲमिनो अम्लाचाच कार्बॉक्सिल निरास करतात (कार्बॉक्सिल गट काढून टाकतात). कार्बन डाय-ऑक्साइडाच्या घनफळावरून त्या अम्लाचे मिश्रणातील प्रमाण ठरविता येते. समस्थानिकी (तोच

अणुक्रमांक पण भिन्न अणुभार असलेल्या त्याच मूलद्रव्याच्या प्रकाराच्या) विरलीकरण पद्धतीनेही एखाद्या मिश्रणातील ॲमिनो अम्लाचे प्रमाण ठरविता येते.
ॲमिनो अम्लाचा चयापचय : कोशिकांतील ॲमिनो अम्लांची संहती ही त्यांच्या भित्तीबाहेरील विद्रावातील संहतीपेक्षा अधिक असते. याचा अर्थ असा की, ॲमिनो अम्लांचे कमी संहती असलेल्या विद्रावातून अधिक संहतीच्या विद्रावात स्थलांतर होत असते आणि असे स्थलांतर होण्यासाठी ऊर्जेची आवश्यकता असते. या प्रक्रियेस ‘कार्यप्रवण स्थलांतर’ म्हणतात. अशा रीतीने कोशिकांतील ॲमिनो अम्लांची संहती त्यांच्या भित्तिबाह्य विद्रावातील संहतीपेक्षा सहस्रपटीने वाढू शकते. कोशिकांतील एंझाइमसदृश प्रवेशक (शिरणाऱ्या) द्रव्यांमुळे हे कार्यप्रवण स्थलांतर घडून येते.
जैव संश्लेषण : प्रथिनांचे घटक असलेल्या ॲमिनो अम्लांचे संश्लेषण करण्याची कार्यक्षमता निरनिराळ्या जीवांची कमीअधिक असते. बुहतेक सर्व सूक्ष्मजंतू आणि वनस्पती असे संश्लेषण करण्याच्या कार्यात कार्यक्षम असतात, परंतु त्यांच्या मानाने पुष्कळशा प्राण्यांची कार्यक्षमता मात्र जवळ जवळ निम्म्याइतकी असते. म्हणून अशा प्राण्यांचा विचार करताना ॲमिनो अम्लांचे ‘आवश्यक’ व ‘अनावश्यक’ असे वर्ग करतात. ज्या आवश्यक अम्लांचा योग्य पुरवठा करण्यास शरीर असमर्थ असते ती अन्नातून पुरवावी लागतात. इष्ट वाढ किंवा नायट्रोजनाचा समतोल (इष्ट तितकेच प्रमाण) राखण्याकरिता ज्या ॲमिनो अम्लाचा आहारात समावेश करणे अवश्य असेल, त्या ॲमिनो अम्लास ‘आवश्यक’ असे म्हणतात. एखाद्या प्राण्याचे दररोजचे नायट्रोजनाचे ग्रहण व उत्सर्जन ही सारख्याच प्रमाणात असली म्हणजे तो नायट्रोजनाच्या बाबतीत संतुलित असतो. ल्युसीन, आयसोल्युसीन, व्हॅलीन, लायसीन, मिथिओनीन, फिनिल ॲलॅनीन, ट्रिप्टोफेन, थ्रिओनीन, हिस्टिडीन व आर्जिनीन ही पांढऱ्या उंदरास आवश्यक अशी ॲमिनो अम्ले आहेत. यांतील पहिली आठ ही सर्व उच्च प्राण्यांनाही आवश्यक असतात. एखाद्या ॲमिनो अम्लाची आहारातील आवश्यकता अनेक बाबींवर अवलंबून असते. अन्नात उपापचयाशी संबंधित असलेले ॲमिनो अम्ल टायरोसीन असले म्हणजे फिनिल ॲलॅनिनाची आवश्यकता तितकीच राहत नाही. तसेच ग्लुटामिक अम्ल व आर्जिनीन यांच्या बाबतीतही होते. त्याचप्रमाणे ॲमिनो अम्लांची आवश्यकता गरोदरपण, अंगावर पाजणे, रोग इ. प्राण्यांच्या स्थितींवर अवलंबून असते. बहुधा सर्व प्राण्यांच्या कोशिकांत चयापचयाचे मार्ग सारखेच असतात. लायसीन मात्र याला अपवाद आहे. सूक्ष्मजंतूंमध्ये त्याचे संश्लेषण ॲस्पार्टिक अम्लापासून डाय-ॲमिनो पिमेलिक अम्लाद्वारा होते. तर बुरशीमध्ये ॲस्पार्टिक अम्लाचा आरंभ आल्फा-कीटो-ग्लुटामिक अम्लापासून होतो.
ॲमिनो गटाची घडण व स्थलांतरण : जैव नायट्रोजनाचा ॲमिनो अम्लांच्या ॲमिनो गटात पुढीलप्रमाणे प्रवेश होतो. ग्लुटामिक अम्ल डी- हायड्रोजीनेज ह्या एंझाइमामुळे आल्फा-कीटो-ग्लुटारिक अम्लाचे क्षपणात्मक ॲमिनीकरण होऊन ग्लुटामिक अम्लात रूपांतर होते. इतर सर्व ॲमिनो अम्ले ही ॲमिनो संक्रमण किंवा ॲमिनो अम्लात फेरफार घडून येऊन तयार होतात. पहिल्याचे उदाहरण म्हणजे ग्लुटामिक अम्लातील ॲमिनो गटाचे आल्फा-कीटो-आयसो-कॅप्रॉइक अम्लात ॲमिनो संक्रमण (रूपांतर) होऊन व्हॅलिनाची निर्मिती. दुसऱ्या प्रकारचे उदाहरण म्हणजे ग्लुटामिक अम्लाचे ⇨ क्षपण व वलयीभवन होऊन (वलयात मांडणी होऊन) ‘प्रोलीन’ तयार होणे. पायरूव्हिक अम्लाचे क्षपणासह ॲमिनीकरण होऊन तयार होणारे ॲलॅनीन व फ्युमॅरिक अम्लात अमोनिया घालून ॲस्पार्टिक अम्ल तयार होणे ही अजैव नायट्रोजनाचे ॲमिनो अम्लातील नायट्रोजनामध्ये रूपांतर होण्याची उदाहरणे होत.
केव्हा केव्हा एंझाइमांमुळे होणाऱ्या विक्रियांत त्यांना साहाय्य करणाऱ्या आणखी एखाद्या को-एंझाइमाची आवश्यकता असते.
ट्रॅन्स-ॲमिनेजला पिरिडॉक्सल फॉस्फेट हे पुढील रीतीने मदत करते. ॲमिनो अम्लातील ॲमिनो गट पिरिडॉक्सल फॉस्फेट घेतो व त्याचे कीटो-अम्लात रूपांतर करतो व त्याचे स्वतःचे पिरिडॉक्समीन फॉस्फेटात रूपांतर होते. पिरिडॉक्समिनाचा ॲमिनो गट दुसऱ्या एखाद्या ॲमिनो गट घेऊ शकणाऱ्या कीटो-अम्लाला मिळू शकतो व त्यामुळे नवीन ॲमिनो अम्ल तयार होऊन पिरिडॉक्सल फॉस्फेट पुन्हा मिळते.
आर्जिनीन व ॲडेनिलिक अम्लांच्या संश्लेषणात ॲमिनो गटाचे संक्रमण निराळ्या प्रकारे होते. या ठिकाणी ॲस्पार्टिक अम्ल हे कीटो गटास जोडले जाते व स्थिर मध्यसंयुग (मधल्या टप्प्यात तयार होणारे संयुग) तयार होते. त्या संयुगाचे दुसऱ्या एंझाइमामुळे विघटन होऊन फ्युमॅरिक अम्ल व आर्जिनीन ही तयार होतात.
ॲस्पार्टेट हे फ्युमॅरेटाच्या ॲमिनीकरणामुळेही मिळते. अमोनिया हा ग्लुटामिनामधील अमाइडाच्या द्वारा कार्बनी संयुगात प्रवेश मिळवितो.
अधःपतन : प्राण्यांच्या, वनस्पतींच्या व सूक्ष्मजीवांच्या कोशिकांतील ॲमिनो अम्लांचे अधःपतन (ऱ्हास) होऊन कार्बन डाय-ऑक्साइड, अमोनिया व पाणी ही तयार होतात.
ॲमिनोनिरास : ॲमिनो गट काढून टाकणे ही ॲमिनो अम्लाच्या विघटनातील पहिली पायरी होय. ऑक्सिडीकरणाने ॲमिनोनिरास होताना एकाच वेळी दोन हायड्रोजन अणूंचा निरास होतो व नंतरच्या जलीय विच्छेदनाने कीटो-अम्ल तयार होते.
ग्लुटामिक अम्ल आणि ॲलॅनीन डी-हायड्रोजीनेज ह्या एंझाइमाच्या उपस्थितीत पिरिडीन न्यूक्लिओटाइड या को-एंझाइमास हायड्रोजनाचे अणू जोडले जातात व त्यामुळे ॲमिनो संक्रमण होते. D व L ॲमिनो अम्लांच्या ऑक्सिडेजांच्या उपस्थितीत हायड्रोजन अणू फ्लाविन या को-एंझाइमाकडे जातात व ऑक्सिजनाचे क्षपण होऊन हायड्रोजन पेरॉक्साइड तयार होते. त्या पेरॉक्साइडाचा निरास जर कॅटॅलेज या एंझाइमामुळे झाला नाही, तर त्याच्यामुळे त्या आल्फा-कीटो-अम्लाचे ऑक्सिडीकरण होऊन एक कार्बन कमी असलेले समभागी (सारखे प्रमाण असणारे) अम्ल तयार होते.
ॲमिनोनिरास हा क्षपणकारक व अन-ऑक्सिडीकारकही असतो. हायड्रॉक्सिल किंवा सल्फहायड्रिल गट असलेल्या अम्लातून पाण्याचा व हायड्रोजन सल्फाइडाचा रेणू मुक्त झाल्यावर त्या अम्लाचे दुसऱ्या ॲमिनो अम्लात रूपांतर होते व शेवटी जलीय विच्छेदनाने कीटो-अम्ल मिळते. याच प्रकारे सेरीन, थ्रिओनीन, होमोसेरीन, सिस्टाइन व होमोसिस्टाइन यांचा ॲमिनोनिरास होतो.
अवायुजीवी (हवेच्या सान्निध्यात न वाढणाऱ्या) सूक्ष्मजीवातील क्षपणात्मक ॲमिनोनिरास पुढे दाखविल्याप्रमाणे घडून येतो :
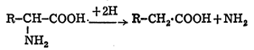
या विक्रियेत दुसऱ्या एखाद्या ॲमिनो अम्लाच्या रेणूचे ऑक्सिडीकरण होऊन दोन हायड्रोजन अणू मिळतात. शिवाय वायुरूप हायड्रोजनदेखील अशा सूक्ष्मजीवांना चालतो. ॲमिनोनिरास होण्यापूर्वी कित्येक ॲमिनो अम्लांच्या कार्बनी शृंखलेत फरक होतो. उदा., ट्रिप्टोफेनाचे इंडॉल व सेरिनात रूपांतर होते व नंतर सेरिनाचा ॲमिनोनिरास होतो. अशा ॲमिनोनिरासामुळे कीटो-अम्ले मिळतात. व त्या कीटो-अम्लांचे ऑक्सिडीकरण होऊन शेवटी कार्बन डाय-ऑक्साइड व पाणी तयार होते. ॲमिनो अम्लांच्या अधःपतनाने होणारे पदार्थ हे कार्बाहायड्रेटांच्या व स्निग्ध पदार्थांच्या चयापचयाच्या अधःपतनाने होणाऱ्या पदार्थांसारखे असतात. उदा., पायरूव्हेट, आल्फा-कीटो ग्लुटारेट किंवा ॲसिटिल को-एंझाएम-ए हे तयार होतात [→कार्बोहायड्रेटे].
कार्बॉक्सिलनिरास : ॲमिनो अम्ल-डी कार्बॉक्सिलेजे ही एंझाइमे सर्व सूक्ष्मजीवांत आढळतात व ती विशेषतः L-ॲमिनो अम्लांचा आल्फा-डी-कार्बॉक्सिलनिरास घडवून आणण्यात उत्प्रेरकाचे कार्य करतात. प्रथिनाच्या विघटनात अशी विक्रिया घडून येत असताना दुर्गंधी अमाइने मिळतात. ऑर्निथिनाच्या कार्बॉक्सिलनिरासाने प्युट्रेसीन हे दुर्गंधी द्रव्य उत्पन्न होते. अमाइन-ऑक्सिडेज एंझाइमामुळे अमाइनाचे आल्डिहाइडात व अमोनियात पुढे दाखविल्याप्रमाणे विघटन होते :
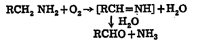
हिस्टिडिनाच्या कार्बॉक्सिलनिरासाने हिस्टामीन मिळते.
रॅसेमीकरण : ॲलॅनीन, मिथिओनीन, ग्लुटामीन, प्रोलीन, लायसीन आणि सेरीन यांचे रॅसेमीकरण (रॅसेमिक ॲमिनो अम्लात रूपांतर होणे) उत्प्रेरणाने (विक्रियेत भाग न घेता विक्रियेची गती वाढविण्याच्या क्रियेने) घडविणारी एंझाइमे आणि हायड्रॉक्सीप्रोलीन व डाय-ॲमिनो पिमेलेटाचे अपिभाजन करणारी (H आणि OH यांच्या कार्बन अणूभोवतील स्थितीत अदलाबदल करून समघटक तयार करणारी) निरनिराळी एंझाइमे सूक्ष्मजीवांत असतात, असे कळून आलेले आहे. L-लायसिनाच्या जैव संश्लेषणात डाय-ॲमिनो व ॲलॅनीन यांचे चयापचयन L-समघटकाने न होता D-समघटकाने होते.
संयोगीकरण : ॲमिनो अम्लांचे संयोगीकरण होऊन पेप्टाइड निर्माण होण्यासाठी ॲमिनो अम्लांना ऊर्जा देऊन त्यांना कार्यप्रवण करावे लागते. ॲमिनो अम्ल व ॲडिनोसीन ५ ट्रायफॉस्फेट (एटीपी) हे को-एंझाइम यांची विक्रिया घडून येऊन एंझाइमाच्या कार्यामुळे ॲडेनिलिक अम्लाचा कार्बॉक्सिल गटाबरोबर संयोग होतो व ॲमिनो अम्लात शक्तिमान बंध तयार होतो. अशा न्यूक्लिओटाइडाशी [ → न्यूक्लिइक अम्ले] जोडलेल्या ॲमिनो अम्लांची एकमेकांबरोबर विक्रिया होऊन पेप्टाइडे तयार होतात. ती प्रथिनांच्या संश्लेषणातील मध्यस्थ होत.
संयोगीकरणातील दुसरी महत्त्वाची गोष्ट म्हणजे सजीव कोशिकेत अशी यंत्रणा असावी लागते की, जिच्यामुळे ॲमिनो अम्ले एकमेकांशी ठराविक अनुक्रमाने जोडली जातील. प्रथिनांची विशिष्ट सक्रियता ही त्यांच्या मालेतील ॲमिनो अम्लांच्या अनुक्रमावर अवलंबून असते. त्या अनुक्रमास अनुसरून त्या मालेच्या ठराविक नमुन्याच्या अनेक आवृत्ती काढावयाच्या असतात व त्यासाठी न्यूक्लिइक अम्लाची आवश्यकता असते. न्यूक्लिइक अम्ल हे गुणसूत्रे (आनुवांशिक लक्षणे एका पिढीतून दुसऱ्या पिढीत नेणारे कोशिकांमधील घटक) व जनुके (आनुवंशिक लक्षणे निदर्शित करणारी गुणसूत्रांवरील एकके, →जीन) यांचे आवश्यक घटक असते. ह्या अम्लाचा रेणू तयार करण्यासाठी चार निरनिराळ्या प्रकारच्या न्यूक्लिओटाइडांची आवश्यकता असते. ती न्यूक्लिओटाइडे काही विशिष्ट क्रमाने मालेत असतात व त्या विशिष्ट क्रमाला ‘रासायनिक संहिता’ म्हणतात. एका जनुकाची दोन जनुके होताना मूळची संहिता तशीच राहत असते व त्या संहितेवरून प्रथिनांत असणाऱ्या ॲमिनो अम्लांच्या अवशेषांच्या अनुक्रमाबद्दल माहिती मिळते [→न्यूक्लिइक अम्ले].
ब–६ जीवनसत्त्व आणि ॲमिनो अम्ले : ज्या एंझाइमांची ॲमिनो अम्लाबरोबर प्रत्यक्ष विक्रिया होते त्यांना को-एंझाइम म्हणून ब-६ हे जीवनसत्त्व लागते [→ जीवनसत्त्व ब६]. हे जीवनसत्त्व निरनिराळ्या रुपांत आढळते, पण त्यांपैकी पिरिडॉक्सल फॉस्फेटच को-एंझाइमाचे कार्य करते. या संक्रमणाच्या विक्रियेत ॲमिनो गटाचा व्युत्क्रम पिरिडॉक्समीन फॉस्फेटाच्याकडून होतो. बहुसंयुजी धातू (निरनिराळ्या प्रमाणात संयोग पावणार्या धातू, →संयुजा) व ॲमिनो अम्लांच्याबरोबर संयोग करून एक विशिष्ट प्रकारचा ‘शिफ-क्षारक’ करण्याची क्षमता
पिरिडॉक्सल फॉस्फेटामध्ये असल्यामुळेच ॲमिनो संक्रमण, कार्बॉक्सिलनिरास, रॅसेमीकरण, हायड्रोजननिरास ह्या विक्रिया घडू शकतात.
ॲमिनो अम्लांचे पोषणातील स्थान : जे जीव सर्वच ॲमिनो अम्लांचे संश्लेषण करू शकतात त्यांच्या आहारात ॲमिनो अम्ले असण्याची आवश्यकता नसते पण ज्या जीवात संश्लेषण होण्याची कोणतीच यंत्रणा नसते, त्यांच्या आहारात सर्व ॲमिनो अम्ले असावीच लागतात. सस्तन प्राण्यांना ८-१० आवश्यक ॲमिनो अम्ले लागतात, तर बहुतेक वनस्पती त्यांना आवश्यक असणाऱ्या ॲमिनो अम्लांचे संश्लेषण स्वतः करतात.
जीवसृष्टीच्या प्रारंभीच्या आदिम (अगदी पहिल्या) जीवांना आवश्यक असलेली ॲमिनो अम्ले त्यांच्या शरीरांत तयार होत असावीत. परंतु क्रमविकासाच्या (उत्क्रांतीच्या) पुढील टप्प्यांत ‘जीवो जीवस्य जीवनम्’ या न्यायाने काही जीव इतरांना खाऊन निर्वाह करू लागल्यावर ॲमिनो अम्लांचा पुरवठा होणे शक्य झाले. तेव्हापासून निर्वाह व योग्य रीतीने वाढ होण्यासाठी जीवांना ॲमिनो अम्लांचा पुरवठा संतुलित प्रमाणात होण्याची आवश्यकता निर्माण झाली.
पहा : ॲलॅनीन ॲस्परजिन ॲस्पार्टिक अम्ल आयसोल्युसीन आर्जिनीन ग्लायसीन ग्लुटामिक अम्ल टायरोसीन ट्रिप्टोफेन थ्रिओनीन प्रथिने प्रोलीन फिनिल ॲलॅनीन मिथिओनीन लायसीन ल्युसीन व्हॅलीन सिस्टाइन सिस्टीन सेरीन हिस्टिडीन.
संदर्भ : 1. Block, R. J. Weiss, K. W. Amino Acid Handbook, Springfield, 1956.
2. Fairley, J. L. Kilgour, G. L. Essentials of Biological Chemistry, New York, 1968.
3. Mahler, H. R. Cordes, E. A. Biological Chemistry, London, 1968.
4. Meister, A. Biochemistry of the Amino Acids, New York, 1957.
शिगटे, रा. धों. केळकर, गो. रा.
“