पाणी : सर्वांच्या परिचयाचा एक सामान्य द्रव पदार्थ. पाणी हे मूलद्रव्य आहे असे पूर्वी समजले जात असे परंतु १७८१ मध्ये हेन्री कॅव्हेंडिश यांनी ज्यात हायड्रोजन व ऑक्सिजन यांच्या घनफळाचे प्रमाण २ : १ आहे अशा मिश्रणात विजेची ठिणगी पाडली, तर पाणी बनते, असे दाखविले. त्यानंतर डब्ल्यू. निकल्सन आणि ए. कार्लाइल यांनी विद्युत् प्रवाहाने पाण्याचे विच्छेदन (रेणूचे तुकडे करणे) केले तेव्हा हेच वायू याच प्रमाणात निर्माण होतात असे त्यांना दिसून आले. या प्रयोगावरून पाणी हे मूलद्रव्य नसून ते हायड्रोजन व ऑक्सिजन यांपासून बनलेले संयुग आहे, हे सिद्ध झाले. याचे रेणुसूत्र (रेणूमध्ये असणाऱ्या अणूंचे प्रकार व त्यांची संख्या दर्शविणारे सूत्र) H2O आहे, हे १८६७ मध्ये निश्चित करण्यात आले.
उपस्थिती व कार्य: पृथ्वीवरील जीवांची उत्पत्ती पाण्यात झाली व त्यामुळे ते जीवोत्त्पत्तीच्या काळाच्या पूर्वीपासून अस्तित्वात आहे, असे निश्चितपणे म्हणता येते. पृथ्वीच्या पृष्ठभागाचा जवळजवळ ३/४ भाग त्याने व्यापिलेला आहे.
प्राणी व वनस्पती यांमध्ये पाणी हा एक महत्त्वाचा घटक आहे. मानवी शरीरात सु. ७०%, जमिनीवरील वनस्पतींत ५०–७५% आणि पाण्यातील वनस्पतींत ९५ ते ९९% पाणी असते. काही खनिज पदार्थांमध्ये पाणी संयोगित अवस्थेत असते [⟶ जलसंयोग].
पृथ्वीवर समुद्र, नद्या, ओढे, सरोवरे, झरे, विहिरी इ. रूपाने पाणी आढळते. कित्येक ठिकाणी जमिनीखाली पाणी अस्तित्वात आहे, पण फार खोल असल्यामुळे ते बाहेर काढणे परवडत नाही [⟶ भूमिजल]. घनरूप पाणी उत्तर व दक्षिण ध्रुवांकडील सतत हिमाच्छादित असलेल्या प्रदेशांत, शीत कटिबंधात व इतरत्र उंच पर्वतराजींवर आढळते. गारा पडतात आणि हिमवर्षाव होतो तेव्हाही त्याचे अस्तित्व प्रत्ययास येते. बाष्परूप पाणी वातावरणात कमी-जास्त प्रमाणात नेहमीच असते.
सूर्याच्या उष्णतेने समुद्र व इतर जलाशय यांच्या पाण्याची वाफ बनते आणि ती वातावरणात शिरून तिचे ढग बनतात. ढगांपासून पावसाच्या, हिमाच्या किंवा गारांच्या रूपाने पाणी परत पृथ्वीस मिळते. असे जलावर्तन किंवा जलस्थित्यंतरचक्र अव्याहत चालू असते [⟶ जलविज्ञान].
पावसाचे पाणी ओहोळांच्या किंवा नदीनाल्यांच्या रूपाने जमिनीवरून वाहते तेव्हा अनेक भूवैज्ञानिक घडामोडी होतात. खडक झिजतात, त्यांतील विद्राव्य (विरघळणारी) लवणे पाण्याबरोबर निघून जातात, खडकांचे तुकडे व माती वाहून जाते आणि गाळाच्या रूपाने इतरत्र निक्षेपित होते (साचते). खडकांच्या भेगांत साठलेले पाणी गोठले म्हणजे ते प्रसरण पावते व त्यामुळे खडक फुटतात. जमिनीवरील लवणे अखेरीस समुद्रात जाऊन साठतात. समुद्रात विद्राव्य लवणांचे प्रमाणु सु. ३·५% असते. ज्या ठिकाणी बाष्पीभवन कमी व साठणारे पाणी जास्त असते अशा ठिकाणी उदा., बाल्टिक समुद्रात, हे प्रमाण कमी असते. याच्या उलट मृत समुद्रात बाष्पीभवन जास्त आणि पाणीपुरवठा कमी असल्यामुळे हे प्रमाण उच्च सु. २२·८% असते.
नागरी जीवनासाठी लागणारे पाणी नद्या, सरोवरे किंवा विहिरी यांपासून मिळते. त्यामध्ये विरघळलेले किंवा संधारित असलेले (लोंबकळत्या स्थितीत असलेले) अनिष्ट पदार्थ असतील, तर त्यावर आवश्यक ते संस्कार करून यथायोग्य करून घ्यावे लागते [⟶ पाणीपुरवठा].
भौतिक गुणधर्म: शुद्ध पाणी रुचिहीन व गंधहीन असते. पाण्याचा पातळ थर वर्णहीन असतो परंतु त्याच्या जाड (२ मी. पेक्षा जास्त) थरातून आरपार पाहिले, तर ते निळसर दिसते. थंड करू लागल्यास ४° से. तापमान येईपर्यंत पाणी आकुंचन पावते. तापमान त्याच्या खाली जाऊ लागले म्हणजे ते प्रसरण पावू लागते व ०° से. तापमानास गोठते. पाण्याच्या या गुणधर्माला पाण्याचे असंगत प्रसरण असे म्हणतात. ४° से. तापमान असलेले पाणी इतर तापमानाच्या पाण्यापेक्षा जड असते म्हणजे त्याची घनता या तापमानाला सर्वांत अधिक असते. या तापमानाच्या १ घ. सेंमी. पाण्याचे वजन हे प्रमाणित १ ग्रॅम वजन मानण्यात आले आहे.
पाण्याचा हा एक विशेष गुण असून त्याला निसर्गात फार महत्त्व आहे. एखाद्या जलाशयाचे पाणी थंड होऊन त्याचे तापमान ४° से. च्या खाली जाऊ लागते तसतसे कमी तापमानाचे पाणी हलके असल्यामुळे पृष्ठभागावर येते व गोठते तेव्हा त्याचा थर पृष्ठभागावर पसरतो. त्याखाली पाणी द्रवरूपच राहते म्हणजे संपूर्ण जलाशय गोठू शकत नाही व त्यामुळे त्यात जलचर प्राणी जिवंत राहू शकतात.
पाणी तापविले असता समुद्रसपाटीला, म्हणजेच वातावरण दाब ७६० मिमी. असताना, ज्या तापमानास उकळते ते तापमान हा सेल्सिअस तापक्रमाचा (तापमान मापक्रमाचा) १०० वा बिंदू (१००° से.) आणि ज्या तापमानास पाणी गोठते तो प्रारंभ बिंदू (०° से.) असे मानण्यात आले आहे [⟶ तापमापन]. समुद्रसपाटीपासून जो जो वर जावे तो तो वातावरण दाब कमी होतो व पाण्याचा उकळबिंदूही १००° से. पेक्षा कमी होतो. याच्या उलट दाब वाढविला, तर पाण्याचा उकळबिंदू चढतो. या गुणधर्माचा उपयोग उच्च तापमान मिळविण्यासाठी केला जातो. नित्याच्या व्यवहारातील दाबपात्रामध्ये (प्रेशर कुकरमध्ये) पाण्याचे तापमान सु. १२०° से. इतके उच्च जाते व त्यामुळे अन्न लवकर शिजते.
पाण्याची विशिष्ट उष्णता (१ ग्रॅम पाण्याचे तापमान १° से.ने वाढविण्यासाठी लागणारी उष्णता) हे उष्णतामापनाचे एकक आहे. तिचे मूल्य् प्रारंभीच्या व अंतिम तापमानबिंदूप्रमाणे थोडेफार बदलते म्हणून १ ग्रॅम पाण्याचे तापमान १४·५° से. पासून १५·५° से. इतके करण्यास लागणारी उष्णता ही प्रमाण मानली जाते. तिला कॅलरी, ग्रॅम कॅलरी किंवा लहान कॅलरी म्हणतात. १ ग्रॅम पाण्याचे तापमान ०° से. पासून १००° से. पर्यंत चढविण्यास लागणाऱ्या उष्णतेच्या १/१०० भागास माध्य (सरासरी) कॅलरी म्हणतात. लहान कॅलरीला १,००० ने गुणले असता येणाऱ्या मूल्यास किलो कॅलरी किंवा मोठी कॅलरी असे म्हणतात. उष्णता ही एक प्रकारची ऊर्जांच असल्यामुळे तिचे मूल्य अलीकडे ऊर्जेच्या एककात म्हणजे जूलमध्ये व्यक्त करतात. १ लहान कॅलरी म्हणजे ४·१८५ जूल होत.
पाण्याची विशिष्ट उष्णता सर्व पदार्थांच्या विशिष्ट उष्णतेपेक्षा जास्त आहे. त्यामुळे पाणी सावकाश तापते व सावकाश थंड होते आणि वातावरणाच्या तापमानाचे नियंत्रण होते.
वाफेत रूपांतर होण्यासाठी १ ग्रॅम पाण्याला ५३९·५ कॅलरी उष्णता लागते, तिला पाण्याची बाष्पीभवनाची सुप्त उष्णता म्हणतात. वाफ थंड केली असता तिचे पाणी बनते तेव्हा ही सुप्त उष्णता बाहेर पडते. तिचाच उपयोग हवी असेल त्या ठिकाणी सोयीस्करपणे उष्णता उत्पन्न करण्यासाठी केला जातो.
०° से. तापमानाच्या पाण्याचे बर्फ होण्यासाठी उष्णता काढून घ्यावी लागते. १ ग्रॅम पाण्याचे बर्फ होते तेव्हा ७९·६७ कॅलरी उष्णता बाहेर पडते. उलटपक्षी १ ग्रॅम बर्फाचे जेव्हा ०° से. तापमानाचे पाणी होते तेव्हा ७९·६७ कॅलरी उष्णता शोषण केली जाते. या मूल्याला पाण्याची द्रवीभवनाची (वितळण्याची अथवा गोठण्याची) सुप्त उष्णता म्हणतात. बर्फाच्या योगाने वस्तू थंड करताना या गुणाचाच आपण उपयोग करून घेतो.
पाण्यातून विद्युत् प्रवाहाचे संवहन फार मंदपणे होते. पाणी हा उत्तम विद्रावक असून त्यात अनेक विरघळतात. विद्युत् संयोजी (ज्यांमधील रासायनिक संयोग घटक अणूंच्या इलेक्ट्रॉनांच्या आपापसात झालेल्या देवघेवीमुळे घडलेला असतो अशी संयुगे उदा., खनिज अम्ले, क्षारके, लवणे इ.) संयुगे यात विरघळविली असता त्यांचे आयनीभवन (घटक अणू विद्युत् भारित रूपात सुटे होणे) होते व त्यामुळे त्यांचे विद्राव विद्युत् संवाहक बनतात.
पाण्याचा ⇨ पृष्ठताण २०° से. तापमानास ०·०७२७ न्यूटन/मी. आहे.
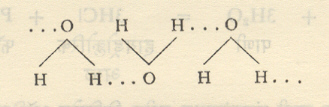 पाण्याचा उकळबिंदू, पृष्ठताण, बाष्पीभवन उष्णता यांची मूल्ये समरूप संघटनेच्या द्रवांशी तुलना करता उच्च आहेत. त्याचप्रमाणे घनरूप होताना प्रसरण पावणे, विरघळलेल्या लवणांचे आयन बनविणे इ. पाण्याचे गुणधर्मही सामान्य द्रव पदार्थांपेक्षा वेगळे आहेत. पाण्याच्या विशेषत्वाचे कारण पाणी हे एक संगमित (ज्याचे रेणू एकमेकांमधील आकर्षणामुळे साहचर्यात राहतात असे) संयुग आहे. याचे कारण ऑक्सिजन अणू ऋण विद्युती (इलेक्ट्रॉनांना आपणाकडे ओढणारे) असल्यामुळे ते समाईक इलेक्ट्रॉनांना आपल्याकडे जास्त खेचून घेतात. त्यामुळे हायड्रोजन अणूंवर किंचित धन विद्युत् भार येऊन ते पाण्याच्या दुसऱ्या रेणूतील ऑक्सिजनाकडे आकर्षिले जातात आणि त्यामध्ये एक प्रकारचा बंध निर्माण होतो. त्याला हायड्रोजन बंध म्हणतात. अशा प्रकारे पाण्याचे २ अथवा ३ रेणू संगमित अवस्थेत पाण्याच्या साध्या रेणूबरोबर समतोलावस्थेत पाण्यात अस्तित्वात असतात.
पाण्याचा उकळबिंदू, पृष्ठताण, बाष्पीभवन उष्णता यांची मूल्ये समरूप संघटनेच्या द्रवांशी तुलना करता उच्च आहेत. त्याचप्रमाणे घनरूप होताना प्रसरण पावणे, विरघळलेल्या लवणांचे आयन बनविणे इ. पाण्याचे गुणधर्मही सामान्य द्रव पदार्थांपेक्षा वेगळे आहेत. पाण्याच्या विशेषत्वाचे कारण पाणी हे एक संगमित (ज्याचे रेणू एकमेकांमधील आकर्षणामुळे साहचर्यात राहतात असे) संयुग आहे. याचे कारण ऑक्सिजन अणू ऋण विद्युती (इलेक्ट्रॉनांना आपणाकडे ओढणारे) असल्यामुळे ते समाईक इलेक्ट्रॉनांना आपल्याकडे जास्त खेचून घेतात. त्यामुळे हायड्रोजन अणूंवर किंचित धन विद्युत् भार येऊन ते पाण्याच्या दुसऱ्या रेणूतील ऑक्सिजनाकडे आकर्षिले जातात आणि त्यामध्ये एक प्रकारचा बंध निर्माण होतो. त्याला हायड्रोजन बंध म्हणतात. अशा प्रकारे पाण्याचे २ अथवा ३ रेणू संगमित अवस्थेत पाण्याच्या साध्या रेणूबरोबर समतोलावस्थेत पाण्यात अस्तित्वात असतात.
रासायनिक गुणधर्म : उच्च तापमानास (सु. १,२००° से. पेक्षा जास्त) पाण्याचे अंशतः विगमन (घटक मूलद्रव्यांत रूपांतर) होते आणि हायड्रोजन व ऑक्सिजन निर्माण होतात. सोडियम, पोटॅशियम व कॅल्शियम यांची पाण्याशी विक्रिया नेहमीच्या तापमानास घडून येते आणि हायड्रोजन व त्या त्या धातूंची हायड्रॉक्साइडे बनतात.
|
Ca |
+ |
2H2O |
= |
Ca(OH) 2 |
+ |
H2 |
|
कॅल्शुयम |
पाणी |
कॅल्शियम हायड्रॉक्साइड |
हायड्रोजन |
अशी विक्रिया मॅग्नेशियम, जस्त व लोखंड या धातू पाण्याच्या वाफेवर घडवून आणतात.
क्लोरीन वायू पाण्यात विरघळतो आणि त्यापासून हायड्रोक्लोरिक व हायपोक्लोरस ही अम्ले बनतात. हायपोक्लोरस अम्लापासून नंतर ऑक्सिजन बाहेर पडतो.
|
H2O |
+ |
Cl 2 |
= |
HCI |
+ |
HOCI |
|
पाणी |
क्लोरीन |
हायड्रोक्लोरिक अम्ल |
हायपोक्लोरस अम्ल |
|
2 HOCI |
= |
2HCI |
+ |
O 2 |
|
हायपोक्लोरस अम्ल |
हायड्रोक्लोरिक अम्ल |
ऑक्सिजन |
तप्त कोळशावर (कार्बनवर) वाफेचा प्रवाह सोडला असता कार्बन मोनॉक्साइड व हायड्रोजन यांचे मिश्रण मिळते. त्याला ⇨ पाणवायू म्हणतात. हे एक इंधन आहे.
|
C |
+ |
H 2O |
= |
CO |
+ |
H 2 |
|
कार्बन |
पाणी |
कार्बन मोनॉक्साइड |
हायड्रोजन |
धातूंच्या ऑक्साइडांवर पाण्याची विक्रिया होऊन क्षार (अल्कली) बनतात. उदा.,
|
CaO |
+ |
H 2O |
= |
Ca(OH)2 |
|
कॅल्शियम ऑक्साइड |
पाणी |
कॅल्शियम हायड्रॉक्साइड |
अधातूंच्या ऑक्साइडांपासून याच तऱ्हेने अम्ले बनतात. उदा.,
|
SO3 |
+ |
H2O |
= |
H2SO4 |
|
सल्फर ट्राय-ऑक्साइड |
पाणी |
सल्फ्यूरिक अम्ल |
कॅल्शियम कार्बाइडावर पाण्याची विक्रिया होऊन ॲसिटिलीन वायू व कॅल्शियम हायड्रॉक्साइड ही संयुगे बनतात.
|
CaC3 |
+ |
2H 2 O |
= |
C2H2 |
+ |
Ca(OH)2 |
|
कॅल्शियम कार्बाइड |
पाणी |
ॲसिटिलीन |
कॅल्शियम हायड्रॉक्साइड |
हॅलोजनी संयुगांपासून हॅलोजनी अम्ल आणि हॅलोजनेतर मूलद्रव्याचे हायड्रॉक्साइड ही तयार होतात.
|
PCI3 |
+ |
3H2O |
= |
3HCI |
+ |
P(OH)3 |
|
फॉस्फरस ट्रायक्लोराइड |
पाणी |
हायड्रोक्लोरिक अम्ल |
फॉस्फोरिक अम्ल |
या प्रकारच्या काही संयुगांपासून वरील विक्रियेत ऑक्सिलवण बनते. उदा.,
|
BiCl3 |
+ |
H2O |
= |
BiOCI |
+ |
2HCI |
|
बिस्मथ ट्रायक्लोराइड |
पाणी |
बिस्मथ ऑक्सिक्लोराइड |
हायड्रोक्लोरिक अम्ल |
अनेक कार्बनी संयुगेही वरीलप्रमाणे पाण्याची विक्रिया होऊन विघटन पावतात. उदा.,
|
CH3COOC2H5 |
+ |
H2O |
= |
CH3COOH |
+ |
C2H5OH |
|
एथिल ॲसिटेट |
पाणी |
ॲसिटिक अम्ल |
एथिल अल्कोहॉल |
या तऱ्हेने झालेल्या पाण्याच्या विक्रियेला ⇨ जलीय विच्छेदन म्हणतात.
काही रासायनिक विक्रियांमध्ये पाणी उत्प्रेरकाचे (विक्रिया सुकर व्हावी म्हणून उपयोगी पडणाऱ्या पण शेवटी शिल्लक राहणाऱ्या पदार्थाचे) कार्य करते. उदा., कार्बन मोनॉक्साइड व ऑक्सिजन हे वायू कोरडे करून मिसळले व मिश्रणात विजेची ठिणगी पाडली, तरी त्यांचा संयोग जवळजवळ घडतच नाही परंतु मिश्रणात पाण्याचा अंश असेल, तर विक्रिया इतकी झपाट्याने होते की, मिश्रणाचा स्फोट होतो.
कित्येक संयुगांबरोबर पाणी समावेशक (संयुगांचे मूळ घटक तसेच ठेवून त्यांत विक्रियाकारक सामावून गेल्याने बनणारी) संयुगे बनविते. अशा संयुगांना हायड्रेटे म्हणतात. उदा., CuSO4. 5H2O कॉपर सल्फेट पेंटाहायड्रेट [⟶ जलसंयोग].
अफेनद पाणी: पाणी खडकांतून वाहत जाते तेव्हा त्यामध्ये कॅल्शियम व मॅग्नेशियम यांची सल्फेटे व क्लोराइडे असतील, तर ती त्यात विरघळतात. पाण्यात सामान्यतः कार्बन डाय-ऑक्साइड थोड्या प्रमाणात विरघळलेला असतो. असे कार्बन डाय-ऑक्साइडमिश्रित पाणी कॅल्शियम व मॅग्नेशियम कार्बोनेटे असलेल्या खडकांच्या सान्निध्यात आले म्हणजे रासायनिक विक्रिया होऊन कॅल्शियम व मॅग्नेशियम बायकार्बोनेटे अनुक्रमे तयार होतात आणि ती विद्राव्य असल्यामुळे पाण्यात विरघळतात.
|
CaCO3 |
+ |
H2O |
+ |
CO2 |
= |
Ca(HCO3)2 |
|
कॅल्शियम कार्बोनेट |
पाणी |
कार्बन डाय-ऑक्साइड |
कॅल्शियम बायकार्बोनेट |
ही बायकार्बोनेटे, सल्फेटे व क्लोराइडे असलेले पाणी साबणाने कपडे धुण्यासाठी वापरता येत नाही. अशा पाण्यात साबणाचा फेस होत नाही म्हणून त्याला अफेनद (फेस न देणारे) पाणी म्हणतात. साबणाबरोबर या संयुगांची रासायनिक विक्रिया होते व अविद्राव्य पदार्थ (उदा., कॅल्शियम स्टिअरेट, मॅग्नेशियम स्टिअरेट) बनतात. त्यामुळे साबण वाया जातो इतकेच नव्हे, तर बनलेल्या अविद्राव्य पदार्थांचा थर कपड्यावर बसून ते जास्त मलिन होण्याचाही संभव असतो.
बायकार्बोनेटांमुळे अफेनद झालेले पाणी उकळले असता फेनद बनते. कारण उकळल्याने बायकार्बोनेटाचे अविद्राव्य कार्बोनेट बनते व वेगळे होते. अशा पाण्याला ‘तात्पुरते अफेनद’ पाणी म्हणतात.
|
Ca(HCO3)2 |
= |
CaCO3 |
+ |
H2O |
+ |
CO2 |
|
कॅल्शियम बायकार्बोनेट (विद्राव्य) |
कॅल्शियम कार्बोनेट (अविद्राव्य) |
पाणी |
कार्बन डाय-ऑक्साइड |
कॅल्शियम व मॅग्नेशियम यांची सल्फेटे व क्लोराइडे यांमुळे आलेली अफेनदता पाणी केवळ उकळल्याने दूर होत नाही, म्हणून अशा पाण्याला ‘कायम अफेनद’ पाणी म्हणतात. ते फेनद करण्यासाठी अशा पाण्यात धुण्याचा सोडा-सोडियम कार्बोनेट-मिसळावा लागतो. मॅग्नेशियम सल्फेटाबरोबर पुढील विक्रिया घडते. मॅग्नेशियम कार्बोनेट अविद्राव्य असल्यामुळे खाली बसते.
|
MgSo4 |
+ |
Na2CO3 |
= |
MgCO3 |
+ |
Na2SO4 |
|
मॅग्नेशियम सल्फेट |
सोडियम कार्बोनेट |
मॅग्नेशियम कार्बोनेट (अविद्राव्य) |
सोडियम सल्फेट |
वाफ तयार करण्यासाठी आणि उद्योगधंद्यातील कित्येक प्रक्रियांसाठी अफेनद पाणी चालत नही [⟶ पाणीपुरवठा]. पाण्याच्या फेनदीकरणासाठी अलीकडे आयन-विनिमय तंत्र [⟶ आयन-विनिमय] आणि एथिलीन डाय-अमाइन टेट्राॲसिटिक अम्लाचा उपयोग करून ग्राभणक्रिया [⟶ ग्राभण] वापरतात.
जड पाणी: जड पाण्याच्या रेणूमध्ये साध्या पाण्याच्या रेणूतील हायड्रोजन अणूंच्या ऐवजी २ द्रव्यमानांक असलेल्या हायड्रोजन समस्थानिकाचे (अणुक्रमांक तोच पण भिन्न अणुभार असलेल्या त्याच मूलद्रव्याच्या प्रकाराचे) दोन अणू असतात. त्याला ड्यूटेरियम ऑक्साइड असेही म्हणतात. त्याचे रेणुसूत्र D2O असे आहे [⟶ड्यूटेरियम, ट्रिटियम व जड पाणी].
बहुवारिक पाणी : (पॉलिवॉटर). रशियातील एन्. एन्. फेड्याकिन तसेच बी. व्ही. डेरजॅग्युइन व त्यांचे सहकारी यांनी १९६२ च्या सुमारास बहुवारिकाच्या (दोन वा अधिक रेणूंचा संयोग होऊन तयार झालेल्या जटिल संयुगाच्या) रूपात असलेला एक पाण्याचा प्रकार सापडल्याचे आणि त्याचे गुणधर्म सामान्य पाण्यापेक्षा वेगळे असल्याचे प्रसिद्ध केले होते परंतु नंतर अनेक प्रयोगशाळांत झालेल्या संशोधनानेही त्याचे अस्तित्व सिद्ध झाले नाही. शेवटी १९७३ मध्ये डेरजॅग्युइन यांनी या संशोधनाचा निष्कर्ष मान्य केला.
सजीव सृष्टी व पाणी : सजीव प्राण्यांच्या शरीरातील नानाविध घडामोडींसाठी पाणी अत्यंत आवश्यक असते. उदा., अन्नपचनादिक्रिया घडण्यासाठी माध्यम म्हणून, शरीराचे तापमान नियंत्रित राहण्यासाठी आणि शरीरातील निरुपयोगी द्रव्यांच्या उत्सर्जन क्रियांसाठी. समशीतोष्ण हवामानात हलके काम करताना सामान्य मनुष्याच्या शरीरातील सु. २·५ लि. पाणी दररोज नाहीसे होते व त्याची भरपाई करावी लागते. खाद्ये व पेये यांत असलेले पाणी आणि शरीरांतील रासायनिक विक्रियांत बनणारे पाणी यांपासून त्यापैकी काही भाग मिळतो आणि साधारणपणे १ लि. पाणी प्रत्यक्ष प्यावे लागते. यासाठी निसर्गातील पाण्यावर यथायोग्य संस्करण करून ते पुरविले जाते [⟶पाणीपुरवठा]. शेतीसाठी पाणी अत्यावश्यक असते [⟶सिंचाई].
यांशिवाय विद्युत् निर्मितीसाठी, उष्णता किंवा यांत्रिक शक्ती यांच्या उत्पादनाकरिता वाफ बनविण्यासाठी, माल व उतारू यांची वाहतूक करण्यासाठी [à जलवाहतूक], आग विझविण्याकरिता, जलदाबयंत्रात माध्यम म्हणून, अनेक औद्योगिक प्रक्रियांत शीतलनासाठी (थंड करण्यासाठी), रासायनिक विक्रियांचे माध्यम म्हणून, शहरे आणि उद्योगधंदे यांतील टाकाऊ व अपायकारक पदार्थ वाहून नेण्यासाठी पाण्याचा उपयोग केला जातो. उद्योगधंद्यात प्रक्रियांचे तापमान नियंत्रित करण्यासाठी व मासळी, फळे इ. पदार्थ टिकावेत म्हणून बर्फाच्या रूपाने पाणी वापरले जाते.
अभिज्ञान : पदार्थात असलेल्या पाण्याचे प्रमाण निश्चित करण्यासाठी वजन करून घेतलेला पदार्थ नियंत्रित तापमानात तापवून व नंतर वजन करून वजनात झालेली घट ठरवितात किंवा पदार्थ तापविताना कोरड्या नायट्रोजनचा प्रवाह प्रथम त्या पदार्थावरून व नंतर वजन करून ठेवलेल्या कॅल्शियम क्लोराइड भरलेल्या नळीमधून जाऊ देऊन नळीच्या वजनात किती वाढ झाली ते काढतात. कार्ल फिशर विक्रियाकारकाचा उपयोग करून [⟶अनुमापन] कार्बनी द्रव पदार्थ आणि खनिज लवणे यांमधील जलांशाचे प्रमाण ठरविता येते.
पहा : जलसंधारण, पाणीपुरवठा प्रदूषण वनस्पति व पाणी सिंचाई.
संदर्भ : 1. Eisenberg, D. Kauzmann, W. The Structure and Properties of Water, London, 1969.
2. Kavanau, J. L. Water and Solute-Water Interactions, San Francisco, 1954.
बांदिवडेकर, प्र. ह.
“