ॲनिलीन : रासायनिक संयुग. सूत्र C6H5NH2. हे प्राथमिक ॲरोमॅटिक अमाइनांपैकी सर्वांत साधे ⇨अमाइन आहे. निळीच्या स्पॅनिश भाषेतील ‘आ निल’ या नावावरून ‘ॲनिलीन’ हे नाव आलेले आहे. नैसर्गिक निळीचे भंजक ⇨ऊर्ध्वपातन करून ॲनिलीन प्रथम मिळविण्यात आले. ते तेलासारखे असून शुद्ध रूपात वर्णहीन असते, पण बाजारी नमुने उजेडात व हवेत राहिल्यावर त्यांना प्रथम पिवळा व अखेरीस काळाही रंग येतो.
गुणधर्म : रेणुभार ९३ वितळबिंदू -६° से. उकळबिंदू १८४° से. वि.गु. १·०२ पाण्यात किंचितसे आणि अल्कोहॉल व ईथरामध्ये सर्रास विरघळते. त्याला विशिष्ट दुर्गंध असून ते विषारी आहे.
कृती : (१) लोहाचे कातरे व ३०% हायड्रोक्लोरिक अम्ल यांनी नायट्रोबेंझिनाचे ⇨क्षपण करून ॲनिलीन तयार केले जाते.
| Fe+HCl
→ |
||||||
| C6H5NO2 | + | 6[H] | C6H5NH2 | + | 2H2O | |
| नायट्रोबेंझीन | ॲनिलीन |
विक्रिया पुरी झाल्यावर वरील पदार्थांच्या मिश्रणात सोडा घालून मिश्रण उदासीन (अम्लधर्मी किंवा क्षारकधर्मी म्हणजे अम्लाबरोबर विक्रिया झाल्यास लवण देणाऱ्या पदार्थाच्या धर्माचे नसलेले) करतात व त्याच्यातील ॲनिलीन पाण्याच्या वाफेबरोबर ऊर्ध्वपातन करून बाहेर काढतात. ऊर्ध्वपातित विद्रावात पाणीही असते. पाण्यात ॲनिलीन किंचित विद्राव्य (विरघळणारे) पण मिठाच्या विद्रावात अविद्राव्य असते, म्हणून ऊर्ध्वपातित विद्रावात पुरेसे मीठ घालतात. त्याचे पाणी ॲनिलीन असे दोन थर होतात. ते झाल्यावर ॲनिलीन वेगळे केले जाते.
(२) आणखी एका वेगळ्या पद्धतीत, क्युप्रस ऑक्साइडाच्या सान्निध्यात क्लोरोबेंझीन हे जलीय (पाण्यात विरघळलेल्या) अमोनियाबरोबर २००°से. तापमानात व पुरेशा दाबाखाली तापवून ॲनिलीन तयार करण्यात येते.
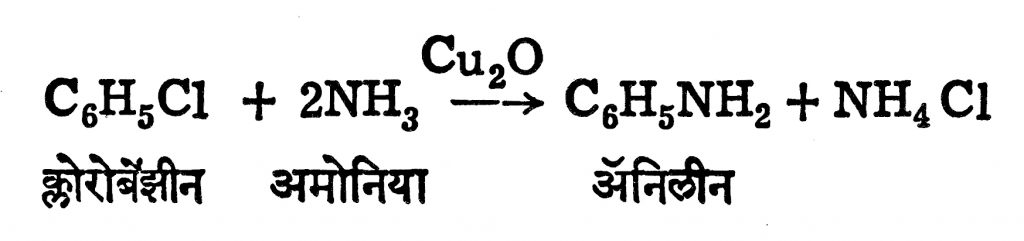
(३) निकेलाच्या उत्प्रेरकाच्या (विक्रियेत भाग न घेता ती जलद घडवून आणणाऱ्या पदार्थाच्या) सान्निध्यात नायट्रोबेंझिनाचे क्षपण करूनही ॲनिलीन मिळवितात.
ॲनिलिनाच्या विक्रिया : (१) ॲसिटल क्लोराइड किंवा ॲसिटिक ॲनहाइड्राइड यांच्या विक्रिया होऊन ॲनिलिनापासून ॲसिटानिलाइट तयार होते.
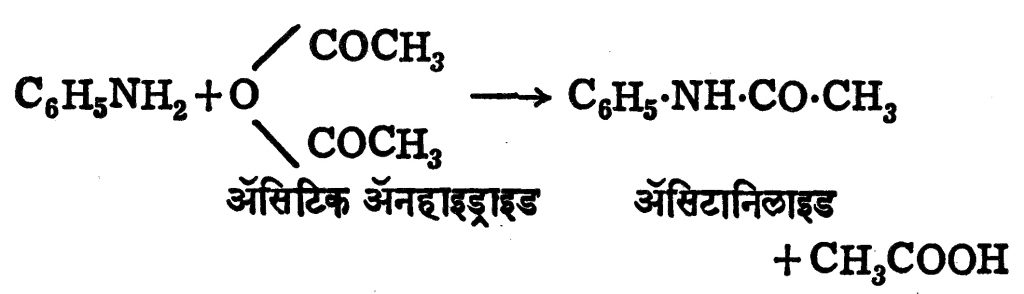
(२) ॲनिलिनामध्ये अतिरिक्त (वाजवीपेक्षा जास्त) क्लोरीनजल (किंवा ब्रोमीनजल) घातले असता २:४:६ ट्रायक्लोरो (किंवा ट्रायब्रोमो) ॲनिलीन हा अनुजात (एका संयुगापासून तयार केलेले दुसरे संयुग) तयार होऊन तो अवक्षेपित होतो (साका तयार होतो).
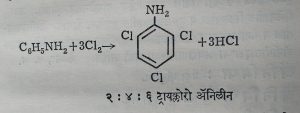
(३) काही विशिष्ट परिस्थितीत (म्हणजे जवळजवळ शून्य अंश से. तापमानात व खनिज अम्लांच्या सान्निध्यात) ॲनिलिनासारख्या प्राथमिक (संयुजा बंधांपैकी एकच बंध दुसऱ्या कार्बन अणूबरोबर जोडलेल्या) ॲरोमॅटिक अमाइनांची नायट्रस अम्लाशी विक्रिया होऊन डायाझोनियम संयुगे तयार होतात.
C2H5NH2 ± HNO2 ±HCL → C6H5N2CL ± 2H2O
नायट्रस अम्ल बेंझीन डायाझोनियम क्लोराइड
ती सैद्धांतिक दृष्ट्या तसेच औद्योगिक दृष्ट्या महत्त्वाची आहेत. रंजकद्रव्ये, कित्येक औषधे व ॲरोमॅटिक संयुगेही संश्लेषणाने (घटकरेणू वा अणू एकत्र आणून कृत्रिम पद्धतीने) बनविण्यासाठी त्यांचा उपयोग होतो. अशा उत्पादनासाठी ॲनिलिनाचा फार मोठ्या प्रमाणात उपयोग होतो.
(४) ॲनिलीन व ॲरोमॅटिक आल्डिहाइडे यांचे संघनन होऊन (दोघांचे मिळून एक संयुग बनून) पाणी वेगळे होते व ॲझो मिथाइने (शिफ क्षारक) तयार होतात.

(५) ॲनिलिनातील NH2 मधील एक अथवा दोन्ही हायड्रोजन अणू अल्किल गटांनी प्रतिष्ठापित होऊन (एक अणू काढून त्या ठिकाणी दुसरा बसविला जाऊन) अल्किल ॲनिलिने मिळतात. उदा., मिथिल ॲनिलीन व डायमिथिल ॲनिलीन. ॲनिलीन व मिथील अल्कोहॉल यांचे मिश्रण सल्फ्यूरिक अम्ल उत्प्रेरक वापरून ऑटोक्लेव्हात (एक प्रकारच्या दाबपात्रात) २३०°से. तापमानास तापवून त्यांचे औद्योगिक उत्पादन करतात.
उपयोग : अनेक रंजकद्रव्ये, औषधी पदार्थ, रबराच्या धंद्यात उपयोगी पडणारी रसायने इत्यादींच्या उत्पादनात महत्त्वाचा मध्यस्थ (उत्पादनप्रक्रियेत अंतिम पदार्थ मिळविण्यापूर्वी तयार करावा लागणारा आवश्यक पदार्थ) म्हणून ॲनिलीन उपयोगी पडते.
संदर्भ : Finar, I. L. Organic Chemistry, Vol. I, London, 1962.
गडम, दि. द.