तुरटी : (ॲलम). त्रिसंयुजी [अणूंची परस्परांशी संयोग पावण्याची क्षमता दर्शविणारा अंक तीन असलेल्या → संयुजा] मूलद्रवाचे सल्फेट, ⇨ जलसंयोगाचे २४ रेणू आणि एकसंयुजी मूलद्रव्याचे सल्फेट यांच्यापासून बनलेल्या सजल द्विलवणांचा (ठराविक प्रमाणात एकत्रितपणे स्फटिकीभूत होणाऱ्या परंतु विद्रावात स्वतंत्रपणे अस्तित्वात असणाऱ्या दोन साध्या लवणांपासून बनणाऱ्या लवणांचा) एक वर्ग. तुरटी या नावाने सामान्यतः ओळखला जाणारा पदार्थ म्हणजे पॉटॅशियम ॲल्युमिनियम सल्फेट किंवा पोटॅश ॲलम हा होय. तुरटीचे सर्वसामान्य रासायनिक सूत्र X2SO4· Y2(SO4)3· 24H2O असे आहे. या मध्ये X = सोडियम, पॉटॅशियम, अमोनिया, सिझियम, चांदी, रुबिडियम, थॅलियम, हायड्रॅझीन, हायड्रॉक्सिल अमाइन, काही कार्बनी अमाइने अथवा लिथियम यांसारखे एकसंयुजी ऋणायन (लवणाच्या विद्वावातून विद्युत् प्रवाह जाऊ दिला असता ऋणाग्राकडे जाणारे धनभारित आयन–अणू, अणुगट वा रेणू) आणि Y = ॲल्युमिनियम, लोह क्रोमियम, मँगॅनीज, कोबाल्ट, कॅलियम, टिटॅनियम, व्हॅनेडियम, इरिडियम, ऱ्होडियम, इंडियम इ. त्रिसंयुजी ऋणायन असू शकतात. तथापि सैद्धांतिक दृष्ट्या शक्य असलेल्या या तुरट्यांपैकी बऱ्याचशा अद्याप तयार करण्यात आलेल्या नाहीत. पोटॅश तुरटीचे सूत्र K2SO4·AI2(SO4)3·24H2O किंवा KAI (SO4)2·12H2O असे लिहितात. अमोनिया तुरटीचे सूत्र (NH4)2SO4·Al2(SO4)3·24H2O किंवा (NH4)AI(SO4)2·12H2O असे आहे.
इतिहास : मानवास सु. ३,०००–४,००० वर्षांपासून तुरटी माहीत असावी असा पुरावा आढळला आहे. प्राचीन ईजिप्तमध्ये मरूद्यानाच्या (ओॲसीसच्या) सभोवती नैसर्गिक स्वरूपातील अशुद्ध तुरटी सापडत असल्याचे व ती शुद्ध करण्याची कृती तेथील लोकांना माहीत होती. भारतातील लोकांना प्राचीन काळापासून तुरटीचा उपयोग कापडावर रंग पक्का बसविण्याकरिता (रंगबंधक म्हणून) करता येतो हे माहीत होते, असे उल्लेख प्राचीन संस्कृत ग्रंथांत आढळून येतात. तुरटीचा उल्लेख वराहमिहिर (सहावे शतक) यांनी रंगबंधक म्हणून केलेला आहे. तुरटीला संस्कृत भाषेत आढकी, काक्षी, मूत्स्ना, तुवरिका, मृत्तालक व सुराष्ट्रज अशी नावे आहेत. मराठी भाषेत तुरटीला फिटकारी, स्फटिकारी, फटकारी, शिब, झीक फटकी, चकचिन इ. नावे आहेत. भारतात पूर्वी चीनमधून तुरटी येत असे, ती सौराष्ट्रातही तयार करीत असत.
तुरटी तयार करण्याच्या कृतीचा पूर्वेतिहास ज्ञात नाही. प्लिनी (इ. स. २३–७९) या रोमन विद्वानांच्या Historia Naturalis या ग्रंथात ‘ॲल्युमेन’ चा (मूळ लॅटिन शब्द अर्थ तुरटी) उल्लेख अनेक लवणांचे मिश्रण असा केलेला आहे. पंधराव्या शतकात तुर्कस्तान भागात कापड व लोकर यांसाठी रंगबंधक म्हणून तुरटी वापरीत होते. १४६० च्या सुमारास जॉन डी कास्ट्रो यांनी कॉन्स्टँटिनोपलमध्ये तुरटी कशी तयार करतात, याविषयी माहिती मिळवून त्यानुसार इटलीतील टोल्फा येथे ॲल्युनाइटापासून तुरटी तयार करण्यास सुरुवात केली. ही पद्धत अद्यापही वापरली जाते. १६०० च्या सुमारास इंग्लंडमध्ये सुभाजांपासून (सहज भंग पावणाऱ्या एक प्रकारच्या खडकापासून) ती तयार करण्यात येऊ लागली. १८४५ मध्ये सुभाजाऐवजी ॲल्युमिनियमयुक्त शेल (एक प्रकारचा खडक) वापरून इंग्लंडमध्ये ती बनविण्यात येऊ लागली. यानंतर विविध प्रकारच्या तुरट्या तयार करण्यात येऊ लागल्या.
कृती : सर्वसामान्यतः विद्रावातून अवक्षेपणाने (न विरघळणारा साका तयार करून) तुरट्या तयार करतात. उदा., पोटॅश तुरटी तयार करण्यासाठी ॲल्युमिनियम सल्फेट आणि पोटॅशियम सल्फेट पाण्यात विरघळवितात व तो विद्राव तापवून त्यातील पाण्याचे प्रमाण कमी करतात आणि मग तुरटीचे स्फटिक बनण्यास सुरुवात होते. एकसंयुजी आयनाचे आकारमान त्रिसंयुजी आयनापेक्षा मोठे झाल्यास तुरटी सहज रीत्या तयार होते, असे मानले जाते. यानुसार सिझियम या मोठ्या एकसंयुजी आयनाच्या सर्व त्रिसंयुजी आयनांबरोबर तुरट्या तयार होतात, तर लिथियम या लहान एकसंयुजी आयनाची फक्त ॲल्युमिनियम या त्रिसंयुजी आयनाबरोबरच तुरटी तयार होते. सल्फेट आयनाऐवजी सिलेनेट, फ्ल्युओरोबेरिलेट (BeF42-) वा क्लोरोझिंकेट (ZnCI42-) हे आयन प्रतिष्ठापित करूनही (एक अणू किंवा रेणू काढून त्याऐवजी दुसरा अणू वा रेणू घालूनही) तुरट्या बनवितात.
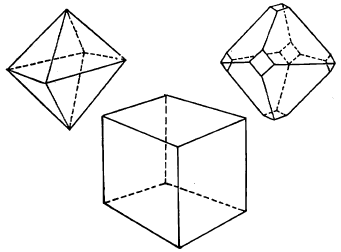
गुणधर्म : पोटॅश तुरटी ही सर्व तुरट्यांत महत्त्वाची असून तिची चव गोडसर तुरट व अम्लीय (आंबट) असते. ही तुरटी रंगहीन व गंधहीन असून ती कठीण, दुधी काचेसारखी पारभासी व अष्टकोनी वा घनाकार स्फटिकाच्या स्वरूपात किंवा पांढऱ्या चूर्ण रूपात मिळते. पोटॅश व अमोनियम तुरट्या हवेत स्थिर असतात, पण सोडियम तुरटी हवेने फुलारते आणि तिचे तुकडे होतात. अमोनियम तुरटीचे स्फटिक रंगहीन असून तिला तुरट चव असते.
३७°–११७° च्या दरम्यानच्या तापमानाला बहुतेक सर्व तुरट्या त्यांच्यात असणाऱ्या पाण्यात विरघळतात. हवेच्या सान्निध्यात काळजीपूर्व तापविल्यास पोटॅश तुरटी १००° से. ला निर्जल होते, एकदम तापविल्यास ती फुलारते आणि भुसभशीत ठिसूळ पदार्थ तयार होतो, त्याला ‘तुरटीची लाही’ असे म्हणतात. जास्त तापमानाला अमोनियम तुरटीचे शुद्ध ॲल्युमिनियम ऑक्साइडात रूपांतर होते.
निरनिराळ्या तुरट्यांचे पाण्यातील विरघळण्याचे प्रमाण वेगवेगळे आहे. १५° से. ला १०० भाग पाण्यात सिझियम तुरटी ०·३५ भाग, पोटॅश तुरटी ९·५९ भाग, अमोनियम तुरटी १२·६६ भाग तर १६° से. ला सोडियम तुरटी ५१ भाग ह्या प्रमाणात विरघळते. ९०° से. ला पाण्याच्या कित्येक पट पोटॅश तुरटी त्यात विरघळते. तुरट्यांचा विद्राव अम्लधर्मी असतो. पोटॅश तुरटी अल्कोहॉलात विरघळत नाही. तुरटीची लाही पाण्यात हळूहळू विरघळते, पण ती पूर्णपणे विरघळत नाही. प्रथिनांच्या विद्रावात तुरटी मिसळल्यास प्रथिने अवक्षेपित होतात. तुरटीमुळे कलिलातील (अतिसूक्ष्म कण लोंबकळत असलेल्या विशिष्ट प्रकारच्या द्रव मिश्रणातील) कणांचे अवक्षेपण होते. तुरटीमुळे जिलेटीन कठीण बनते.
उपयोग : पोटॅश तुरटीचा उपयोग रंगबंधक म्हणून, आगकाडीचा गुलाव्यतिरिक्त भाग अग्निरोधी करण्यासाठी, पाणी शुद्ध करण्यासाठी इ. कामांसाठी करतात. तुरटीच्या लाहीचा उपयोग ⇨ चर्मपूरणात परिरक्षक म्हणून, व्रण व जखमा धुण्यासाठी, हिरड्या फुटण्यावर स्तंभक (आकुंचन करणारी) म्हणून, गुळण्या करण्यासाठी, बाह्योपचारात रक्तस्रावरोधी म्हणून, फेसयुक्त अग्निशामकात, तसेच उत्तर भारतात उंट व म्हशी यांच्या पिण्याच्या पाण्यात मिसळण्यासाठी इ. कामांसाठी वापरतात. अमोनियम तुरटीचा उपयोग पोटॅश तुरटीसारखाच करतात. त्यांशिवाय तिचा उपयोग बेकिंग चूर्णात (भिजविलेल्या पिठात कार्बन डाय–ऑक्साइड निर्माण व्हावा म्हणून यीस्टऐवजी वापरण्यात येणाऱ्या रासायनिक द्रव्यांच्या चूर्णात) करतात. सोडियम तुरटीचा उपयोग पाणी शुद्ध करण्यासाठी, रंगबंधक म्हणून व बेकिंग चूर्णात करतात. क्रोम तुरटीचा उपयोग कातडी कमावण्यासाठी व कापड उद्योगात रंगबंधक म्हणून करतात. फेरिक तुरटीचा रंगबंधक म्हणून आणि औषधी उपयोगासाठी (स्तंभक, गुळण्या करण्यासाठी आणि अंतर्गत रक्तस्राव थांबविण्यासाठी) वापर करतात.
द्रव हिलियममुळे मिळणाऱ्या नीच तापमानापेक्षाही कमी तापमान (सु. ०·१० से.पर्यंत) पोटॅश व क्रोम तुरटी यांच्या मिश्रणाचा वापर करून मिळविता येते व मोजताही येते [→ नीच तापमान भौतिकी].
संदर्भ : 1. Parkes, G. D. Ed. Mellor’s Modern Inorganic Chemistry, London, 1961.
2. Partington, J. R. General and Inorganic Chemistry, London, 1966.
आठवले, वि. त्र्यं.
“