विगमन : विद्युत् चुंबकीय प्रारण (उदा., प्रकाश प्रारण म्हणजे तरंगरूपी ऊर्जा) शोपले जाऊन अथवा अन्य पदार्थाशी टक्कर होऊन काही संयुगांच्या रेणूंचे दोन वा अधिक घटकांत (उदा., अणू, रेणू, आयन किंवा मूलक यांत) विभाजन होण्याची प्रक्रिया. (विद्युते भारित अणू, रेणू वा अणुगट म्हणजे आयन, तर विक्रियेत तसाच राहणारा, पण स्वतंत्र अस्तित्व नसलेला अणुगट म्हणजे मूलक होय). विद्राव केल्याने अथवा प्रकाश, उष्णता इ. बाह्य ऊर्जास्त्रोतांमुळे पदार्थात विगमन सुरू होते. विगमनाची प्रक्रिया व्युत्क्रमी म्हणजे उलट दिशेत होणारी असते. याचा अर्थ विभाजित घटकांचे स्थलांतर झालेले नसल्यास व्युत्क्रमी प्रक्रियेमध्ये या घटकांपासून पुन्हा मूळ संयुग तयार होते.
औष्णिक विगमन : उष्णतेच्या साहाय्याने होणाऱ्या विगमन प्रक्रियेस औष्णिक विगमन असे म्हणतात. अमोनियम क्लोरइड (नवसागर) या पदार्थाला उष्णता दिली असता त्याच्या काही भागाचे अमोनिया वायू व हायड्रोक्लोरिक अम्ल या रेणूंमध्ये (घटकांमध्ये) विभाजन होते आणि काही भाग तसाच राहतो. ही प्रक्रिया व्युत्क्रमी असते म्हणजे अमोनिया वायू व हायड्रोक्लोरिक अम्ल यांचे रेणू एकमेकांशी संयोग पावून पुन्हा अमोनियम क्लोराइड रेणू तयार होतात. ही प्रक्रिया पुढील समीकरणाने दर्शविता येते.
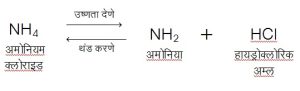 |
फॉस्फरस पेटाक्लोराइड व चुनखडी यांचे विगमन ही औष्णिक विगमन प्रक्रियेची परिचित उदाहरणे आहेत. तसेच उच्च तापमानाला पाण्याचे हायड्रोजन व ऑक्सिजन यांच्यात विभाजन होऊन विगमन होते. या तीन विक्रिया सूत्ररूपांत पुढीलप्रमाणे दाखवितात.
 |
 |
2H2O ⟶ 2H2+O2
आयनी विगमन : इ. स. १८८७ साली स्वांटे ऑगस्ट अऱ्हेनियस यांनी अम्ले, क्षारक (अम्लाशी विक्रिया झाल्यास लवणे देणारे पदार्थ) व लवणे ही संयुगे विद्युत् विच्छेद्य आहेत, असा सिद्धांत मांडला. यानुसार वितळलेल्या अथवा विद्रावात (विशेषतः पाण्यात) विरघळविलेल्या अशा संयुगांतून विजेचा प्रवाह जाऊ शकतो. नेहमीच्या परिस्थितीत ही सर्व विद्युत् भाररहित असतात परंतु ज्या वेळी पाण्यात विरघळवून त्यांचा विद्राव केला जातो, त्या वेळी या विद्युके भाररहित संयुगाच्या रेणूंचे धन आणि ऋण अशा दोन निरनिराळ्या विद्युत् भारित आयनांमध्ये हे विभाजन होते. विभाजन न झालेल्या रेणूंच्या संख्येत व दोन निरनिराळ्या प्रकारच्या विद्युत भारित आयनांच्या संख्येमध्ये समतोल राखला जातो. उदा.,
NaCI ⇌Na+ + CI−
येथे सोडियम क्लोराइड (मीठ) या धन विद्युत् भारित सोडियम आयन व ऋण विद्युत् भारित क्लोरीन आयन यांमध्ये विगमन झाले. अशा तऱ्हेने विगमन झालेल्या लवणातील आयनांचे पुन्हा एकत्रीकरण होऊन लवणाचा रेणू तयार होतो. ही सर्व प्रक्रिया मिश्रणामध्ये होत असते.
अशा तऱ्हेच्या विद्रावामध्ये निरनिराळया विद्युत् भारांचे आयन निर्माण करमाऱ्या प्रक्रियेला आयनी विगमन किंवा विद्युत् विच्छेद्य विगमन असे म्हणतात. हे विगमन विद्रावाच्या विरलतेप्रमाणे म्हणजे जंशी संहती (विरळलेल्या पदार्थाचे प्रमाण) कमी होत जाईल तसे वाढत जाते. अपरिमित (अनंत) विरलतेच्या विद्रावामध्ये विद्युत् विच्छेद्य पदार्थाचे आयनामध्ये संपूर्ण विगमन झालेले असते, असे मानतात.
विद्युत् विच्छेद्य विगमन ही व्युत्क्रंमी प्रक्रिया असल्याने आयनांमध्ये रूपांतर न झालेल्या रेणूमध्ये व आयनांमध्ये एक प्रकारचा समतोल असतो. समजा, क्ष व य या दोन आयनांमध्ये विगमन झाले, तर त्यांतील समतोल पुढील सूत्राने दर्शविता येईल.
क्ष य ⟶ क्ष+ +य−
यामध्ये संहतीचा विचार केला, तर समतोलाच्या वेळी पुढील सूत्रात अभिप्रेत असलेली स्थिती असते.
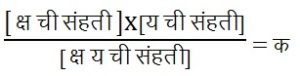 |
यामधील क या राशीला आयनी स्थिरांक किंवा विगमन स्थिरांक असे म्हणतात.
औष्णिक विगमनामध्ये देखील विगमन स्थिरांकाचा विचार केला जातो. उदा.,
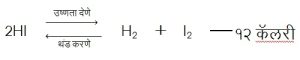 |
या प्रयोगात हायड्रोजन आयोडाइडाचे हायड्रोजन व आयोडीन यांमध्ये विगमन होते. यामध्ये उष्णता वाढविल्यास समतोल बिघडून तो उजवीकडे झुकतो आणि हायड्रोजन व आयोडीन यांचे प्रमाण वाढते आणि हायड्रोजन आयोडाइडचे प्रमाण कमी होते म्हणजे उष्णतेने विगमनाचे प्रमाण वाढते. विगमनामध्ये संयुगाचे किंवा अणूंचे प्रमाण तापमान, त्या वेळचा दाब व पदार्थाची संहती किंवा अवलंबून असते.
प्रकाशरासायनिक विगमन : नुसत्या प्रकाशाने रासायनिक पदार्थाचे रेणू किंवा अणूंमध्ये होणारे विभाजन म्हणजे प्रकाशरासायनिक विगमन होय. उदा.,
 |
H + HBr ⟶ H2 + Br
Br + Br ⟶ Br2
याचा उपयोग छायाचित्र काढण्याच्या प्रक्रियेत होतो. छायाचित्र पट्टीवरील सिल्व्हर ब्रोमाइडाचे प्रकाशाच्या साह्याने विगमन होऊन चांदी (Ag) ब्रोमीन (Br) हे अणू तयार होतात आणि छायाचित्र घेणे शक्य होते.
 |
विगमनाच्या प्रक्रियेमध्ये तापमान, दाब व संहती या तीन घटकांना फार महत्त्व असते. त्यांच्या नियमनाने रेणूचे उत्पादन करता येते. चुना, अमोनिया व ऑक्सिजन यांचे उत्पादन विगमन प्रक्रियेने करता येते.
दीक्षित, व, चिं.