विसरण : स्वयंप्रेरणे (उत्स्फूर्तपणे) पदार्थ आजूबाजूला पसरण्याची जी क्रिया होते त्या क्रियेस विसरण प्रक्रिया म्हणता येईल. या प्रक्रियेने नैसर्गिक रीत्या एक घटक दुसऱ्या घटकात मिसळला जातो. अर्थात निसर्गतः ते घटक एकमेकांत मिसळणारे असले पाहिजेत. या प्रक्रियेत बाह्य शक्तीने ढवळणे अथवा अन्य प्रकारे प्रवाह निर्माण करणे किंवा गती देणे अभिप्रेत नाही.
एखाद्या बंद खोलीत एका ठिकाणी जर आपण एखादे उडून जाणारे म्हणजेच बाष्पीभवन होणारे सुगंधी द्रव्य ठेवले, तर त्या खोलीत कुठल्याही प्रकारचा हवेचा प्रवाह नसतानासुद्धा, त्या पदार्थाचा सुगंध हळूहळू सर्व खोलीभर सारख्या प्रमाणात दरवळतो. सुगंधी द्रव्याची पृष्ठभागावर प्रथम वाफ होते आणि तेथून वायुरूपात विसरण प्रक्रियेने यथावकाश तो सुगंध सर्व खोलीभर सारख्या प्रमाणात पसरतो. तसाच प्रकार एखाद्या पात्रातील स्तब्ध पाण्यात मिठाचा खडा टाकला तर घडतो. खड्याच्या पृष्ठभागाशी मीठ पाण्यात विरघळते आणि तेथून ते विद्रावाचा एक घटक या स्वरूपात यथावकाश पात्रातील सर्व पाण्यात सारख्या संहतीत म्हणजेच सारख्या प्रमाणात पसरते. घन पदार्थाच्या बाबतीतही कित्येक वेळा असा प्रकार घडतो. शिशाच्या अगदी निकट सान्निद्यात ठेवलेले सोने हळूहळू विसरण प्रक्रियेने शिशामध्ये मिसळल्याचे आढळून येते.
वायू, द्रव्य इ प्रवाही पदार्थ मुद्दाम ढवळून त्यांच्या घटकांचे समप्रमाणात मिश्रण फार लवकर करता येईल. अशी क्रिया बाह्य ऊर्जेवर अवलंबून असते. विसरण प्रक्रियेने नैसर्गिक रीत्या मिसळले जाण्याची प्रक्रिया घटकांच्या फक्त अंतर्गत ऊर्जेवर अवलंबून असते. एक अवस्था मिश्रणात एखाद्या घटकाची संहती निरनिराळ्या ठिकाणी निरनिराळी असेल, तर कालांतराने त्या घटकांची त्या मिश्रणातील संहती एकसारखी होण्याची प्रक्रिया नैसर्गिक आहे. वायुरूप आणि द्रवरूप अवस्थांमध्ये अशी प्रक्रिया जाणवण्याइतक्या गतीने होते. घन पदार्थात विसरण प्रक्रिया न जाणवण्याइतक्या सूक्ष्म गतीने होते.
विषम प्रमाणात विखुरलेली संहती एकसारखी होण्याच्या प्रक्रियेत या विवक्षित घटकाच्या अणूंचे काही प्रमाणात एकीकडून दुसरीकडे स्थानांतरण म्हणजे स्थलांतर अपेक्षित आहे. या स्थलांतराकरिता गती आवश्यक आहे. अशी गती त्या घटकाच्या अणूंमध्ये, तापमानावर अवलंबून, अंगभूत (स्वयंस्थित) असते. सर्व पदार्थांचे सर्व अणू शून्य केल्व्हिन या तापमानाला गतिशून्य असतात. तापमान जसजसे वाढत जाते, त्या प्रमाणे घटकाच्या स्वभावधर्मानुसार (गुणधर्मानुसार) त्याच्या अणूंना विशिष्ट अंगभूत उर्जा प्राप्त झालेली आसते. या उर्जेचे द्दश्य स्वरूप त्या तापमानाला त्या घटकाच्या असलेल्या घन, द्रव अगर वायुरूपाने आपल्याला दिसते. वायुरूप अवस्थेत घटक बंदिस्त जागा पूर्णाशाने व्यापतो. वायूला पात्राचा आकार आणि आकारमान प्राप्त होतात. वायूला पृष्टभाग नसतो. द्रवरूप अवस्थेतील पदार्थ ज्या पात्रात ठेवला असेल त्या पात्राचा आकार घेतो पण त्याचे मूळचे आकारमान बदलत नाही. पाच लिटर द्रव दहा लिटरच्या गोल पात्रात ठेवला, तर त्याचा आकार अर्धगोल होऊन आकारमान पाच लिटरच राहते. द्रव पदार्थाला पृष्ठभाग असतो घन अवस्थेत पदार्थाला स्वतःचा आकार आणि स्वतःचे आकारमान असते. ज्या पात्रात तो ठेवला जातो, त्याच्या आकाराचा आगर आकारमानाचा त्याच्यावर परिणाम होत नाही ( वाळू, चूर्ण,इ घन पदार्थ सकृत् दर्शनी प्रवाही वाटतात पण हे पदार्थ एका अवस्थेत नसतात. असे पदार्थ अनेक सूक्ष्म घन कणांचे बनलेले असतात).
घन अवस्थेतील पदार्थांचे सर्व अणू एखाद्या काल्पनिक त्रिमितीय रांगोळीमधील ठिपक्यांप्रमाणे एका विशिष्ट जालकात म्हणजेच काल्पनिक पिंजऱ्यात इतर अणूंच्या संदर्भात आपापल्या जागा घट्ट पकडून बसलेले असतात. ही जालके स्फटिकरूप किंवा अस्फटिकरूप असतात. घन अवस्थेत अणूंची एकमेकांना पकडून ठेवणारी बंधने (बंध) द्दढ असतात. त्यामुळे फक्त अपवादात्मक परिस्थितीत अणू आपली जागा सोडून स्थांनांतरण करू शकतात. तापमानानुसार अंगभूत ऊर्जा अणूंच्या फक्त कंपनांच्या स्वरूपात अनुभवता येते. तापमान वाढत जाते त्याप्रमाणे अणूंची स्वतःची कंपने वाढत जातात आणि अंगभूत ऊर्जाही वाढते. पदार्थाच्या स्वभावधर्मानुसार एका विशिष्ट तापमानाच्या पुढे अणूंची अंगभूत ऊर्जा नुसत्या कंपनांपुरतीच मर्यादित राहत नाही. वाढत्या कंपनामुळे अणूंना एकमेकांशी घट्ट बांधून ठेवणारे बंध काहीसे सैल होतात. पदार्थाचे अणू अशा परिस्थितीत इतर अणूंच्या संदर्भात काही प्रमाणात हालचाल करू शकतात. अशा वेळी घन पदार्थाची जालके बऱ्याच प्रमाणात मोडतात आणि पदार्थ वितळतो. द्रवरूप अवस्थेत पदार्थाच्या अणूंना हालचालीचे मर्यादित स्वातंत्र प्राप्त होते. अणूंना एकमेंकाजवळ बांधून ठेवणारे बंध काही प्रमाणात अजून अस्तित्वात असतात.त्यामुळे द्रव अवस्थेत अणूंना प्रवाहीपणा प्राप्त झाला तरी पदार्थ एकजिनसी राहतो. त्याचा आकार बदलू शकतो, पण आकारमान कायम राहते.
द्रव पदार्थाचे तापमन आणखी वाढत राहिले, तर त्याच्या अणूंची हालचाल करण्याची क्षमता अधिकाधिक वाढत राहते शेवटी एक वेळ अशी येते की, वाढत्या तापमानमुळे द्रवाच्या अणूंना एकमेकांजवळ बांधून ठेवणारे सर्व बंध संपुष्टात येतात आणि त्या पदार्थाच्या इतर अणूंच्या संदर्भात प्रत्येक अणू मुक्तपणे संचार करू शकतो. (⟶ बाष्पीकरण) या परिस्थितीत आकारमानाचेही बंधन राहत नाही दिलेल्या बंदिस्त जागेचा आकार आणि आकारमान वायुरूप पदार्थ घेतो वायुरूप पदार्थाचे सर्व अणू अंगभूत ऊर्जेच्या जोरावर इतर अणूंच्या संदर्भात स्वैर संचार करण्यास मोकळे असतात (⟶ द्रव्याचा गत्यात्मक सिद्धांत). अधिक तापमानात अंगभूत ऊर्जा अधिक असते आणि अणूंचीः स्वतःची गतीही अधिक असते. अर्थात स्वैरसंचार करणारे हे अणू एखाद्या पात्रात कोंडलेले असल्याने सर्वस्वी मुक्त नसतात. थोडेसे अंतर चालून गेल्यावर त्याच अवस्थेतील इतर गतिमान अणूंबरोबर त्यांच्या सतत टकरा होत असतात. अशा टकरांमुळे अणूंच्या मुक्त गतीची दिशाही सारखी बदलत असते.
घन, द्रव आणि वायुरूप अवस्था असताना विसरण प्रक्रियेतील स्थानांतरण वर वर्णन केलेल्या आणि तापमानावर अवलंबून असणाऱ्या अणूतील अंगभूत उर्जेवर आधारित असते. विसरणात होणारे स्थानांतरण आधिक संहतीकडून कमी संहतीकडे सर्व दिशांना होत असते आणि हव्या त्या दिशेकडे विसरण रूपाने जाणारा विसरण प्रवाह मोजता येतो.
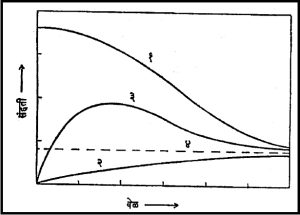
वायू अवस्थेतील विसरण : वायूमंधील अणूंची अंगभूत गती वायूच्या तापमानावर अवलंबून असते. तापमान वाढले की गती वाढते. वायूमध्ये असलेल्या सर्व अणूंच्या आपापसात सतत टकरा होत असतात. एका टकरीनंतर दुसरी टक्कर व्हावयाच्या आधी सरासरीने अणू किती अंतर चालून जाईल हे तापमानाच्या सम प्रमाणात आणि दाबाच्या व्यस्त प्रमाणावर अवलंबून असते या अंतराला ‘माध्यमुक्त पथ’ (मुक्त संचार सरासरी अंतर) असे म्हणतात. या टकरांच्या योगाने सर्व अणू दिशांना गतिमान असतात. परिणामतः द्रव्यमान प्रवाह शून्य असतो म्हणजे वायुमिश्रणाचे प्रत्यक्ष स्थानांतरण होत नाही. या टकरांमुळे सर्व दिशांना मिळणारी गती हीच वायू अवस्थेतील विसरण प्रक्रियेस कारणीभूत आहे. वाफ झालेले सुगंधी द्रव्य याच नियमानुसार खोलीभर पसरते. वाफ स्थितीत सुगंधाचे अणू मुक्त असतात. हवेच्या इतर अणूंबरोबर त्यांच्या टकरा सुरू होतात. यामुळे काही अणू पुढील दिशेने, तर काही उलट दिशेनेही फेकले जातात. या सर्व हालचालींमध्ये पुढे जाणाऱ्या अणूंची संख्या मागे येणाऱ्या अणूंच्या संख्येपेक्षा जास्त आसते. परिणामी ते अणू मूळ जागेपासून दूर दूर जाऊ लागतात अशी स्थिती फार काळ टिकली म्हणजे मागे फिरणाऱ्या अणूंची संख्याही वाढत जाते. असे होता होता सर्व खोलीभर कालांतराने अशी स्थिती प्राप्त होते की, कुठल्याही दिशेने पुढे जाणाऱ्या आणि मागे येणाऱ्या अणूंची संख्या सर्व ठिकाणी सारखी होते. अशा संतुलित स्थितीमध्ये सर्व खोलीभर सुगंधी द्रव्याची संहती सारखी असते. अर्थात अशा वेळी मूळचे द्रव अगर घन अवस्थेतील सुगंधी द्रव्य पूर्णपणे उडून गेलेले असेल. अशा बंद खोलीत सुगंधी द्रव्याची मूळच्या अ जागेजवळील संहती, विरूद्ध टोकाच्या ब ठिकाणची संहती आणि आधल्यामधल्या क या ठिकाणची संहती कालमानाप्रमाणे कशी बदलत जाऊ शकेल याचा आलेख आ. १ मध्ये दाखविला आहे.
कालांतराणे समप्रमाणात पसरलेली संहती ‘४’ या तुटक रेषेने दाखवली आहे ‘४’ स्थिती प्राप्त होण्यास दीर्घकाल लागण्याची शक्यता आहे.
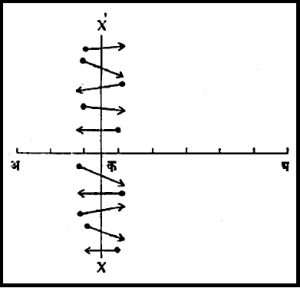
अशाच प्रकारची प्रक्रिया दोन निरनिराळे वायू अगर घटकांची असमान संहती असलेली वायूमिश्रणे एकमेकांच्या सानिध्यात आली म्हणजे घडते. बाह्य शक्तीच्या मदती शिवाय त्यांचे समान संहतीचे मिश्रण विसरण प्रक्रियेने घडते. विसरणाचा वेग अणूंच्या माध्य मुक्त पथावर अवलंबून असतो. वायुमिश्रणात एका घटकाच्या जास्त सहंतीच्या ठिकाणापासून कमी संहतीच्या ठिकाणाकडे सरकणाऱ्या अणूंची संख्या उलट दिशेने मागे फिरणाऱ्या अणूंच्या संख्येपेक्षा जास्त असते. म्हणजेच जास्त संहतीच्या क्षेत्राकडून कमी संहतीच्या क्षेत्राकडे त्या घटकाचा विसरण प्रवाह सुरू झाला असे समजता येईल. वस्तूतः हा प्रवाह नळामधील प्रवाहप्रमाणे एकाच दिशेला धावणाऱ्या अणूंचा नसून आपल्याला अभिप्रेत असलेल्या दिशेच्या त्या विवक्षित ठिकाणी काटकोन करून असणाऱ्या पातळीच्या पुढच्या बाजूकडे सरकणाऱ्या आणि मागच्या बाजूकडे सरकणाऱ्या अणूंच्या वजाबाकी इतका असतो. आ. २ मध्ये ही कल्पना स्पष्ट केली आहे. अ पासून ब कडे जाणारा क ठिकाणचा विसरण प्रवाह क या ठिकाणी असलेल्या X.X’ या काटकोन करणाऱ्या काल्पनिक पातळीतून ब च्या बाजूला किती अणू जात आहेत आणि अ च्या बाजूस किती अणू फिरत आहेत यांच्या वजाबाकी इतका म्हणजे, सहा उणे चार बरोबर, दोन इतका आहे. यात लक्षात घेण्याची वस्तूस्थिती ही की X.X’ या काल्पनिक पातळीतून जाणाऱ्या अणूंची दिशा कुठलीही असू शकेल.
अशा तऱ्हेने विवक्षित दिशेला लंब दिशेत असणाऱ्या प्रतलाच्या एकक क्षेत्रफळातून प्रत्येक सेकंदाला त्या दिशेकडे पार करून जाणाऱ्या अणूंच्या नक्त (निव्वळ) संख्येने विसरण प्रवाह दर्शवितात. हा विसरण प्रवाह पहिल्या फिक नियमानुसार (ए फिक या जर्मन शास्त्रज्ञांच्या नावावरून पडलेले नाव) मांडलेल्या खालील समीकरणाने दाखविला जातो.
J = -D (dc/dx) …………….. (१)
(यात J = लंब प्रतलाच्या एकक क्षेत्रफळातून कमी संहतीच्या दिशने जाणारे नक्त अणू, (dc/dx) = संहतीचा अवकलांक आणि D = विसरण गुणांक आहे). समीकरणाच्या उजव्या बाजूचे ‘उणे’ चिन्ह प्रवाह जास्त संहतीकडून कमी संहतीकडे जातो असे दाखवते. हे समीकरण मांडताना दोन संहतींमधील फरक बदलत नाही. आणि (dc/dx) हा अवकलांक स्थिर आहे, असे गृहित धरले आहे. याचा अर्थ असा की, संदर्भ प्रतलापासून जितके नक्त अणू पुढे जातील तितकेच अणू मागून येऊन त्या ठिकाणची जागा घेतील असे गृहित धरले आहे. अशा संतुलित अवस्थेत विसरण प्रवाह J हा सुद्धा अवचलित असेल.
पुढे गेलेल्या अणूंची जागा मागून येणारे अणू जर पूर्णपणे भरून काढीत नसतील, तर त्या ठिकाणची संहती हळूहळू कमी होईल. त्याचप्रमाणे पुढच्या ठिकणाची संहती हळूहळू वाढत जाऊ शकेल (जर तेथून पुढे निघून जात नसतील तर). यांतील एक अगर दोन्ही क्रियांचा परिणाम म्हणून dc/dx हा अवकलांक कालमानानुसार कमी होत जाईल. अशा परिस्थितीत एखाद्या ठिकाणच्या संहतीचे कालमानानुसार बदलणारे प्रमाण दुसऱ्या फिक नियमावर आधारलेल्या समीकरणाने खालीलप्रमाणे दाखविले जाते.
(dc/dt) = D (d2c/dx2) ……………….. (२)
[यात (dc/dt) = कालमानानुसार विशिष्ट ठिकाणी बदलत जाणाऱ्या संहतीचा (d2c/dx2) = बदलत जाणाऱ्या संहतीचा द्वितीय अवकलांक आणि D = संहतीनुसार न बदलणारा विसरण गुणांक आहे). तथापि जेव्हा विसरण गुणांक ‘D’ संहतीनुसार बदलत असतो, जेव्हा एखाद्या ठिकाणची कालमानानुसार बदललेली संहती ठरविताना D चे संहतीनुसार बदलत जाणारे प्रमाण विचारात घ्यावे लागते.
दोन वायूमिश्रणांमध्ये विसरण प्रवाह सुरू आहे आणि मागून येऊन पूर्णपणे भराव करणारे अणू अस्थित्वात नाहीत, अशा परिस्थित ‘अ’ आणि ‘ब’ या दोन काल्पनिक बिंदूच्या आणि त्यांच्यामध्ये असलेल्या सर्व ठिकाणांच्या बाबतीत कालमानाप्रमाणे संहतीमध्ये कसा बदल होत जाऊ शकेल ते आ. ३ मध्ये दाखविले आहे. X अक्षावर ‘अ’ पासून ‘ब’ पर्यंतचे अंतर दाखविले आहे.Y –अक्षावर संहती दाखवली आहे. dt = 0 हा आलेख विसरण प्रवाह सुरू होण्याच्या वेळेचा नसून प्रयोगाकरिता त्याचे मापन सुरू झालेल्या वेळेचा आहे . हा आलेख मापन सुरू करण्याच्या वेळी असलेली अ आणि ब यांमधील सर्व ठिकांणांची संहती दाखवतो. कालमापनाच्या dt =1, dt= 2, dt= 10 टप्यांचे आलेख आक़ृतीत दाखविलेले आहेत. बराच काळ लोटल्यानंतर सर्व ठिकाणाची संहती सारखी होईल. तो आलेख (dt= ∞) आ. १ मधील ‘४’ या आलेखासारखाच असेल. त्यावेळी विसरण प्रवाह बंद होईल. म्हणजेच कोणत्याही ठिकाणी ‘अ’ च्या अगर ‘ब’ च्या दिशेकडे जाणाऱ्या अणूंची संख्या सारखीच असेल अ आणि ब या बिंदूंमधील कुठल्याही ठिकाणची संहती dt= 0 पासून dt= ∞ पर्यंत कशी बदलत जाईल ते, त्या ठिकाणच्या X अक्षावर Y अक्षास समांतर रेषा काढून तिने निरनिराळ्या कालमानांच्या आलेखांना जे छेद दिले असतील , तेथील संहती लक्षात घेऊन एक नवा आलेख काढून त्यायोगे समजून घेता येईल. असे आलेख आ. १ मधील आलेखांसारखेच असतील.
वायूमध्ये होणाऱ्या विसरणाचे विसरण गुणांक त्या घटक वायूच्या अणुभारावर आणि आकारमानावर, म्हणजेच घनतेवर, अवलंबून असतात. ⇨ टॉमस ग्रॅहॅम यांच्या सिद्धांतानुसार हे प्रमाण खालील समीकरणाने दाखविले जाते.
(V1/V2) = √D2/√D1 …………(३)
(यात V1 आणि V2 = त्या त्या घटकांचे विसरणाचे वेग, D1 आणि D2 = त्या त्या घटकांच्या सापेक्ष घनता आहेत.)
विसरणाचा वेग घनतेच्या वर्गमुळाच्या व्यस्त प्रमाणात असतो. हायड्रोजनाची सापेक्ष घनता एक समजली, तर ऑक्सिजनाची सोळा होते. याचा अर्थ हायड्रोजनाचा विसरण वेग (समजा V1), ऑक्सिजनाच्या विसरण वेगापेक्षा (समजा V2) चौपट असतो.

निरनिराळ्या वायूंचे एकमेकांत मिसळण्याचे विसरण गुणांक मोजण्याकरिता आ.४ मध्ये दाखविलेले उपकरण वापरतात. या उपकरणात दोन उभ्या नळ्या (न. १ आणि न. २) एका तोटीद्वारे (त)जोडलेल्या असतात. खालच्या नळीत जड वायू भरतात व हालका वायू वरच्या नळीत ठेवतात. तोटीच्या छेदाचे क्षेत्रफळ नळ्यांच्याच आकारमानाचे असते. सर्व उपकरण समान तापमानाला ठेवतात. तोटी उघडताच विसरण प्रवाह सुरू होतात. वेळोवेळी नळ्यांमधून नमुने घेऊन घटक वायूंची संहती मोजतात आणि त्यावरून त्या घटकांचे त्या मिश्रणातील विसरण गुणांक निश्चित करतात.
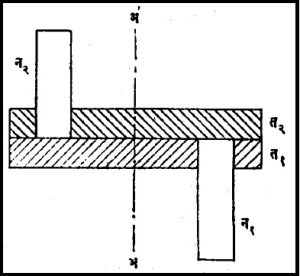 विसरण गुणांक मोजण्याकरिता वापरण्यात येणारे ओवर मायर यांचे उपकरण आ. ५ मध्ये दाखविले आहे. या उपकरणात अ-अ’ या आसाभोवती एकमेकांना चिटकून फिरणाऱ्या काचेच्या दोन तबगड्या असतात (त१ व त२) प्रत्येक तबगडीमध्ये एक नळी (न१आणि न२) बसविलेली असते. दोन्ही नळ्यांचे आकारमान सारखेच असते आणि तबकड्या फिरवून त्यांची तोंडे समोरासमोर आणता येतात. खालच्या नळीत जड वायू असतो आणि वरच्या नळीत हलका वायू ठेवतात. आसाभोवती तबकड्या फिरवून दोन्ही नळ्यांची तोंडे समोरासमोर आणली म्हणजे विसरण सुरू होते. नळ्यांमधील वायूंचे नमुने वेळोवेळी तपासून घटकांचे त्या मिश्रणातील विसरण गुणांक काढता येतात.
विसरण गुणांक मोजण्याकरिता वापरण्यात येणारे ओवर मायर यांचे उपकरण आ. ५ मध्ये दाखविले आहे. या उपकरणात अ-अ’ या आसाभोवती एकमेकांना चिटकून फिरणाऱ्या काचेच्या दोन तबगड्या असतात (त१ व त२) प्रत्येक तबगडीमध्ये एक नळी (न१आणि न२) बसविलेली असते. दोन्ही नळ्यांचे आकारमान सारखेच असते आणि तबकड्या फिरवून त्यांची तोंडे समोरासमोर आणता येतात. खालच्या नळीत जड वायू असतो आणि वरच्या नळीत हलका वायू ठेवतात. आसाभोवती तबकड्या फिरवून दोन्ही नळ्यांची तोंडे समोरासमोर आणली म्हणजे विसरण सुरू होते. नळ्यांमधील वायूंचे नमुने वेळोवेळी तपासून घटकांचे त्या मिश्रणातील विसरण गुणांक काढता येतात.
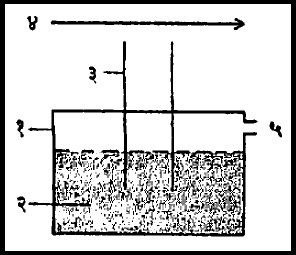
दोन्ही बाजूंनी उघडी तोंडे असलेली नलिका उडून जाणाऱ्या एखाद्या द्रवाच्या पात्रात उभी अर्धवट बुडविली आणि वरच्या तोंडाजवळून ईप्सित वायूचा प्रवाह जाऊ दिला, तर संतुलित अवस्था प्राप्त होऊन पात्रातील उडून गेलेल्या द्रवाचे प्रमाण पाहून त्या द्रवाच्या वाफेचा त्या ईप्सित वायूमधील विसरण गुणांक काढता येतो. आ. ६ मध्ये अशा तऱ्हेचे उपकरण दाखविले आहे.
वायूतील विसरण गुणांक तापमानाच्या सम प्रमाणात आणि दाबाच्या व्यस्त प्रमाणात बदलतो. वायूतील विसरण गुणांक मोजताना करावयाच्या प्रयोगात वायू ढवळला जाणार नाही याची काळजी घ्यावी लागते. सर्व उपकरण समान दाबाखाली आणि समान तापमानाला ठेवणे अवश्यक असते.
वायूंमध्ये विसरणाचे प्रमाण साधारपणे १·० ते ०·१ सेंमी २ से या दरम्यान असते. याचा अर्थ वायूचे अणू विसरण पद्धतीने दर सेकंदास ०·१ ते १·० सेंमी च्या दरम्यान इतस्ततः विखुरले जातात.
द्रव अवस्थेतील विसरणः द्रव अवस्थेमध्ये पदार्थाचे अणू काही प्रमाणात एकमेकांशी बांधलेले असतात. वायू अवस्थेप्रमाणे प्रत्येक अणू मुक्त संचार करू शकत नाही. परंतु अणूंची हालचाल आणि प्रवाहीपणा ठराविक मर्यादेत असतो. अणूंची गती वायू अवस्थेमधील अणूंपेक्षा कमी असते.इतस्ततः संचार करीत असताना प्रवाहीपणा बरोबरच वायूप्रमाणे, त्याच अवस्थेतील इतर अणूंशी त्यांच्या टकरा होतच असतात. माध्य मुक्त पथ अत्यंत कमी असतो. सर्व अणूनां एकत्र जवळजवळ ठेवणारे बल प्रभावी असते. म्हणून द्रव अवस्थेस पदार्थाचे आकारमान विवक्षित राहते. द्रव अवस्थेतील मर्यादित प्रमाणात उपलब्ध असलेल्या अंगभूत गतीमुळे त्यात मिसळू शकेल असा दुसरा पदार्थ त्याच्या सान्निध्यात आला की, त्यांचे एकमेकांत विसरण सुरू होते. द्रव पदार्थात मिसळणारा घन पदार्थ
द्रवाच्या सान्निध्यात आला तरी तसाच प्रकार अनुभवास येतो. सुगंधी पदार्थाच्या संदर्भात त्याची वाफ होऊन हवेत मिसळते, तर मिठाच्या खड्याच्या संदर्भात त्याच्या पृष्ठभागाशी मिठाचा विद्राव तयार होऊन त्यातील आयन (विद्युत् भारित आणू वा रेणू ) वायू अवस्थेतील अणूंप्रमाणे प्रवाही स्वरूपात सर्व द्रवात सम प्रमाणात विसरण प्रक्रियेने मिसळतात. ⇨कलिल स्वरूपामधील घटकसुद्धा त्यांच्या प्रवाहीपणामुळे ते मिसळू शकत असणाऱ्या द्रवात विखुरले जाऊ शकतात. द्रवाला पृष्ठभाग असतो. आणि निसर्गतःच एकमेकांत मिसळले जाणाऱ्या द्रव अगर घन पदार्थाचेच ईप्सित विसरण होऊ शकते. वायू अवस्थेतील विसरण आणि द्रव अवस्थेतील विसरण यांत हा महत्वाचा फरक आहे. सर्व वायू मुक्त संचार गुणधर्मामुळे सर्व द्रव एकमेकांत मिसळू शकत नाहीत गुणधर्म जुळणारे द्रव किंवा घन पदार्थ विवक्षित द्रवात मिसळू शकतात.
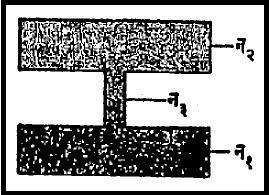
द्रवातील विसरण गुणांक मोजण्याची उपकरणे साधारणपणे वायूतील विसरण गुणांक मोजण्याच्या उपकरणांसारखीच असतात. त्यापैकी एक उपकरण आ. ७ मध्ये दाखविले आहे. यात न १ आणि न २ ही मोठ्या आकारमानाची पात्रे न ३ या सूक्ष्म नलिकेने जोडलेली आहेत. ज्या घटकाचा द्रवातील विसरण गुणांक मोजावयचा असेल, त्या द्रवाच्या जास्त संहतीचा विद्राव खालच्या पात्रात (न१ मध्ये ) ठेवतात आणि कमी संहतीचा विद्राव वरच्या पात्रात (न२ मध्ये ठेवतात. सूक्ष्म नलिका न ३ मधून न१ पासून न२ कडे विसरण प्रवाह सुरू होतो. संतुलित गतीने विसरण सुरू झाल्यावर वेळोवेळी एका पात्रातील नमुने तपासून त्यायोगे न३ मधून होणारा एकूण विसरण प्रवाह मोजता येतो. त्याकरिता खालील समीकरण वापरतात.
J = S/Δt π r 2 …………… ( ४ )
(येथे J = एकक क्षेत्रफळातून वाहणार विसरण प्रवाह, S = विसरण झालेली घटकाची मात्रा, t= मापनाचा काल, π r 2= सूक्ष्म नलिकेच्या छेदाचे क्षेत्रफळ होय.)
विसरण प्रवाहाचे प्रमाण समजल्यानंतर पहिल्या फिक नियमानुसार मांडलेल्या समीकरण (१) चा वापर करून विसरण गुणांक मोजता येतो. ते समीकरण खालीलप्रमाणे आहे.
J = D (dc/dx)
(येथे J = समीकरण (४) अन्वेय मिळालेले विसरण प्रवाहाचे मूल्य, dc = न१ आणि न२ मधील संहतीतील फरक dx = न३ या सूक्ष्म नलिकेची लांबी होय).
या प्रयोगात फक्त न३ मधील विसरण प्रवाह मोजायचा असल्याने न१ आणि न२ पात्रांतील विद्राव ढवळत ठेवून त्या प्रत्येकामधील संहती समान ठेवली जाते.
द्रव पदार्थातील विसरण गुणांकाची मात्रा जर संहतीनुसार बदलत असेल, तर न१ आणि न२ मधील संहतीमध्ये अगदी थोडा फरक ठेवला जातो. अशा विद्रावांना दुसरा फिक नियम लागू होतो. न ३ या सूक्ष्म नलिकेतील विद्रावाची संहती बाहेरच्या बाहेर प्रकाश मापकांचा उपयोग करून त्यांच्याद्वारे नलिकेतील विद्रावाचे प्रकाश प्रणमन (वक्रीभवन) मोजून नलिकेतील विद्रावाला धक्का न लावता मोजता येते आणि त्यावरून त्या सूक्ष्म नलिकेतील dc/dx या अवकलकांचे मूल्य काढता येते.
द्रवातील विसरण गुणांक न३ या सूक्ष्म नलिकेऐवजी न१ आणि न२ या पात्रांमध्ये एक सच्छिद्र पडदा ठेवूनही मोजता येतो.
एखाद्या घटकाच्या विशिष्ट संहती विद्रवाने संपूर्ण दंडगोल (सिलिंडर) पूर्णपणे भरून तो दंडगोल विद्रावकाने (विरघळवणाऱ्या पदार्थाने) भरलेल्या मोठ्या पात्रात उभाच्या उभा पूर्ण बूडवून त्याचे तोंड विद्रवकाच्या पृष्ठभागाखाली राहील अशा रीतीने ठेवला म्हणजे दंडगोलाच्या मुखामधून त्या घटकाचे विद्रावकात विसरण सुरू होते. वेळोवेळी दंडगोलातील विद्रावाचे नमुने तपासून त्या घटकाचा त्या विद्रवातील विसरण गुणांक काढता येतो.
द्रव पदार्थात श्यानता आणि विसरण गुणांक यांचा घनिष्ठ संबंध असतो, कारण दोन्ही गुण द्रव्याच्या प्रवाहीपणावर अवलंबून असतात. या संबधीचे समीकरण खालील प्रमाणे मांडले जाते.
u = (1/6π ηr )……………..… ( ५ )
आणि D = u k T……………..… ( ६ )
[ यांत u =प्रवाहीपणा , r = अणूची त्रिज्या , η = श्यानता, k = एक स्थिरांक, T= निरपेक्ष तापमान (के.) साथ होय].द्रवातील विसरण श्यनतेच्या व्यस्त प्रमाणात असते. संहतीच्या प्रमाणात द्रवाचा प्रवाहीपणाही बदलतो आणि त्याचा विसरणावरही व्यस्त प्रमाणात परिणाम होतो. द्रवातील विसरणाचे प्रयोग करतेवेळी दोन द्रवातील पृष्टभाग स्थिर राहून इतर प्रक्रियांनी द्रव एकमेकांत मिसळले जाणार नाहीत याची काळजी घ्यावी लागते.
विसरण प्रक्रियेत प्रचलांमध्ये (विशिष्ट परिस्थितीत स्थीर मूल्य असणार्या चलांमध्ये म्हणजे बदलत्या राशीमध्ये) पडणारे फरक लक्षात घेऊन समीकरणामध्ये उचित बदल करावे लागतात. सर्वदिशीय विसरण एक दिशीय विसरण स्तंभातून अगर गोलकातून होणारे विसरण इत्यादींच्या निरनिराळ्या प्रचलांकरिता निरनिराळी समीकरणे मांडता येतात. बर्याच वेळा वायू अगर द्रव अवस्थेत फक्त विसरण प्रवाहच न उद्भवता संनयन (अभिसरण) अगर इतर द्रव्यमान प्रवाह निर्माण होऊ शकतात. अशा वेळी विवक्षित दिशेने निर्माण होणारा परिणामी प्रवाह हा द्रव्यमान प्रवाह व विसरण प्रवाह यांच्या एकूण बेरजेइतका असतो. द्रव अवस्थेतील विसरणाचा वेग वायूतील विसरणापेक्षा दहा हजार ते एक लक्ष पटीने कमी असतो.
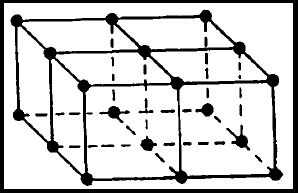
घन अवस्थेमधील विसरण : अगोदर सांगितल्याप्रमाणे, घन अवस्थेमध्ये अणूंना बांधून ठेवणारे बल खूप प्रभावी असते, या स्थितीत अणू प्रवाही नसतात. रांगोळीमधील टिपक्यांप्रमाणे एखाद्या विशिष्ट जालकामध्ये बंधांनी जखडून ठेवल्यासारखे अणू आपपाल्या जागी स्थिर असतात. अशा पिंजरारूपी जालकची काल्पनिक स्थिती आ. क्र. ८ मध्ये दाखविली आहे. या आकृत्तीमध्ये टिपक्यांच्या रूपाने अठरा अणू दाखविले आहेत व त्यांना जखडून ठेवणारे अद्शय बंध सरळ आणि तुटक रेषांनी दाखविले आहेत. अशा जालकांमध्ये निर्माण होणार्या अनियमितपणावर घन अवस्थेतील विसरण अवलंबून असते. घटकांचे अणू उडी मारून जालकात शिरून त्यात अनियमितपणामुळे निर्माण होणार्या जागा घेतात. अशा प्रकारे होणार्या विसरणाचे प्रमाण वायूमधील विसरणापेक्षा खूपच कमी म्हणजे सु. १०२० इतक्या सूक्ष्म प्रमाणात होत असते. घन अवस्थेतील जालकामध्ये एक सेंमी अंतर चालून जायाला घटकाच्या अणूस सु. दहा पर्व (१० ११ ) वर्ष लागतील. इतक्या सूक्ष्म प्रमाणात होणारे विसरण मोजणे केवळ अशक्यप्राय असते.
शून्य केल्व्हिन तापमानाला सर्व पदार्थाची जालके नियमित आणि परिपूर्ण असतात. अशावेळी विसरण घडत नाही. पदार्थाचे तापमान वाढत जाते तेव्हां कंपनांच्या स्वरूपात अणूमध्ये ऊर्जा साठवली जाते. वाढत्या तापमानामुळे जालकांमध्ये अनियमितपणा निर्माण होऊ लागतो. अशुद्धी स्वरूपात असलेले घटकसुद्धा घन अवस्थेमध्ये जालकात अनियमितपणे विखुरलेले असतात. तसाच प्रकार रसायनांमध्ये मिसळल्या गेलेल्या त्याच मुलद्रव्य़ाचा अन्य प्रकारच्या रसायनांच्या बाबतीत आढळून येतो. या अनियमितपणामुळे जालकांमध्ये भरल्या न गेलेल्या पोकळ्या तयार होतात.आणि विसरणास वाव मिळतो सिल्वहर आयोडाईडसारख्या रसायनात आयोडिनाचे (I) आयन नियमितपणे विखुरलेले आढळतात.तर चांदीचे (Ag) आयन अनियमितपणे विखुरलेले असतात. अशा परिस्थितीत स्थानांतरणास वाव मिळून विसरण होऊ शकते. जालकात मोकळी जागा असेल तर फक्त अजू बाजूचेच अणू ही जागा घेऊ शकतात. एकमेकाशेजारचे अणू आपआपल्या जागी बदलणे शक्य असते, पण वस्तुत तसे होताना दिसत नाही. शिशाच्या अनिकट सानिध्यात आल्यावर सोन्याचे अणू शिशाच्या जालकात प्रवेश करतात अशावेळी शिशाचे अणू आपली जागा सोडत नाहीत. त्याचे जालक स्थिर असते. सोन्याचे अणू शिशाच्या जालकातील मोकळ्या जादेत शिरतात.
मिश्रधातंमध्ये विद्युतप्रवाह सोडल्यास घटक धातुंचे आयन आपली जागा सोडतात. मिश्र विद्युत विच्छेद्य स्फटिकांमध्ये सर्व आयनांचा प्रवाहीपणा सारखा नसल्याने विसरण होण्यास योग्य परिस्थिती निर्माण होऊ शकते.
स्वयंविसरण : वायूतील आणि काही प्रमाणात द्रव अवस्थेतील अणू मुक्त असल्याने समान संहती, समान दाब आणि समान तापमान असलेल्या स्थितीत सुद्धा अंतर्गत विसरण सुरूच असते. फक्त कुठल्याही ठिकाणी कुठल्याही दिशेला परिणामी विसरण प्रवाह शुन्य असतो. इतकेच. अशा विसरणाचा गुणांक काढण्यासाठी समान अणूभार आणि समान अणूअकारमान असणारे वायू वापरतात. किरणोत्सर्गी (भेदक कण वा किरण बाहेर टाकणार्या) समस्थानिकांचा (अणुक्रमांक तोच पण अणूभार भिन्न असलेल्या त्याच मुलद्रव्याचा प्रकारांचा) वापर करूनही स्वंयविसरण गुणांक काढता येतो. स्वंयविसरण श्यानतेच्या व्यस्त प्रमाणात असते.
घन पदार्थ आणि वायू : घन पदार्थाच्या पृष्ठभागावरून त्याच्याशी रासानिक विक्रिया घडविणारा वायू वाहत असेल, तर त्या वायूतील घटक विसरण प्रक्रियेने घन पदार्थात मिसळू शकतात. लोखंडाच्या पृष्ठ भागावरून क्रोमियम क्लोराईड, हायड्रोजन व हायड्रोजन क्लोराईड हे वायू मिश्रण योग्य तापमानाला वाहत ठेवल्यास रासायनिक विक्रिया होऊन लोखंडाच्या पृष्ठ भागावर क्रोमियमच्या अणूंचा थर देता येतो.
धातू आणि वायू : धातूमध्ये वायूचे होणारे विसरण घटक वायूच्या त्या धातूमध्ये होणार्या शोषणावर आणि प्रवाहीपणावर अवलंबून असते. नैसर्गिक हायड्रोजनचे पॅलॅडियामामध्ये शोषण होते आणि शोषणानंतरसुद्धा त्याचा प्रवाहीपणा टिकून राहतो. इतर कुठल्याही वायूचे पॅलॅडियामामध्ये शोषण होत नाही. हायड़्रोजन वायू पॅलॅडियामाच्या पटलातू विसरण पद्धतीने मिश्रणातील इतर घटक वायूपासून अलगकरता येतो. नैसर्गिक हायड्रोजनामध्ये ड्यूटोरियम हा समस्थानिकही असतो.ड्यूटरियमची घनता हायड्रोजनच्या तुलनेत दुप्पट असते. समीकरण (३) प्रमाणे हायड्रोजनचे विसरण ड्यूटोरियमपेक्षा १.३१ पटीने अधिक वेगाने होते.या गुणधर्माचा उपयोग करून पॅलॅडियामची पटले वापरून नैसर्गिक हायड्रोजनपासून ड्यूटोरियम अलग करणे शक्य होते.
धातूंच्या पृष्ठभागावरील प्रक्रिया : लोखंडाच्या पृष्ठभागावर क्रोमियमचा थर देता येतो.याचा उल्लेख वर आलाच आहे . पुष्कळ धातूंची सर्वसाधारण तापमानालासुद्ध हवेतील ऑक्सिजन, क्लोरीन हायड्रोजन सल्फाईड, सल्फरडायऑक्साईड इ. वायूबरोबर रासायनिक विक्रिया होतेच. अशी विक्रिया झाल्यानंतर निर्माण होणाऱ्या. रसायनाची घनता जर जास्त असेल, तर त्याला कमी जागा लागते. परिणामी निर्माण होणार्या कणांच्या फटीमधून घातक वायू मोकळेपणाने आत शिरून आतल्या भागातील धातूवर विक्रिया करू शकतो. याउलट रसायनाची घनता कमी असेल तर त्याच्या कणांना जास्त जागा लागते आणि त्यामुळे सर्व कण एकमेकांना घट्टपणे चिकटतात. या प्रकारात त्या रसायनाचा धातूच्या पृष्ठभागावर दाट आणि घट्ट थर जमतो.अशा थरातून फक्त विसरण प्रक्रियेनेच वायू अतिल धातूपर्यंत पोहचू शकतो.पण घन थरातील विसरण क्रिया अत्यंत मंद वेगाने होत असल्यामुळे आतील बाजूचे संरक्षण होते.
लोखंडाचे गंजणे : लोखंड आणि ऑक्सिजन यांची विक्रिया होऊन उत्पन्न झालेल्या ऑक्साईडच्या थरातून लोखंडाचे अणू विसरण प्रक्रियेने प्रवास करून ऑक्सिजनच्या वरच्या अणूपर्यंत येऊन पोहचतातअसे आढळून आले आहे. त्यामुळे गंजण्याच्या विक्रियेला निसर्गत प्रतिबंध होत नाही. लोखंडामध्ये अल्प प्रमाणात खालच्या वर्गातील धातू मिसळल्या तर त्यांच्या पृष्ठभागावर ऑक्साईडचा घट्ट थर जमा होण्यास मदत होते व गंजण्याच्या प्रक्रियेस प्रतिबंध होतो. लोखंडात अल्प प्रमाणात मिसळलेल्या ऑल्यूमिनियम, सिलिकॉन क्रोमियम इत्यादींच्या ऑक्साईडचे असे घट्ट थर तयार होतात. लोखंडात अल्प प्रमाणात मॅग्नेशियम किंवा जस्त या धातू मिसळलेल्या असतील, तर त्यांचे अणू पृष्टभागाशी तयार झालेल्या ऑक्साईडच्या थरातून विसरण प्रक्रियेने वर जातात आणि संरक्षक थर तयार होतो., असे आढळून आले आहे.[ → गंजणे ].
अर्धपार्य पटले : सेंद्रिय (जैव) अर्धपार्य पटलात सूक्ष्म छेदाच्या आरपार नलिका असतात. त्यांच्या छेदाचा व्यास वायूतील अणूंच्या माध्य मुक्त पथाच्या जवळपास असतो.अशा नलिकातून वायू इकडून तिकडे जात असताना द्रव्यमान प्रवाहपेक्षा टकरा खात जाणारा विसरण प्रवाहक जास्त महत्वाचा ठरतो.वायूची विसरणक्षमता त्याच्या अणूभाराच्या व्यस्त प्रमाणात असते. एखादे वायू मिश्रण जर अशा अर्धपार्य पटलातून आरपार जाऊ दिले तर पटलातून पलीकडे जाणार्यावायूत लाहान अणूभाराच्या वायूचे प्रमाण मिश्रणातील इतर घटकांपेक्षा जास्त असते.अशा प्रकारे अर्धपार्य पटलांचा उपयोग करून विसरण प्रक्रियेने वायूमिश्रणातील हलका वायू अलग करणे शक्य होते.[ →तर्षण].
नैसर्गिक युरेनियामध्ये फक्त ०·०७ टक्के मंजनक्षम युरेनियम (२३५) हा घटक असतो.तो घटक अशा अर्धपार्य पटलांचा वापर करून पाहिजे असेल तितक्या प्रमाणात अलग करता येतो. बाष्पीभवन होणारे युरेनियम फ्ल्युओराईड(UF6) हे रसायन वापरतात. एका टप्प्यात फक्त १·००४२९ इतक्या प्रमाणात युरेनियम (२३५) चे प्रमाण वाढण्याकरिता एकामोगोमागएक असे हजारो टप्पे अंतर्भुत केलेली संयंत्रे उपयोगात आणावी लागतात. युरेनियमच्या अशा संपन्नीकरणाची अधिक माहिती युरेनियम व अणूकेंद्रीय अभियांत्रिकी या लेखात दिलेली आहे.
खाणीतील धोकासूचक यंत्रणा : अर्धपार्य पटलांचा उपयोग करून दगडी कोळशाच्या खाणीतील धोकादायक मिथेन वायूचे अस्थित्व दर्शवून धोक्याची सूचना देणारे उपकरण विकसित केलेले आहे. या उपकरणाच्या तोंडाशी विशिष्ट तर्हेचे अर्धपार्य पटल बसविलेले असते. अतिल बाजूस उपकरणाच्या कुपीमधील हवेचा दाब दाखविणारा पार्चा वायूदाबमापक असतो. या विशिष्ट अर्धपार्य पटलातून फक्त मिथेन वायू जमा होऊ लागला म्हणजे विसरण प्रक्रियेने तो उपकरणाच्या कुपीत जातो. आतील हवा पटलातून बाहेर पडू शकत नाही.परिणामी कुपीमधील दाब वाढतो. वाढलेल्या दाबामुळे वायू दाबमापकातील पार्याची पातळी चढते.आणि उपकरणात बसविलेल्या विद्युत मंडलाच्या साहाय्याने धोक्याची सूचना दिली जाते. [ → धोकासूचक, विद्युत् ].
खनिजे : झिओलाईट नावाच्या खजिनांच्या स्फटिकाजलात समांतर स्तररचना (पत्रण) आढळून येते. अशा खजिनांमध्ये अशा स्तरांच्या समांतर दिशेने होणारे विसरण त्या स्तरांच्या आरपार जाणार्या विसरणाच्या प्रवाहपेक्षा हजारो पट अधिक असते, असे आढळून आले आहे.
प्रचल : निरनिराळ्या प्रचलांचे निरनिराळे परिणाम विसरण प्रक्रियेवर उमटत असतात. याची काही उदाहऱणे पुढे् दिली आहेत.
दाब : वायूमिश्रणात दोन ठिकणी भिन्न दाब निर्माण होऊन दाब क्रमिकता निर्माण झाली, तर विसरण प्रवाह सुरू होऊन हलका घटक कमी दाबाच्या दिशेकडे अधिक प्रमाणात जमा होतो.
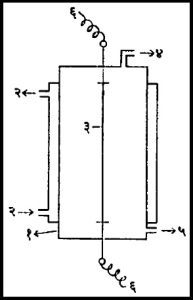
तापमान : वायूमिश्रण किंवा द्रवमिश्रण यात दोन ठिकाणाच्या तापमानात फरक असेल तर तापमान क्रमिकता तयार होऊन विसरण विसरण प्रवाह सुरू होतो. आणि काही प्रमाणात घटकांचे अलगीकरण होते. वायूमिश्रणातील हलका वायू उच्च तापमानच्या ठिकाणाकडे अधिक प्रमाणात जमा होतो. प्रत्येक्षात होणारे अलगीकरणाचे प्रमाण घटकांच्या अणूभारतील फरकावर अवलंबून असते. आणि हे प्रमाण हे प्रमाण अत्याल्प असते, निऑन (२०) आणि निऑन (२२) यांचे अलगीकरण एका टप्प्यात १·०१६५ इतक्याच प्रमाणात होते हायड्रोजन आणि ड्यूटेरिअम यांच्या अलगीकरणाचे प्रमाण साधारण १·१७२८ इतके असते. या तत्वाचा उपयोग करून क्लूशिअस नलिका बनवलेली आहे. अशी नलिका आ. ९ मध्ये दाखविली आहे. या उपकरणात एक उभी नलिका असते.या नलिकेच्या बाहेरील बाजूस पाणी किंवा इतर द्रव खेळता ठेवून नलिकेची भिंतविशिष्ट तापमानाला थंड ठेवण्याची व्यवस्था असते. नलिकेमध्ये मध्येभागी खालपासून वरपर्यंत धातूची एक विद्युत रोधक तार बसवलेली असते. नलिकेत वायूमिश्रण भरून ठेवलेले असते. प्रयोग सुरू करतेवेळी मधल्या तारेत विद्युत प्रवाह खेळवून तीठराविक उच्च तापमानाला कायम ठेवली जाते. बाहेरील भिंत थंड असते त्यामुळे मध्यापासून भिंतीपर्यंत तापमान क्रमिकता तयार होते. आणि विसरण प्रवाह सुरू होतो. हलका अणूभार असलेला घटक अधिक प्रमाणात मधल्या तारेकडे जाऊ लागतो. तसाच जड अणूभाराचा घटक अधिक प्रमाणात भिंतीकडे जाऊ लागतो. याच वेळी भिंतीजवळ वरून खाली आणि मधल्या गरम तारेजावळ खालून वरच्या अंगाकडे संनयन प्रवाह एकमेकास पूरक असतात. दोन्ही प्रवाहांच्या एकूण परिणामामुळे हलका घटक मध्यभागीअसलेल्या तारेच्या वरच्या अंगाकडे जमा होऊ लागतो. आणि जड घटक भिंतीच्या बाजूने खालील अंगास जमा होऊ लागतो. ही प्रक्रिया बराच वेळ चालू ठेवली म्हणजे अलगीकरणचे हजारो टप्पे केवळ एकाच नलिकेत पार पाडता येतात.या नलिकेचा उपयोग करून निऑन (२०) आणि निऑन (२२) असे अगदी जवळ जवळ सारखेच अणूभार असलेले घटकसुद्घ सुद्धा रूपात अलग करता येतात. या नलिकेचा युरेनियम (२३५) पाहिजे तितक्या शुद्ध स्वरूपात मिळविण्याकरिता उपयोग करता येतो.
तांत्रिक प्रक्रिया : रसायन तंत्रविद्येतील द्रव्यमान स्थानांतरणाच्या क्षेत्रात विसरण प्रक्रियेसफार मोठे महत्व प्राप्त झाले आहे. ⇨ बाष्पीकरण, ⇨ऊर्ध्वपातन, ⇨निष्कर्षण, ⇨ शुष्कीकरण, ⇨ वायुशोषन, ⇨ उत्प्रेरण इ. प्रक्रियांमध्ये द्रव्यमान एका अवस्थेतून दुसर्या अवस्थेत जात असताना पृष्टभागाशी कल्पिलेल्या पटलातून त्या घटकास जावे लागते. त्या विविक्षित घटकाच्या अशा पटलातून जाणार्या विसरण विसरण प्रवाहावर पुष्कळ वेळा संयंत्राची कार्य पद्धति अवलंबून असते. अशा परिस्थित संयंत्रणाचे अभिकल्प (आराखडे) तयार करताना त्या विवक्षित घटकाच्या अशा पटलांतील विसरण गुणांची संपूर्ण माहिती असणे अवश्यक ठरते.
इतर घडामोडी : यांखेरीज रोजच्या व्यवाहारात दिसणार्या अनेक घडामोडी विसरण प्रक्रियेवर अवलंबून असतात असे आढळून येईल. उदा स्नायूमध्ये टोचलेले औषध विसरण प्रक्रियेने रक्तात मिसळते. काकडी, कैरी इ. अनेक वनस्पतिनां मीठ लावल्यास त्यांच्यातून पाणी बाहेर येते हाताच्या पंजावर मीठ धरून ठेवले तरी तोच अनुभव येतो. शीतपेटीत खालच्या कप्प्यातील वस्तू सुकत जातात आणि वरच्या पेटीत बर्फाचा थर जमतो. उन्हात धान्य वाळविणे इ. अनेक प्रक्रिया विसरणावर अवलंबून असतात.
पहा : अपोहन, आयन- विनिमय, तर्पण, ब्राऊनीय, गति, रेडिओ रसायनशास्त्र, वनस्पतिचे खनिज पोषण.
संदर्भ : 1. Cunningham, R F. , Williams, R J Dffitusion in Gases and Porous Media London, 1980.
2.Cusster, E.L. Diffusion : Mass Transfer In fluid Systems. New York 1985.
3. Edwards, D.K. and others Transfer Processes London 1979.
4. Gebhart, B. Heat Conduction and mass Diffusion New Yark. 1993.
5. Just, W Diffusion in Solids, Liquids and and Gases, New York, 1955.
6. Murch , G Ed. Diffusion in Solides : Unsolved Problems, New York, 1972
7. Philibert,J.Atom Movements : Diffusion and mass Transfer in Solids, 1991.
8. Rossiter, B W., Hamilton. J.F ., Eds, Physical Methods of Chemistry, Vol.6, 1992.
जोशी, गं. कृ.; दीक्षित, व. चिं.