रंगद्रव्ये : (पिगमेंट्स). रंगद्रव्य हा ⇨ रंगलेपाचा एक प्रमुख घटक असून ज्या विशिष्ट रंगद्रव्याचा उपयोग केलेला असेल त्यावर रंगलेपाचे प्रकाशीय व इतर मुख्य गुणदोष अवलंबून असतात. त्यामुळे रंगलेप तयार करण्यापूर्वी रंगद्रव्याच्या सर्व गुणधर्मांची सविस्तर माहिती असणे आवश्यक आहे. रंगद्रव्याची व्याख्या साधारणपणे स्वतःचा एक अपारदर्शक रंग असलेला, अतिसूक्ष्म कणांच्या रूपात असलेला व रंगलेपाकरिता वापरण्यात येणाऱ्या वाहक द्रव्य पदार्थात अविद्राव्य (न विरघळणारा) असणारा घन पदार्थ अशी करण्यात येते. वाहक वाळल्यानंतर एक पटल तयार होऊन रंगद्रव्याचे कण त्यात एका पातळीत बांधले जाऊन पृष्ठभागाला रंग प्राप्त होतो. रंगद्रव्याची व्याख्या यापेक्षा जास्त व्यापक आहे. कारण पृष्ठलेपामध्ये वाहक हा शुष्कन तेल किंवा संश्लेषित (कृत्रिम रीत्या बनविलेले) रेझीन असू शकतो. जसे टिटॅनियम डाय-ऑक्साइड हे तेल, संश्लेषित रेझीन, नायट्रोसेल्युलोज किंवा ⇨ प्लॅस्टिकीकारक यांमध्ये विद्राव्य असल्यामुळे रंगलेप पटलामध्ये त्यांचा रंगद्रव्य गुणधर्म मिळतो. पाण्यात अविद्राव्य असणारे पदार्थ म्हणजे रंगद्रव्य अशी व्याख्या चुकीची ठरते, कारण काही कार्बनी पदार्थ पाण्यात अविद्राव्य पण तेलात विद्राव्य असतात व त्यामुळे रंजकद्रव्ये म्हणून वापरले जातात. त्याचप्रमाणे वस्त्रांच्या रंजनक्रियेत वापरली जाणारी काही रंजकद्रव्ये पाण्यात अविद्राव्य पण तेल, नायट्रोसेल्युलोज इ. जलेतर माध्यमांत विद्राव्य असतात व त्यामुळे त्यांचा उपयोग रंगद्रव्य म्हणून केला जातो. याशिवाय काही रंगीत पदार्थ असेही आहेत की, ज्या द्रव्यांत ते विद्राव्य असतात त्यात पटल निर्माण करणारा पदार्थही विद्राव्य असतो आणि ज्या वेळी या विद्रावाचे बाष्पीभवन होऊन पटल तयार होते त्या वेळी रंगीत पदार्थ हा रंगद्रव्य म्हणून काम करतो.
रंगद्रव्यांच्या अविद्राव्यता गुणधर्मामुळे त्यांचा वापर रंगलेप, छपाईची शाई इ. पृष्ठलेपांत किंवा प्लॅस्टिके, रबर, काँक्रीट यांसारख्या मोठ्या प्रमाणावर रंग लागणाऱ्या पदार्थांमध्ये केला जातो. रंगद्रव्यांमुळे रंगलेपास रंगछटा, अपारदर्शकता, पसरणे यांसारखे विशिष्ट गुणधर्म प्राप्त होतात. तसेच प्रकाश, अम्ल, क्षार (अल्कली), विद्रावक (विरघळविणारे पदार्थ) यांपासून रंगलेपाचे संरक्षण होण्यास रंगद्रव्याचा महत्त्वाचा वाटा असून वरील प्रत्येक गुणधर्म रंगलेपाच्या पटलाच्या उपयुक्त आयुष्याशी निगडित आहे. रंगद्रव्याच्या रासायनिक संघटनाचाही रंगलेपाच्या उपयुक्त आयुष्यावर फारच महत्त्वाचा परिणाम होतो, कारण प्रत्यक्ष वापरात रंगलेपाचा इतर (रासायनिक व अरासायनिक) पदार्थांशी संबंध येतो त्या वेळी रासायनिक विक्रिया झाल्यास रंगलेपाचा नाश होऊन तो निरुपयोगी ठरतो. जसे प्रशियन ब्ल्यूची क्षारामुळे, कॅडमियम सल्फाइडाची अम्लामुळे झिंक ऑक्साइडाची उच्च अम्लता तुल्य असलेल्या माध्यमात विनाशक रासायनिक विक्रिया होते. याव्यतिरिक्त रंगद्रव्याच्या रासायनिक संघटनाचा त्याच्या विद्राव्यता, प्रणमनांक (प्रकाशाचा निर्वातातील वेग व निर्दिष्ट माध्यमातील वेग यांचे गुणोत्तर), रंगछटा व विशिष्ट गुरुत्व या अंगभूत गुणधर्मांवर परिणाम होतो. या सर्व गोष्टी लक्षात घेता रंगद्रव्याची वाहकातील बंधकात एकजीव होण्याची क्षमता अशी पाहिजे की, (१) निर्माण होणारा रंगलेप काही ठराविक आकारमानाच्या कणांपासून मुक्त असावा (२) काही ठराविक वेळेपर्यंत खराब न होता रंगलेप साठविता यावा (३) समाधानकारकपणे रंगलेप लावता यावा (४) कमीत कमी प्रक्रिया कराव्या लागाव्यात. जर रंगद्रव्य पाण्यात वापरावयाचे असेल, तर रंगद्रव्याचे पाण्यातील अर्ध-मऊ मिश्रण (पेस्ट) चटदिशी वापरण्यास योग्य असते किंवा पाण्याशिवाय वापरावयाचे असेल, तर कोरड्या चूर्णरूपात जास्त उपयुक्त ठरते परंतु गेल्या कित्येक वर्षांपासून रंगद्रव्य तेल वाहकांमध्ये अगोदरच विखरून विक्री करण्याची प्रवृत्ती वाढत आहे. यामुळे एकच रंगद्रव्य बाजारात निरनिराळ्या अवस्थांत उपलब्ध असू शकते.
रंगलेप हा मुख्यतः रंगद्रव्याचे द्रव वाहकात विखुरलेले रूप असते व त्यामुळे त्याचे बरेच उपयुक्त गुणधर्म दोन्ही घटकांच्या भौतिक व रासायनिक गुणधर्मांवर अवलंबून असतात.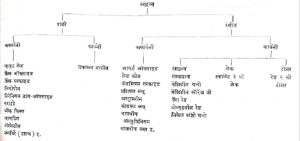 रंगलेपाचे वापरण्याचे गुणधर्म व स्थैर्य यांवर रंगद्रव्याच्या गुणधर्माचा परिणाम होतोच पण त्याचा मोठा वाटा रंगलेपास रंगछटा व अपारदर्शकता (कृष्ण-धवल भेद दिसेनासा करण्याची क्षमता) देण्यात येते. रंगद्रव्याने केलेले प्रकाशाचे परावर्तन, प्रणमन (एका माध्यमातून दुसऱ्या माध्यमात शिरताना होणारा दिशेतील बदल) व शोषण हे मूलभूत गुणधर्म अपारदर्शकतेशी निगडित आहेत. विवेचक (काही विशिष्ट निवडक तरंगलांब्यांच्या प्रकाशाच्या बाबतीत होणारे) शोषण हे रंगछटेशी निगडित आहे. पदार्थाची रंगछटा त्याच्या रासायनिक संघटनावर म्हणजे पदार्थातील मूळ अणू कोणते व ते एकमेकांना कसे जोडले गेले आहेत यांवर अवलंबून असते. प्रकाशाचे शोषण हे पदार्थातील अणू व रेणू यांच्या इलेक्ट्रॉनीकीय व अणुकेंद्रीय संघटनानुसार होते. शोषण कोणत्या तरंगलांबीच्या प्रकाशाचे होते, हे त्या रंगद्रव्याच्या संरचनेवर अवलंबून असते. कार्बनी रसायनशास्त्रात काही प्रकारच्या आणवीय विन्यासांमुळे (मांडण्यांमुळे) दृश्य रंग येतो. त्यांना क्रोमोफोर म्हणतात. रंगछटा ही त्या एकंदर रेणूची संरचना तसेच काही विशिष्ट अणुगटांच्या उपस्थितीमुळे बदलू शकते. अशा गटांना ऑक्सोक्रोम म्हणतात व त्यांमुळे मूळ रंगछटा दाट होते. –C=C– –C=O –C=N –N=O ही क्रोमोफोरांची काही उदाहरणे होत. ॲमिनो –NH2, हायड्रॉक्सी –OH, नायट्रो –NO3, अल्किल–CH3, हॅलोजन (साधारणपणे) –Cl ही ऑक्सोक्रोमांची उदाहरणे आहेत.
रंगलेपाचे वापरण्याचे गुणधर्म व स्थैर्य यांवर रंगद्रव्याच्या गुणधर्माचा परिणाम होतोच पण त्याचा मोठा वाटा रंगलेपास रंगछटा व अपारदर्शकता (कृष्ण-धवल भेद दिसेनासा करण्याची क्षमता) देण्यात येते. रंगद्रव्याने केलेले प्रकाशाचे परावर्तन, प्रणमन (एका माध्यमातून दुसऱ्या माध्यमात शिरताना होणारा दिशेतील बदल) व शोषण हे मूलभूत गुणधर्म अपारदर्शकतेशी निगडित आहेत. विवेचक (काही विशिष्ट निवडक तरंगलांब्यांच्या प्रकाशाच्या बाबतीत होणारे) शोषण हे रंगछटेशी निगडित आहे. पदार्थाची रंगछटा त्याच्या रासायनिक संघटनावर म्हणजे पदार्थातील मूळ अणू कोणते व ते एकमेकांना कसे जोडले गेले आहेत यांवर अवलंबून असते. प्रकाशाचे शोषण हे पदार्थातील अणू व रेणू यांच्या इलेक्ट्रॉनीकीय व अणुकेंद्रीय संघटनानुसार होते. शोषण कोणत्या तरंगलांबीच्या प्रकाशाचे होते, हे त्या रंगद्रव्याच्या संरचनेवर अवलंबून असते. कार्बनी रसायनशास्त्रात काही प्रकारच्या आणवीय विन्यासांमुळे (मांडण्यांमुळे) दृश्य रंग येतो. त्यांना क्रोमोफोर म्हणतात. रंगछटा ही त्या एकंदर रेणूची संरचना तसेच काही विशिष्ट अणुगटांच्या उपस्थितीमुळे बदलू शकते. अशा गटांना ऑक्सोक्रोम म्हणतात व त्यांमुळे मूळ रंगछटा दाट होते. –C=C– –C=O –C=N –N=O ही क्रोमोफोरांची काही उदाहरणे होत. ॲमिनो –NH2, हायड्रॉक्सी –OH, नायट्रो –NO3, अल्किल–CH3, हॅलोजन (साधारणपणे) –Cl ही ऑक्सोक्रोमांची उदाहरणे आहेत.
वर्गीकरण : रंगद्रव्यांचे वर्गीकरण करण्याची एक सर्वमान्य पद्धत वर दर्शविली आहे.
याशिवाय रंगद्रव्यांचे संश्लेषित व नैसर्गिक (किंवा खनिज) असेही वर्गीकरण काही वेळा करण्यात येते. काही महत्त्वाच्या रंगद्रव्यांची माहिती खाली दिलेली आहे.
पांढरी रंगद्रव्ये : यांत निरनिराळ्या खनिज व संश्लेषित रंगद्रव्यांचा समावेश होतो. ही रंगद्रव्ये मूळ रूपात व इतर रंगछटा कमीजास्त करण्यासाठी वापरली जात असल्याने त्यांचे उत्पादन व खप खूप मोठ्या प्रमाणात होतो.
टिटॅनियम डाय-ऑक्साइड : हे मुख्यतः ⇨ इल्मेनाइट या धातुकापासून (धातुयुक्त खनिजांपासून) बनविले जाते. याचे रा. सं. FeO. TiO2 असून निरनिराळ्या ठिकाणी सापडणाऱ्या निक्षेपांत (साठ्यांत) टिटॅनियम डाय-ऑक्साइडाचे प्रमाण ३५% ते ६०% इतके बदललेले आढळते. निसर्गात टिटॅनियम डाय-ऑक्साइड ⇨ ॲनॅटेज, ⇨ रूटाइल व ⇨ ब्रुकाइट या तीन रूपांत आढळते. त्यांपैकी ॲनॅटेज व रूटाइल हीच रूपे रंगद्रव्य म्हणून उपयोगी पडतात. रासायनिक दृष्ट्या ती सारखीच आहेत पण त्यांच्या स्फटिक जालकातील टिटॅनियम व ऑक्सिजन यांची मांडणी भिन्न आहे.
प्रथम धातुक वाळवून त्याची अतिसूक्ष्म पूड तयार करतात व ती शिशाचे अस्तर लावलेल्या मोठ्या काँक्रीट पात्रात टाकून संहत (विद्रावातील प्रमाण जास्त असलेल्या) सल्फ्यूरिक अम्लाबरोबर वाफ सोडून प्रक्रिया चालू करतात. प्रक्रिया झालेला घन पदार्थ गरम पाण्यात विरघळविला, तर टिटॅनियम सल्फेट व फेरिक सल्फेट असा मिश्र विद्राव मिळतो. फेरिक लोहाचे फेरस लोहात रूपांतर करून फेरस सल्फेट स्फटिकरूपात वेगळे काढले जाते. उरलेल्या विद्रावात मुख्यत्वे टिटॅनियम सल्फेट असते. विद्राव गरम करून त्यामध्ये ॲनॅटेजाचे किंवा रूटाइलाचे सूक्ष्म स्फटिक टाकतात, यामुळे मूळ विद्रावातील स्फटिक बनण्यास मदत मिळते. हा विद्राव काळजीपूर्वक पाणी घालून विरल केला जातो व जलीय विच्छेदनामुळे (पाण्याच्या विक्रियेने रेणूचे तुकडे झाल्यामुळे) टिटॅनियम सल्फेटाचे टिटॅनियम हायड्रेट (सजल टिटॅनियम डाय-ऑक्साइड) या अतिसूक्ष्म पांढऱ्या घन पदार्थात रूपांतर होते. पांढऱ्या लगद्यांच्या स्वरूपातील हा पदार्थ गाळून धुतात. त्यामुळे त्यातील अपद्रव्ये निघून जातात. नंतर हा पदार्थ फिरत्या लांब दंडगोलावर भट्टीत १,००० अंश से.ला भाजतात. पाणी व संश्लेषित सल्फ्यूरिक अम्ल यांचे बाष्पीभवन होऊन हायड्रेटाचे रूपांतर टिटॅनियम डाय-ऑक्साइड स्फटिकात होते. हायड्रेट हे अतिसूक्ष्म कणरूपात असल्यामुळे रंगलेप तयार करण्यास उपयोगी पडत नाही. भाजण्याच्या क्रियेत स्फटिक वाढविले जाऊन महत्तम अपारदर्शकता मिळते. त्यानंतर ⇨ केंद्रोत्सारणासारख्या क्रिया करून टिटॅनियम डाय-ऑक्साइडाचे सर्व कण शक्य तितक्या प्रमाणात एकसारखे केले जातात व रंगलेपाचे गुणधर्म जास्त चांगले होण्यासाठी अँटिमनी ऑक्साइडासारखे पदार्थ अल्प प्रमाणात घालतात. शेवटी प्रक्रियित टिटॅनियम डाय-ऑक्साइड वाळवून आवश्यकतेप्रमाणे बारीक करतात व आवेष्टित करून बाजारात पाठवितात. नैसर्गिक रूटाइल स्फटिक इतर धातूंच्या भेसळीमुळे रंगीत असतात. अतिसूक्ष्म दळलेल्या रूटाइल खनिजात ९८% टिटॅनियम डाय-ऑक्साइड असू शकते. ते विशिष्ट भट्टीत वायुरूप क्लोरिनाबरोबर तापविल्यास त्याचे टिटॅनियम टेट्राक्लोराइडात रूपांतर होते. हे द्रवरूप असल्याने ऊर्ध्वपातनाने (तापवून व बाष्परूप पदार्थ थंड झाल्यावर गोळा करून) अतिशय शुद्ध स्वरूपात मिळू शकते. त्यापासून टिटॅनियम डाय-ऑक्साइड मिळविण्याच्या बाकीच्या क्रिया वरीलप्रमाणेच असतात.
उच्च प्रणमनांक, सफेदपणा व रासायनिक अक्रियता हे टिटॅनियम डाय-ऑक्साइडाचे महत्त्वाचे गुणधर्म आहेत. ते बिनविषारी आहे. उच्च प्रणमनांकामुळे त्याला प्राप्त झालेल्या उत्तम अपारदर्शकतेमुळे त्याला विशेष महत्त्व आलेले आहे. ॲनॅटेज स्फटिकाचा प्रणमनांक २·५२ तर रूटाइलाचा २·७६ असतो. रूटाइल हे झिंक ऑक्साइडापेक्षा आठ पटींनी जास्त प्रकाश परावर्तित करते, असे दिसून आले आहे. ॲनॅटेज स्फटिक सूक्ष्म आकारमानातील कण रूपात दृश्य वर्णपटातील सर्व तरंगलांब्यांचे परावर्तन व प्रकीर्णन करतो. त्यामुळे परावर्तित व प्रकीर्णित प्रकाशाचे तरंगलांबी संघटन आपाती प्रकाशाप्रमाणेच असते. यामुळे त्याचे चूर्ण पूर्ण सफेद दिसते. रूटाइल स्फटिक ४३० मिलिमायक्रॉनपेक्षा कमी तरंगलांबीच्या प्रकाशाच्या काही भागाचे शोषण करतो व त्यामुळे त्याचे चूर्ण किंचित पिवळट दिसते. टिटॅनियम डाय-ऑक्साइडावर खूम गरम तीव्र अम्लांचा व क्षारांचा परिणाम होतो परंतु उत्पादनात वा प्रत्यक्ष वापरताना ज्यांचा संबंध येतो, अशा सामान्य वायू व द्रव पदार्थाचा त्यावर काही परिणाम होत नाही.
रंगद्रव्य व वाहक यांच्या प्रणमानांकांमधील फरकामुळे कोणत्याही एका तरंगलांबीकरिता जास्तीत जास्त अपारदर्शकता देणाऱ्या कणाचे आकारमान इष्टतम असते. अल्किल रंगलेपासाठी ॲनॅटेज रंगद्रव्याच्या कणाचे जे आकारमान उपयुक्त ठरते तेच पायस रंगलेपाकरिता चालत नाही. प्रत्यक्षात निरनिराळ्या माध्यमांत वापरता येणारे परंतु रंगलेपाच्या मुख्य गुणधर्मावर फारसा वाईट परिणाम होत नाही असे कण-आकारमान ठरवितात. सर्वसाधारणपणे टिटॅनियम डाय-ऑक्साइड रंगद्रव्य कणाचे आकारमान ०·२५ मायक्रॉन असते.
टिटॅनियम डाय-ऑक्साइडाच्या शुद्ध नमुन्याचे अंगभूत गुणधर्म हे काही उत्तम रंगलेप तयार करण्यास योग्य असतातच असे नाही. त्यामुळे त्यावर काही प्रक्रिया करून ते जास्त उपयुक्त करावे लागते. याकरिता (१) प्रत्यक्ष उत्पादन क्रिया करताना काही नियंत्रणे ठेवणे, (२) इतर रंगद्रव्ये किंवा समावेशके वापरणे, (३) संघटनातील इतर पदार्थ योग्य गुणधर्माचे किंवा त्यांचे सुधारित प्रकार वापरणे वगैरे उपाययोजना करतात.
वातावरणक्रियेच्या परिणामाने रंगलेप लावलेल्या पृष्ठभागाचे चूर्णन होऊन विघटन होते. ज्या ठिकाणी बंधकाचे विनाशी ⇨ ऑक्सिडीभवनहोते तेथे बंधक खराब होऊन रंगद्रव्याचे कण नीट एकत्र बांधलेले राहत नाहीत. रंगद्रव्य व बंधक यांचे प्रमाण वाढविले, तर चकाकी टिकण्याची क्षमता कमी होते व चूर्णन लवकर सुरू होते परंतु संरक्षक रंगलेपाकरिता जेव्हा चकाकी टिकणे महत्त्वाचे नसते तेव्हा रंगद्रव्याचे अधिक प्रमाण पटलाचे आयुष्य वाढविते. प्रकाशाच्या क्रियेमुळे ॲनॅटेज रंगद्रव्य काही दिवसांनी पिवळट होत जाते आणि त्यामुळेच रूटाइलाचा शोध लागेपर्यंत त्याचा फारसा व्यापक प्रमाणात उपयोग केला गेला नाही. चूर्णन व निस्तेजन (विटणे) या क्रियांना प्रतिकार करण्यासाठी टिटॅनियम डाय-ऑक्साइडाच्या रेणूंच्या पृष्ठभागावर इतर अकार्बनी ऑक्साइडे (विशेषेकरून सु. १% अल्युमिना) लावल्यास बराच उपयोग होतो परंतु रूटाइल वापरात आल्यापासून हा प्रयोग मागे पडला, मात्र या प्रयोगामुळे घरांसाठी वापरावयाच्या पांढऱ्या एनॅमल रंगलेपात खूपच फरक पडल्याने रूटाइलाइतकाच ॲनॅटेजाचा उपयोग होऊ लागला.
टिटॅनियम व्हाइट्स या नावाखाली आल्फा टिटॅनियम डाय-ऑक्साइड व बेरियम सल्फेट किंवा कार्बोनेट अथवा गॅमा टिटॅनियम डाय-ऑक्साइड आणि कॅल्शियम सल्फेट अशी निरनिराळी मिश्रणे बाजारात उपलब्ध आहेत. ही मिश्रणे एकत्र अवक्षेपण (अविद्राव्य साक्याच्या रूपात मिळविणे), एकत्र भाजणे अथवा एकत्र दळणे या क्रियांनी तयार करता येतात. या मिश्रणात २५–८०% टिटॅनियम डाय-ऑक्साइड असते व त्या प्रमाणात त्यांचे गुणधर्म असतात.
टिटॅनियम डाय-ऑक्साइड रंगद्रव्याचा उपयोग सर्वसाधारणपणे गडद छटा सोडून सर्व प्रकारच्या रंगलेपांमध्ये करता येतो. त्याच्या रासायनिक अक्रियतेमुळे पहिल्या, दुसऱ्या व अंतिम हात द्यावयाच्या सर्व प्रकारच्या रंगलेपांत त्याचा वापर करण्यात येतो. त्याच्या उपयोगामुळे मूळ पृष्ठभाग गंजण्याच्या प्रक्रियेस मदत होत नाही पण ते स्वतः गंजरोधक रंगद्रव्य नाही. टिटॅनियम डाय-ऑक्साइडावर अम्लाचा वा त्याच्या वाफांचा परिणाम होत नसल्याने अशा वातावरणात हे रंगद्रव्य असलेले रंगलेप लवकर खराब होत नाहीत. टिटॅनियम डाय-ऑक्साइड विषारी नसल्याने त्याचा उपयोग खाद्यपदार्थ उद्योगात, दुग्धव्यवसायात व मुलांच्या खेळण्याकरिता लागणाऱ्या रंगलेपांत करण्यात येतो. कागद, पांढरे रबर व प्लॅस्टिके, लिनोलियम, छपाईची शाई, काचेची व मृत्तिका पात्रे इत्यादींत या रंगद्रव्याचा उपयोग करतात.
झिंक ऑक्साइड : टिटॅनियम डाय-ऑक्साइडाच्या शोधापूर्वी झिंक ऑक्साइड व झिंक सल्फाइड ही रंगद्रव्ये बऱ्याच प्रमाणात वापरली जात होती परंतु टिटॅनियम डाय-ऑक्साइडाच्या जास्त चांगल्या गुणधर्मामुळे यांचा उपयोग कमी होत गेला तरी पण कमी दर्जा किंवा कमी किंमत आवश्यक असेल तेथे यांचा अजूनही वापर केला जातो किंवा टिटॅनियम डाय-ऑक्साइडाबरोबर मिश्रण करूनही यांचा उपयोग करतात. (अ) झिंक ऑक्साइड किंवा झिंक व्हाइट (झिंक ऑक्साइडाची पेस्ट) आणि (आ) झिंक सल्फाइड किंवा बेरियम सल्फेटाबरोबरील मिश्रण (याला लिथोपोन म्हणतात) यांवर आधारलेली पांढरी रंगद्रव्ये वापरात आहेत.
जस्त हे निसर्गात इतर धातूंबरोबर (विशेषतः शिसे, लोह, मँगॅनीज, कॅडमियम, चांदी यांच्याबरोबर) थोड्या प्रमाणात मिश्र रूपात आढळते. ते स्फॅलेराइट किंवा झिंक ब्लेंड (ZnS) या धातुकाच्या रूपात सापडते व त्यात अपद्रव्ये असल्याने सर्वसाधारणपणे ते काळे किंवा तपकिरी असते. जस्त, मँगॅनीज व लोह यांचे जटिल ऑक्साइड फ्रँक्लिनाइट या नावाच्या धातुक रूपात अमेरिकेतील न्यू जर्सी राज्यात सापडते व अमेरिकेतील जस्ताचा पुरवठा मुख्यत्वे त्यापासून होतो. त्याचा मुख्य फायदा म्हणजे ते शिशापासून मुक्त आहे. जस्त हे कार्बोनेट, कॅलॅमीन, विलेमाइट, झिंकाइट इ. प्रकारांतही उपलब्ध आहे.
झिंक ऑक्साइडाचे उत्पादन करण्याच्या दोन मुख्य पद्धती आहेत : (१) अप्रत्यक्ष पद्धत : ही फ्रान्समध्ये विकसित झाली, (२) प्रत्यक्ष पद्धत : ही अमेरिकेत वापरली जाते. या दोन पद्धतींतील फरक हा केवळ सुरुवातीच्या कच्च्या मालापुरता आहे. अप्रत्यक्ष पद्धतीत जस्त धातू मूळ रूपात वापरली जाते व प्रत्यक्ष पद्धतीत झिंक ऑक्साइड जस्त धातुकापासून सरळ मिळविले जाते. दोन्ही पद्धतींत जस्ताचे बाष्प जाळून झिंक ऑक्साइड मिळविले जाते.
झिंक ऑक्साइडाचे संघटन व गुणधर्म कच्च्या मालाची शुद्धता व उत्पादन पद्धती यांवर अवलंबून असतात. नेहमी आढळणारी अपद्रव्ये म्हणजे कॅडमियम व शिसे ही असून ती उत्पादन क्रियेत बाष्पीभवनाच्या वेळी येतात. यांशिवाय कारखान्यातील यांत्रिक हाताळणीत आयर्न ऑक्साइड, सिलिका व ॲल्युमिना ही अपद्रव्ये झिंक ऑक्साइडाबरोबर येतात. अप्रत्यक्ष पद्धतीत मिळणारे ऑक्साइड प्रत्यक्ष पद्धतीने मिळणाऱ्या ऑक्साइडापेक्षा जास्त शुद्ध असते कारण त्यात कच्चा माल म्हणून वापरण्यात येणारी जस्त धातू शुद्ध स्वरूपात वापरता येते.
अमेरिकेखेरीज ब्रिटन वगैरे देशांत मूळ धातुकात सल्फर ऑक्साइडे किंवा क्षारकीय लेड सल्फेट असल्यामुळे प्रत्यक्ष पद्धतीने तयार केलेल्या झिंक ऑक्साइडाबरोबर क्षारकीय लेड सल्फेट अपद्रव्य म्हणून येते परंतु यामुळे काही अपाय होत नाही. काही वेळा प्रत्यक्ष पद्धतीत मुद्दाम सल्फर ऑक्साइडे कच्च्या मालाबरोबर घालतात व त्यामुळे लेडेड (लेड सल्फेटयुक्त) झिंक ऑक्साइड मिळते. ५%, १५%, २५% वा ३५% क्षारकीय लेड सल्फेट असलेली झिंक ऑक्साइडे बाह्य पृष्ठभागी लावावयाच्या रंगलेपांकरिता विशेष उपयुक्त असतात.
झिंक ऑक्साइडाच्या कणांचे आकारमान दोन्ही पद्धतींत नियंत्रित करता येते. अप्रत्यक्ष पद्धतीत आकारमान साधरणपणे ०.२ मायक्रॉन, तर प्रत्यक्ष पद्धतीत ०.२५ मायक्रॉन असते.
वरील पद्धतींनी तयार केलेले झिंक ऑक्साइड षट्कोणी घट्ट बांधलेल्या स्फटिक जालक रूपात असते, असे क्ष-किरण परीक्षेवरून दिसून येते. सूक्ष्मदर्शकातून पाहिले असता त्यांचा आकार गोलाकार लांबट, अनियमित सूच्याकृती वा पट्टिकेसारखा आढळतो व पुष्कळ वेळ २-३ स्फटिक एकत्र होऊन पुंजके झालेले असतात. प्रणमनांक २.०८. झिंक ऑक्साइडाची रंगद्रव्यशक्ती ही व्हाइट लेड (१.९) व झिंक सल्फाइड (२.३७) यांच्या दरम्यान असून साधारणपणे लिथोपोनापेक्षा कमी असते.
शुद्ध ऑक्साइड तेजस्वी पांढरे असते. बाजारात उपलब्ध असलेले ऑक्साइड त्यातील अपद्रव्यांनुसार चकचकीत पांढरे ते पिवळट वा करडे पांढरे असते (उदा., कॅडमियमामुळे तपकिरी पिवळसर छटा येते). झिंक ऑक्साइड जंबुपार (दृश्य वर्णपटातील जांभळ्या रंगाच्या पलीकडील अदृश्य) प्रकाशाकरिता अपारदर्शक आहे. ०.०००१ मिमी. जाडीचे पटल ३,६०० Åच्या खालील सर्व तरंगलांब्यांचे प्रारण (तरंगरूपी ऊर्जा) रोखू शकते. झिंक ऑक्साइडाचे नेहमीचे रंगद्रव्य प्रकार बिनविषारी आहेत पण लेडेड झिंक ऑक्साइड विषारी असल्याने त्याच्या वापरावरील निर्बंध पाळणे आवश्यक असते.
झिंक ऑक्साइड हे व्यापारी उपयोगाच्या अनेक वस्तूंना पांढरा रंग देण्यासाठी वापरण्यात येते पण त्याचा मुख्य उपयोग रबर व रंगलेप उद्योगांत होतो. नैसर्गिक व संश्लेषित रबरांना पांढरा रंग प्राप्त करून देण्यासाठी झिंक ऑक्साइडाचा उपयोग करतात. रंगलेप उद्योगात झिंक ऑक्साइड या बहुगुणी रंगद्रव्यामुळे पटलाचे बाह्यरूप वाढते, टिकाऊ रंगलेपातील ओलिओरेझीनयुक्त वाहकातील अम्लाबरोबर विक्रिया होऊन तयार झालेला जस्त साबण पटल घट्ट करण्यास मदत करतो आणि यामुळे बाह्य पृष्ठभागावरील रंगकामाची वातावरणक्रियेने होणाऱ्या चूर्णनामुळे होणारी खराबी नियंत्रित होते. झिंक ऑक्साइडामुळे रंगलेपाच्या पटलामध्ये अपघर्षण व आर्द्रतारोध निर्माण होऊन ती धुवून काढून टाकण्यास अधिक सुलभ होते.
झिंक ऑक्साइड जंबुपार प्रकाशाला अपारदर्शक असल्याने बाह्य रंगलेपामध्ये त्याचा विशेष उपयोग होतो. त्यामुळे बाह्य रंगलेपाची खराबी बरीच कमी होते म्हणून झिंक ऑक्साइडाला बाह्य रंगलेपाची रंगधारणाशक्ती (रंग धरून ठेवण्याची शक्ती) वाढविण्यास विशेष प्राधान्य आहे. याशिवाय झिंक ऑक्साइड कवकप्रतिबंधक (बुरशीसारख्या हरितद्रव्यरहित वनस्पती वाढण्यास प्रतिबंध करणारे) असल्याने बाह्य भिंतीवरील रंगलेपावर कवके वाढत नाहीत व त्यामुळे जहाजाच्या समुद्रात राहणाऱ्या भागावर लावण्याच्या रंगलेपात त्याचा उपयोग केला जातो.
पाण्यातील रंगलेपात झिंक ऑक्साइड वापरल्याने कुजण्याच्या क्रियेवर नियंत्रण राहते. अप्रत्यक्ष पद्धतीने मिळविलेल्या नेहमीच्या आकारमानाच्या झिंक ऑक्साइडामुळे रंगलेप पटलास चकाकी येते व विशेषतः अंतर्गत उपयोगाच्या रंगलेपात सूक्ष्म कणांमुळे उत्तम प्रकारे चकाकी टिकण्याचा गुणधर्म येतो. मोठ्या आकारमानाची ऑक्साइडे (विशेषतः सूच्याकृती व लेडेड ऑक्साइडे) बाह्य रंगलेपाकरिता जास्त उपयोगी पडतात. सूच्याकृती स्फटिकांमुळे रंगलेप पटलाची ताकद वाढते व त्याला तडे जाण्याचे प्रमाण कमी होते.
झिंक ऑक्साइड बिनविषारी असल्याने आवेष्टित खाद्यपदार्थांशी संबंध येणाऱ्या रंगलेपांत त्याचा उपयोग करता येतो आणि यामुळे खाद्यपदार्थाकरिता वापरण्यात येणाऱ्या शोभादायक रंगांच्या बाबतीतील आरोग्यविषयक धोके कमी होतात. हे ऑक्साइड इतर पांढऱ्या रंगद्रव्यांबरोबर मिश्रण करून वापरता येत असल्याने त्यांची किंमत कमी होऊन काही प्रमाणात दर्जा वाढविता येतो. ओलिओरेझीनयुक्त अम्लाबरोबर याच्या होणाऱ्या विक्रियेमुळे रंगलेपाची समसांद्रता (एकसारखा दाटपणा), ब्रश वापरण्याची सुविधा व वापरण्याचे गुणधर्म या दृष्टीने, तसेच साठवणीमध्ये रंगद्रव्य घट्ट होण्याच्या व पिवळट छटा येण्याच्या क्रियांना प्रतिबंध करण्यासाठी याचा उपयोग होतो. यामुळे टिटॅनियम डाय-ऑक्साइड व झिंक सल्फाइड रंगद्रव्यांबरोबर मिश्रण केलेल्या रूपात झिंक ऑक्साइडाचा फार मोठ्या प्रमाणात उपयोग केला जातो. यांखेरीज मृत्तिका पात्रे, काच, लिनोलियम, वस्त्र उद्योग, शाई, कागद यांमध्ये तसेच रंगलेपांत वापरावयाच्या झिंक स्टिअरेट, झिंक रेझिनेट, झिंक क्रोम यांसारख्या संयुगांच्या उत्पादनाकरिता झिंक ऑक्साइड वापरले जाते.
झिंक सल्फाइड : या पांढऱ्या रंगद्रव्याचे तीन प्रकार वापरात आहेत : (१) लिथोपोन : हे संमिश्र रंगद्रव्य बेरियम सल्फेट व २६-३२% झिंक सल्फाइड यांपासून बनवितात. (२) ६०% लिथोपोन : यात बेरियम सल्फेट व ६०-६१% झिंक सल्फाइड असते. (३) ९५% शुद्ध असलेले झिंक सल्फाइड.
ही रंगद्रव्ये तयार करण्यासाठी झिंक सल्फेट व बेरियम सल्फाइड यांचे विद्राव एकत्र आणून झिंक सल्फाइड व बेरियम सल्फेट यांचे एकत्र अवक्षेपण करतात.
ZnSO4 + BaS ⟶ ZnS + BaSO4
यात झिंक सल्फाइडाचे प्रमाण २९.४ % असते.
झिंक सल्फाइड हे खालीलप्रमाणे झिंक क्लोराइडापासूनही बनविले जाते.
ZnCl2 + BaS ⟶ZnS + BaCl2
(अवक्षेप) (पाण्यात विद्राव्य)
बेरियम सल्फाइड मिळविण्यासाठी बराइट खनिज व कोक किंवा अँथ्रॅसाइट एकत्र केलेले चूर्ण एका लांब फिरत्या नलिकाकार भट्टीत पुरेशी हवा व प्रोड्युसर वायू (कार्बनयुक्त इंधन व हवा यांच्या आंशिक ज्वलनाने तयार होणारा वायू) यांच्या मिश्रणाने १,१०० अंश से. पर्यंत तापवितात. मूळ कच्च्या मालातून आलेली सिलिकॉन, लोह, ॲल्युमिनियम व कॅल्शियम ही अपद्रव्ये काढून टाकून अतिशय शुद्ध बेरियम सल्फाइड विद्राव रूपात मिळवितात. झिंक सल्फेट व झिंक क्लोराइड ही संयुगे इतर रासायनिक उद्योगंतून मिळालेल्या उपपदार्थांपासून तयार केली जातात.
झिंक सल्फाइडाची झिंक ब्लेंड (घनीय) व व्ह्यूर्टझाइट (षट्कोणी) अशी दोन स्फटिकरूपे आहेत. पहिले सामान्य तापमानाला स्थिर असून दुसरे १,०२० से. पेक्षा जास्त तापमानास तयार होते. व्ह्यूर्टझाइट स्फटिक जंबुपार प्रकाशात अस्थिर असल्याने त्यापासून बनविलेले लिथोपोन सूर्यप्रकाशात काळे पडते परंतु आता भट्टीत टाकतानाच अल्प प्रमाणात कोबाल्ट धातूचे मिश्रण करून हा दोष दूर केला जातो. झिंक सल्फाइडाचा प्रणमनांक २.३७ असून ते टिटॅनियम डाय-ऑक्साइडानंतरचे अतिशुभ्र रंगद्रव्य आहे. त्याची रंगद्रव्यशक्ती लिथोपोनाच्या दुपटीहून जास्त आहे. लिथोपोनाची रंगद्रव्यशक्ती झिंक ऑक्साइडापेक्षा २५% जास्त असून ६०% लिथोपोन हे या बाबतीत लिथोपोन व झिंक सल्फाइड यांच्यामध्ये येते. झिंक सल्फाइडाचे लिथोपोनामध्ये निराळे अस्तित्व असून ते लिथोपोनातून अलग काढणे रासायनिक विक्रियेनेच शक्य होते. झिंक सल्फाइड रंगद्रव्ये अतिशुभ्र असून त्यांची तुलना अतिशय उत्तम दर्जाच्या झिंक ऑक्साइडाबरोबर होऊ शकते. झिंक सल्फाइड बिनविषारी असून रासायनिक दृष्ट्या अक्रिय असल्याने त्याचा उपयोग शिसेयुक्त रंगद्रव्याबरोबर शुष्कन तेलात करता येतो. या रंगद्रव्याची शुष्कन तेलाशी किंवा रेझीनयुक्त अम्लाशी विक्रिया होत नाही. झिंक सल्फाइड जंबुपार प्रकाशाला झिंक ऑक्साइडापेक्षा कमी अपारदर्शक असून त्याची रंगछटा टिकविण्याची क्षमता झिंक ऑक्साइडापेक्षा थोडी कमी आहे.
झिंक सल्फाइड रंगद्रव्ये ही रंगलेप, रबर, लिथोलियम, प्लॅस्टिके, कागद, शाई, कातड्यावरील अंतिम संस्करण द्रव्ये, चर्मसदृश कापड इत्यादींत वापरतात. झिंक सल्फाइड बाह्य रंगलेपासाठी फारसे वापरले जात नाही पण अंतिम हात देण्यापूर्वी द्यावयाच्या रंगलेपाकरिता वापरतात. त्याचा मुख्य दुर्गुण म्हणजे वातावरणक्रियेमुळे त्याचे प्रथम चूर्णन व नंतर झीज होते. झिंक ऑक्साइड किंवा भरणद्रव्ये यांच्याबरोबर मिश्रण करून हा दोष पुष्कळसा दूर करता येतो. झिंक सल्फाइड रंगद्रव्ये संश्लेषित पायस वाहकात (उदा., पॉलिव्हिनिल ॲसिटेट, पॉलिस्टायरीन इ.) वापरल्यास चूर्णन होत नाही, असेही दिसून आले आहे. झिंक सल्फाइड रंगद्रव्य हे अतिशुभ्र रंगद्रव्यांपैकी असल्याने रंगीत रंगद्रव्यांबरोबर मिसळून स्वच्छ छटा मिळविण्याकरिता पुष्कळ प्रमाणात वापरले जाते. ह्या छटा विटण्याच्या बाबतीत चांगल्या स्थिर असून बहुतेक वाहकांत सहजपणे ओल्या होतात व विखुरतात आणि त्यामुळे रंगद्रव्याचे चूर्ण करण्याचा वेळ व खर्च यांत बचत होते. त्याच्या बिनविषारीपणामुळे अंतर्गत सुशोभन, खाद्यपदार्थांचे डबे इत्यादींकरिता त्याचा उपयोग केला जातो.
झिंक सल्फाइड अतिसूक्ष्म प्रमाणात तांबे, चांदी व काही धातवीय संयुगांबरोबर उच्च तापमानाला तापविले असता सक्रियित होऊन पुष्कळ प्रकारची अनुस्फुरक (कोणत्या तरी ऊर्जा स्रोताने उत्तेजित झाल्याने विद्युत् चुंबकीय प्रारणाचे उत्सर्जन करणारी व उत्तेजन थांबल्यावर उत्सर्जन बंद होणारी) व प्रस्फुरक (कोणत्या तरी ऊर्जा स्रोताने उत्तेजित झाल्याने विद्युत् चुंबकीय प्रारणाचे उत्सर्जन करणारी पण उत्तेजन थांबल्यावरही उत्सर्जन चालू ठेवणारी) रंगद्रव्ये तयार करता येतात. प्रस्फुरक झिंक सल्फाइड अंधारात वस्तू दिसण्यासाठी (उदा., वाहतूक नियंत्रणाच्या खुणा) व विशेष शोभादायक परिणामासाठी वापरतात. अनुस्फुरक झिंक सल्फाइड दूरचित्रवाणी व रडार यांतील → ऋण-किरण नलिकेकरिता वापरण्यात येणाऱ्या रंगलेपातील मुख्य घटक आहे.
धुवून काढून टाकता येणारे पाण्यातील रंगलेप आणि अंतर्गत उपयोगासाठी लागणारे रंगलेप यांच्या गरजेपोटी लिथोपोनाच्या वापरात त्वरित वाढ झाली. पुरेशी अपारदर्शकता, ब्रशाने लावण्याची सुलभता, समपातळीत येण्याची क्षमता आणि साठवणीतील असाधारण स्थैर्य या गुणधर्मांमुळे लिथोपोनाचा प्रसार लवकर झाला व हे गुणधर्म अद्यापही महत्त्वाचे ठरतात. अलीकडील काळात फिकट छटा लोकप्रिय झाल्यामुळे त्याकरिता ६०% लिथोपोन व झिंक सल्फाइड यांचा जास्त उपयोग केला जातो. नवीन संश्लेषित रेझीनयुक्त पायस व संश्लेषित रंगलेप यांमुळे आधुनिक वाहकांना जास्त रंगद्रव्य-प्रमाण चालत नाही आणि जास्त विद्रावकांचा उपयोग करावा लागल्याने पूर्वीपेक्षा जास्त ताकद असलेली रंगद्रव्ये वापरावी लागतात. इष्ट सरासरी रंगधारणक्षमता ही आता साधारणपणे ६०% लिथोपोनाच्या बरोबर मानण्यात येते. हे साधण्याकरिता झिंक सल्फाइड एकटे किंवा अधिक ताकद असलेल्या टिटॅनियम डाय-ऑक्साइडाबरोबर वापरतात.
इतर पांढरी रंगद्रव्ये : व्हाइट लेड : हे सु. २,००० वर्षे माहीत असलेले व सर्वांत जुन्या ज्ञात असलेल्या रंगद्रव्यांपैकी एक आहे. ‘व्हाइट लेड’ हे नाव ब्रिटनमध्ये कित्येक शतके प्रचारात आहे. हे एक प्रकारचे रंगद्रव्य असून ते शिशाच्या क्षारकीय कार्बोनेटांचे किंवा हायड्रॉक्सी कार्बोनेटांचे मिश्रण आहे, असे सिद्ध झाले आहे परंतु रंगद्रव्याच्या रासायनिक संघटनावरून त्याची रंगलेपाकरिता असणारी उपयुक्तता ठरविता येत नाही. कणांचे आकार व सूक्ष्मता यांसारख्या गुणधर्मांचे प्रमाणही पहावे लागते.
डच पद्धत या व्हाइट लेडाच्या सर्वांत जुन्या उत्पादन पद्धतीत मोठ्या लाकडी पिंपात धातवीय शिशाचा ढीग रचून त्यावर हवा, आर्द्रता, कार्बन डाय-ऑक्साइड व ॲसिटिक अम्ल यांची प्रक्रिया करून व्हाइट लेड बनवीत असत. आता सर्वत्र नवीन उत्पादन क्रिया वापरल्या जातात. या सर्व क्रिया लेड ऑक्साइड किंवा हायड्रॉक्साइड हे लेड ॲसिटेटामध्ये विद्राव्य आहे व व्हाइट लेड अविद्राव्य आहे या तत्त्वावर आधारलेल्या आहेत.
अपारदर्शकता वाढविण्याकरिता थोड्या प्रमाणात टिटॅनियम डाय-ऑक्साइडाचे चूर्णनबरोबर प्रकार व इतर उपयुक्त भरणद्रव्ये वापरून व्हाइट लेडाची ब्रशाने लावण्याची सुलभता व प्रवाहीपणा हे गुणधर्म सुधारता येतात, तसेच अपारदर्शकता कमी न करता स्थिरता वाढविता येते. याचा मुख्य उपयोग लाकूड आणि संदला (भिंतीच्या पृष्ठभागाकरिता वापरण्यात येणारे मऊ गिलाव्यासारखे द्रव्य) यांकरिता तसेच जवसाच्या तेलात १०% शेंदूर (रेड लेड) घालून त्यासह पृष्ठभागाकरिता करतात. व्हाइट लेडाचे शोभादायक गुणधर्म कमी असल्याने त्याचा दीर्घ काळाकरिता केवळ संरक्षक रंगद्रव्य म्हणून उपयोग होत नाही.
अँटिमनी ऑक्साइड : हे सफेद चूर्णरूप असून कमी प्रतीचे करड्या रंगाचे असते. याचा प्रणमनांक २.० आहे. याचे रंगलेप वाहकात ओले होण्याचे व विखुरण्याचे गुणधर्म चांगले आहेत. हे रासायनिक दृष्ट्या अक्रिय व बिनविषारी आहे. याचा मुख्य उपयोग ॲनॅटेज, टिटॅनियम डाय-ऑक्साइड रंगद्रव्याबरोबर मिश्रण करण्याकरिता होतो. यामुळे टिटॅनियम डाय-ऑक्साइडाचा चूर्णनाचा दुर्गुण कमी होण्यास साहाय्य होते. आग मंदावण्यास मदत करणाऱ्या रंगलेपात अँटिमनी ऑक्साइड वापरले जाते.
कॅल्शियम प्लंबेट : हे एक गंजरोधक रंगद्रव्य असून त्याचा उपयोग गंजरोधक रंगलेपाकरिता विशेषतःजस्तलेपित लोखंडी पत्र्यांकरिता वापरावयाच्या रंगलेपासाठी करतात. व्यापारी रंगद्रव्यात ९४-९७ % कॅल्शियम प्लंबेट असून त्यात कल्शियम प्लंबाइट, सिलिका, ॲल्युमिना, मॅग्नेशिया इ. अपद्रव्ये असल्यामुळे त्याचा रंग फिका पिवळट (बिस्किटासारखा) असतो.
भरणद्रव्ये : ही नैसर्गिक किंवा संश्लेषित अकार्बनी संयुगे असून रासायनिक दृष्ट्या अक्रिय असतात. अतिसूक्ष्म कणरूपातील ही द्रव्ये मूळ रंगलेपातील महाग रंगद्रव्याची जागा काही अंशी घेण्यासाठी वापरतात. यामुळे उत्पादन खर्च कमी करता येतो. आधुनिक काळात वापरली जाणारी भरणद्रव्ये वरील कार्यापेक्षा पुढील चांगले गुणधर्म प्राप्त करून देण्यासही मदत करतात : (१) द्रवरूपातील रंगलेप साठवणीत जास्त काळ स्थिर राहू शकतात कारण काही भरणद्रव्ये ही रंगद्रव्य संधारक (द्रव्यात लोंबकळत्या अवस्थेत राहण्यास मदत करणारी) म्हणून कार्य करून खाली तळाशी बसणारे अती घट्ट थर होण्याची क्रिया मंदावण्यास मदत करतात किंवा अजिबात होऊ देत नाहीत. (२) झोळ येणे वा पडद्यासारखे स्वरूप प्राप्त होणे हा काही रंगलेपांचा दोष रंगद्रव्याबरोबर योग्य भरणद्रव्य वापरून दूर करता येतो. (३) काही भरणद्रव्ये रंगलेपाच्या मूळ लेपास प्रबलित करून वापर, खरचटणे इ. प्रकारे होणाऱ्या झिजेपासून काही प्रमाणात संरक्षण देतात, तसेच प्रकाश, आर्द्रता, गंजकारक वातावरण यांचा प्रतिकार करण्यास मदत करून रंगलेपाचे आयुष्य वाढवितात. (४) त्यांच्या उपयोगामुळे रंगलेपाचे एकावर एक देण्यात येणारे थर एकमेकांना चिकटण्यास मदत होते. (५) रंगलेपाच्या थराची पूर्णता वाढण्यास मदत होते.
सर्वसाधारण उपयोगात असलेली भरणद्रव्ये म्हणजे बेरियम सल्फेट (बराइट, ब्लँक फिक्स), बेरियम कार्बोनेट, कॅल्शियम सल्फेट, कॅल्शियम कार्बोनेट (व्हायटिंग), सिलिका व निरनिराळ्या धातूंची सिलिकेटे (उदा., ॲस्बेस्टीन, संगजिरे, केओलीन वगैरे) ही होत. ही सर्व नैसर्गिक किंवा मुद्दाम तयार केलेल्या रूपात मिळतात.
रंगीत अकार्बनी रंगद्रव्ये : लेड क्रोम : ही रंगद्रव्ये रासायनिक प्रक्रियेने अवक्षेपित करून फिकट प्रिमरोझ ते शेंदरी छटांमध्ये तयार केली जातात. या रंगद्रव्यांचा मुख्य घटक लेड क्रोमेट (PbCrO4) असला, तरी त्यामुळे मिळणाऱ्या विविध छटा त्या त्या वेळी तयार होणारे निरनिराळे स्फटिक आकार व ते एकमेकांशी कशा प्रकारे संलग्न होतात यांवर अवलंबून असतात. दुसरे महत्त्वाचे कारण म्हणजे लेड क्रोमेट व लेड सल्फेट हे घटक एकत्र येऊन ‘मिश्र स्फटिक’ तयार होतात आणि ते एकमेकांशी इतके एकजीव होतात की, ते अलग करणे फारच कठीण असल्याने मिश्रणाला मिश्र स्फटिक म्हणण्याऐवजी ‘घन विद्राव’ म्हणतात.
कोष्टक क्र. १. लेड क्रोम रंगद्रव्ये
| छटा | घटक | स्फटिक आकार |
| फिकट प्रिमरोझ | लेड क्रोमेट, ३० – ५०% लेड सल्फेट (स्थिरीकरण केलेले) | समचतुर्भुजी |
| प्रिमरोझ किंवा लेमन (लिंबू) फिकट रंग | लेड क्रोमेट, ४५ – ५५% लेड सल्फेट | एकनताक्ष |
| लेमन रंग | लेड क्रोमेट, २० – ४५% लेड सल्फेट | एकनताक्ष |
| मध्यम | लेड क्रोमेट | एकनताक्ष |
| नारिंगी | क्षारकीय लेड क्रोमेट | चतुष्कोणीय |
| शेंदरी | लेड क्रोमेट, लेड सल्फेट व लेड मॉलिब्डेट | चतुष्कोणीय |
शुद्ध लेड मॉलिब्डेट हे पांढरे असून त्याचे स्फटिक चतुष्कोणीय असतात परंतु लेड क्रोमेट व लेड सल्फेट यांच्या बरोबर स्फटिकीकरण होताना स्फटिक चतुष्कोणीय व शेंदरी होतात. मॉलिब्डेट आयनांनी (-MoO4) लेड क्रोमेट स्फटिकांचा आकार बदलल्याने हा रंगबदल होतो.
लेड क्रोम रंगद्रव्ये निरनिराळ्या छटांमध्ये तयार करता येतात. यांच्या सर्व प्रतींची अपारदर्शकता व रंजनक्षमता (छटा देण्याची शक्ती) चांगली असते. ही रंगद्रव्ये साधारणपणे स्वस्त असतात. ती तेल विद्रावकांत अविद्राव्य असून रंगलेप वाहकांत सहजपणे विखुरतात. वाहकांबरोबर त्यांची विक्रिया होत नसल्याने ती रंगलेप, छपाईची शाई व लिनोलियम यांकरिता मोठ्या प्रमाणात वापरतात. मॉलिब्डेट क्रोम रंगद्रव्ये नारिंगी क्रोम रंगद्रव्यांपेक्षा जास्त ताकदवान असतात आणि ती पुष्कळशा अधिक लाल छटांमध्ये तयार करता येतात परंतु प्रकाशाच्या क्रियेने ती फिकट होतात. सर्व लेड क्रीम रंगद्रव्यांत शिशाचे प्रमाण बरेच असले, तरी ती विषारी समजली जात नाहीत.
झिंक क्रोम : ही रंगद्रव्ये ZnCrO4 या सूत्राप्रमाणे व्यापारी प्रमाणावर तयार करता येत नाहीत, तर क्षारकीय झिंक पोटॅशियम क्रोमेट [K2CrO4, 3ZnCrO4, Zn(OH)2] अशी तयार करतात. झिंक क्रोम ही लेमन यलो छटांमध्ये उपलब्ध असून रंगद्रव्ये म्हणून पुष्कळ उपयुक्त आहेत परंतु त्यांची अपारदर्शकता व रंजनक्षमता ही लेड क्रोमांपेक्षा कमी दर्जाची आहे. ती प्रकाशामध्ये विटत नाहीत. झिंक क्रोम आणि प्रशियन ब्ल्यू (निळे) ही रंगद्रव्ये कोरडी एकत्र दळल्यास झिंक ग्रीन (हिरवी रंगद्रव्ये) मिळतात.
प्रशियन ब्ल्यू : या रंगद्रव्यांचे रासायनिक संघटन KFe, Fe(CN)6, xH2O असे देता येईल. काही ब्ल्यूंमध्ये पोटॅशियमाची जागा काही प्रमाणात किंवा पूर्णत: अमोनिया गट (NH4) किंवा सोडियम हे घेतात.
या रंगद्रव्यांचे पुढील चार मुख्य प्रकार आहेत : (१) उच्च ब्राँझिंग़ ब्ल्यू-मुख्यतः छपाईच्या शाईकरिता ( रंगद्रव्य वाहकात चूर्णरूपाने साधारण उच्च प्रमाणात समाविष्ट केल्यास काही निळ्या रंगद्रव्यांना धातवीय चमक प्राप्त होते या गुणधर्माला ब्राँझिंग म्हणतात). (२) मध्यम ब्राँझिंग ब्ल्यू (मिलॉरी ब्ल्यू) – ही रंगद्रव्ये साधारणपणे लेड क्रोम ग्रीनच्या उत्पादनाकरिता किंवा निळ्या रंगाच्या फिकट छटा तयार करण्यासाठी वापरतात. (३) ब्राँझिंग न होणारी ब्ल्यू रंगद्रव्ये – सेल्युलोज लॅकरकरिता. (४) विद्राव्य ब्ल्यू रंगद्रव्ये.
प्रशियन ब्ल्यूचे उत्पादन दोन टप्प्यांत केले जाते : (१) प्रथम फेरोसायनाइडाचा विद्राव फेरस सल्फेटामध्ये टाकून ‘व्हाइट पेस्ट’ [K2 Fe.Fe(CN)6] तयार करतात. ही पेस्ट फिकट हिरवटसर निळ्या (मोरपंखी) छटेची असते. (२) व्हाइट पेस्टचे ऑक्सिडीकरण करून गर्द निळ्या छटेचे प्रशियन ब्ल्यू रंगद्रव्य मिळवितात. ऑक्सिडीकरण विद्रावाच्या उकळबिंदूच्या वर तीव्र अम्ल वातावरणात पोटॅशियम डायक्रोमेट, सोडियम क्लोरेट वा इतर ऑक्सिडीकारकाच्या साहाय्याने केले जाते. ऑक्सिडीकरण जास्त प्रमाणात झाल्यास निळ्या छटेवर विपरीत परिणाम होतो.
सोडियम फेरोसायनाइड वापरले, तर निळी छटा फिकट होते व ती समाधानकारक नसते परंतु जास्त प्रमाणात अमोनियम सल्फेट वापरले, तर NH4 गटाचा रंगद्रव्यात समावेश होऊन जास्त समाधानकारक रंगद्रव्य मिळते आणि त्याची छटा व घनता पोटॅश ब्ल्यूसारखी असते. अमोनिया ब्ल्यूचे उत्पादन पोटॅश ब्ल्यूपेक्षा स्वस्त असल्याने शक्य तेथे ते वापरले जाते परंतु पोटॅश ब्ल्यू हे काही बाबतींत जास्त समाधानकारक असल्याने त्याचा उपयोग केला जातो.
ब्राँझिंग न होणारी ब्ल्यू रंगद्रव्ये तयार करण्यासाठी काही खास समावेशक द्रव्यांचा उपयोग न करता उत्पादन परिस्थितीची फक्त जुळवाजुळव करण्यात येते परंतु अजिबात ब्राँझ छटा घालविणे जवळजवळ अशक्य आहे.
विद्राव्य प्रशियन ब्ल्यू रंगद्रव्ये तयार करण्यासाठी प्रशियन ब्ल्यू फिल्टर केकचा ऑक्झॅलिक अम्ल किंवा पोटॅशियम फेरोसायनाइड किंवा या दोन्हींबरोबर अवजड मिश्रण यंत्रात लगदा बनवितात व राळा कमी तापमानाला वाळविला जातो.
प्रशियन ब्ल्यू रंगद्रव्याच्या स्वच्छ निळ्या छटा, ब्राँझिंग परिणामामुळे तकाकीचे रूपांतरण होऊन येणारी अधिक रंजनक्षमता परंतु कमी असलेली अपारदर्शकता हे गुणधर्म महत्त्वाचे आहेत. पांढऱ्या रंगद्रव्याबरोबर मिश्रण करून उत्तम प्रकारच्या हिरवटसर निळ्या रंगछटा मिळतात. ही रंगद्रव्ये तेलांत वा विद्रावकांत पसरत नाहीत व विद्राव्य ब्ल्यू रंगद्रव्यांखेरीज बाकीची पाण्यात विरघळत नाहीत. अम्लांना ती चांगली रोधक आहेत पण क्षारांचा त्यांच्यावर चटकन परिणाम होतो. क्षारामुळे गेलेला रंग पुन्हा अम्ल घालून परत आणता येतो.
लेड क्रोम ग्रीन : ही रंगद्रव्ये ब्रन्सविक ग्रीन व क्रोम ग्रीन या नावांनीही ओळखली जातात. ही लेड क्रोम व प्रशियन ब्ल्यू यांची यांत्रिक रीतीने केलेली मिश्रणे होत. ही मिश्रणे दोन प्रकारे बनवितात. (१) लेड क्रोम व प्रशियन ब्ल्यू ही रंगद्रव्ये इमारतीकरिता लागणारा चुना बनविण्याच्या पद्धतीप्रमाणे विशिष्ट प्रकारच्या चक्कीमध्ये दळणे. (२) लेड क्रोमचे प्रशियन ब्ल्यूबरोबर अवक्षेपण करून या रंगद्रव्यांना स्ट्रक ग्रीन म्हणतात. दुसऱ्या पद्धतीत जास्त गडद व स्थिर हिरवी छटा मिळविता येते, तर पहिल्या प्रकारात घटकांच्या प्रमाणांवर नियंत्रण ठेवता येत असल्याने निरनिराळ्या मधल्या छटा बनविता येतात.
प्रशियन ब्ल्यू हे ज्वलनशील असून लेड क्रोम हे त्याकरिता लागणारा ऑक्सिजन सहज पुरविते. त्यामुळे एकदा आग लागली म्हणजे ती आटोक्यात आणणे कठीण असते. आग लागलेला भाग चटकन बाजूला काढून अलग करणे आवश्यक असते. मिश्रण करताना आग लागल्यास लगेच बराइटे टाकल्यास विरलीकरण होऊन व तापमान कमी होऊन जळणारे रंगद्रव्य तात्पुरते विझविता व बंदिस्त करता येते.
चांगली अपारदर्शकता, रंग भरण्याची क्षमता, स्वस्तपणा व क्षार सोडून इतर बाबतींत योग्य स्थिरता या गुणधर्मामुळे ही रंगद्रव्ये रंगलेप व लिनोलियम यांकरिता मोठ्या प्रमाणात वापरली जातात.
क्रोमियम ऑक्साइड ग्रीन : ही रंगद्रव्ये तयार करण्यासाठी सोडियम डायक्रोमेट व गंधक यांचा ढीग धूममार्ग असलेल्या व विटांनी बांधलेल्या कोठीत जाळतात. साधारणपणे ३०-४०% जास्त गंधक वापरले जाते. जास्तीचे गंधक सल्फर डाय-ऑक्साइडाच्या रूपात बाहेर पडते व त्याचे शोषण करणे आवश्यक असते, नाहीतर प्रदूषण होण्याचा धोका असतो.
क्रोमियम ऑक्साइड (Cr2O3) व सजल क्रोमियम ऑक्साइड [Cr2O(OH)4] यांची उष्णता व रसायने यांना प्रतिकार करण्याची क्षमता चांगली आहे. प्रकाश, अम्ल व क्षार यांचा त्यांवर वाईट परिणाम होत नाही. रंगछटा मात्र निस्तेज असते. या रंगद्रव्यांची अपारदर्शकता व रंजनक्षमता कमी असल्याने रंगलेपात त्यांचा उपयोग कमी प्रमाणात होतो. जास्त करून ती डिस्टेंपर, रंगीत सिमेंट रंगलेप व मृत्तिका वस्तू यांकरता वापरली जातात.
क्रोमियम ऑक्साइड रंगलेपाचे महत्त्व दुसऱ्या महायुद्धात वाढले. हा रंगलेप अवरक्त प्रकाश (दृश्य वर्णपटातील तांबड्या रंगाच्या अलीकडील अदृश्य प्रकाश) परावर्तित करीत असल्याने त्याचा मायावरण रंगलेप [⟶ मायावरण,सैनिकी] म्हणून उपयोग करण्यात आला, कारण अवरक्त छायाचित्रणात युद्धाचे सामान गवताच्या आणि झाडाझुडपांच्या रंगात स्पष्ट दिसते.
आयर्न ऑक्साइड व सजल आयर्न ऑक्साइड रंगद्रव्ये : विविध रूपांतील आयर्न ऑक्साइड रंगद्रव्य म्हणून कित्येक शतके वापरले जात आहे. जगातील निरनिराळ्या भागांत ते मोठ्या प्रमाणात आढळते व त्यामुळे अतिप्राचीन काळातील कलावंतांनी त्याचा गुहांतील चित्रांत उपयोग केलेला दिसून येतो. हजारो वर्षे असलेली ही प्राचीन कला आयर्न रेड (तांबडे) ऑक्साइड व यलो ऑकर (पिवळी माती, सजल ऑक्साइड) यांचा टिकाऊपणा सिद्ध करते. नैसर्गिक आयर्न ऑक्साइडांबरोबर नंतर कारखान्यांतही ही ऑक्साइडे तयार होऊ लागल्याने फिकट पिवळ्यापासून लाल-भगव्यापर्यंत, तसेच पूर्ण काळी या सर्व छटा उपलब्ध झाल्या.
रंगद्रव्य उत्पादनाला योग्य असे नैसर्गिक आयर्न ऑक्साइड प्रकार पुढील प्रदेशांत खाणींतून काढले जातात : रेड ऑक्साइडे – स्पेन, इराणचे आखात, अमेरिकेची संयुक्त संस्थाने व ब्रिटन यलो ऑकर – दक्षिण आफ्रिका, उत्तर आफ्रिका, भारत, इटली, सार्डिनिया, अमेरिकेची संयुक्त संस्थाने, फ्रान्स, स्पेन व ब्रिटन सिएना – इटली ब्राऊन (तपकिरी) अंबर–सायप्रस संकीर्ण आयर्न ऑक्साइडे – ब्रिटन फ्रान्स, उत्तर आफ्रिका, स्पेन, इराणचे आखात. जगातील इतर भागांतही थोड्या प्रमाणात ही खनिजे सापडतात पण त्यांचा उपयोग जास्त करून स्थानिक स्वरूपातच केला जातो.
नैसर्गिक आयर्न ऑक्साइड खनिजांचे रूपांतर रंगलेपांत वापरण्यास योग्य अशा रंगद्रव्यात करण्यासाठी पुढील प्रक्रिया करतात : (१) नैसर्गिक आर्द्रता काढून टाकण्यासाठी शुष्कीकरण, (२) योग्य त्या आकारमानातील कण तयार करण्यासाठी दळणे, (३) रंगद्रव्यांत दोष निर्माण करणारी अपद्रव्ये काढून टाकण्यासाठी शुद्धीकरण, (४) रेणूला जोडले गेलेले पाणी काढून टाकण्यासाठी भट्टीत भाजणे. यामुळे नैसर्गिक खनिजात नसलेली पण हवी असलेली योग्य रंगछटा मिळविण्यात येते. वर उल्लेखिल्याप्रमाणे ही खनिजे निरनिराळ्या प्रदेशांत सापडत असल्याने त्यांबरोबर असणारी अपद्रव्ये निरनिराळी असतात. यामुळे त्यांच्या रंगछटा वेगवेगळ्या असून त्यांच्या शुद्धीकरणाच्या क्रियाही निरनिराळ्या असतात. या निरनिराळ्या रंगीत मातीसंबंधी अधिक माहिती ‘रंगीत माती’ या नोंदीत दिलेली आहे.
पर्शियन गल्फ रेड : याचा पोत कठीण असून त्यात ६०-८०% फेरिक ऑक्साइड (Fe2O3) व थोड्याफार प्रमाणात विद्राव्य क्लोराइडे असल्याने त्याच्या उपयोगात दोष उद्भवतात.
स्पॅनिश रेड ऑक्साइडे : ही वरीलपेक्षा जास्त शुद्ध (८०-९० % फेरिक ऑक्साइड) असून यांत अगदी थोड्या प्रमाणात विद्राव्य अपद्रव्ये असतात. त्यामुळे ही वरीलपेक्षा जास्त उपयोगी आहेत.
ब्रिटिश रेड ऑक्साइडे : ही मऊ ५०-६०% फेरिक ऑक्साइडयुक्त असून ब्रिटनमधील विक या गावातील खाणीत मिळणाऱ्या दुसऱ्या प्रकारात ८५-८८% फेरिक ऑक्साइड असते. विद्राव्य अपद्रव्ये कमी असल्याने हा दुसरा प्रकार स्पॅनिश रेड ऑक्साइडाच्या तोडीचा असतो.
बॉक्साइट-अवशेष रेड : हा ॲल्युमिनियमाच्या उत्पादनात मिळणारा उपपदार्थ आहे. बॉक्साइट हे सोडियम हायड्रॉक्साइडाबरोबर वितळवून अवशेषाचे पाण्याबरोबर निष्कर्षण करतात. या रंगद्रव्यात ६०% फेरिक ऑक्साइड असून त्याला पिवळटसर तांबडी छटा असते.
पर्पल ऑक्साइड : हे पण एका उपपदार्थापासून बनते. आयर्न पायराइट हे खनिज सल्फ्यूरिक अम्लाच्या उत्पादनात वापरतात. त्यात मिळणाऱ्या अवशेषात ८५-९०% फेरिक ऑक्साइड असून थोड्या प्रमाणात आयर्न सल्फाइड असते. त्यामुळे जांभळट तपकिरी रंगाचे रंगद्रव्य मिळते.
नैसर्गिक ब्राउन ऑक्साइडे : सिएना व अंबर यांमध्ये ॲल्युमिनियम सिलिकेटे सजल आयर्न ऑक्साइडाबरोबर संयोजित झालेली असतात आणि तेलांतील त्यांच्या सापेक्ष पारदर्शकतेचे हे कारण असावे, असे समजले जाते. यामुळे रंगलेप लावल्यावर त्याचे एकूण स्वरूप कणीदार असल्यासारखे दिसण्यासाठी या रंगद्रव्यांचा वापर करतात. अभ्रकसदृश आयर्न ऑक्साइड धातुक हे अभ्रकाप्रमाणे पातळ पत्रीसारख्या आकाराचे असून अतिशय शुद्ध रूपात (९८-९९% फेरिक ऑक्साइड) सापडते. यापासून गर्द करडा रंगलेप तयार करता येतो व तो पोलादी कामाकरिता पुष्कळ प्रमाणात वापरला जातो.
ब्लॅक (काळे) ऑक्साइड : हे पर्पल ऑक्साइडाप्रमाणे ॲनिलिनासारख्या पदार्थाच्या उत्पादनातून उपपदार्थ म्हणून मिळते. दुर्बल अम्ल विद्रावात लोखंड वापरून नायट्रो संयुगांचे → क्षपण करताना ब्लॅक आयर्न ऑक्साइडाचा राळा मिळतो. त्याच्याबरोबर काही प्रमाणात कार्बनी अपद्रव्ये असतात. हे ऑक्साइड तापरोधक नसून त्याची रंजनक्षमता पण कमी आहे आणि त्यामुळे स्वस्त रंगलेपांत व सिमेंटासाठी वापरावयाच्या रंगलेपांत त्याचा वापर करतात.
संश्लेषित आयर्न ऑक्साइडे व सजल आयर्न ऑक्साइडे : ही रंगद्रव्ये पिवळ्या, तांबड्या, तपकिरी ते काळ्या अशा विविध रंगछटांमध्ये उपलब्ध आहेत. त्यांच्यातील फरक केवळ रासायनिक
संघटनापुरताच आहे असे नसून एकच संघटन असलेल्या रंगद्रव्यांमध्ये अंतर्गत रेणवीय संरचना निरनिराळी आढळते. आकृतीमध्ये निरनिराळ्या आयर्न ऑक्साइडांचे एकमेकांशी असलेले रासायनिक संबंध दाखविले आहेत. उत्पादनातील निरनिराळ्या परिस्थितींवर म्हणजे सुरूवातीचा कच्चा माल, अवक्षेपणाची परिस्थिती, भाजण्यासाठी दिलेला काळया सर्वांवर नियंत्रण ठेवून वरील रंगद्रव्ये तयार करतात. सुरुवातीचा कच्चामाल म्हणून लागणारे फेरस क्लोराइड (पिकल लिकर) व फेरस सल्फेट (कॉपरस) हे दोन्ही पदार्थ लोखंड व पोलाद यांच्यावरील प्रक्रियेत उपपदार्थ म्हणून मिळतात.
लेमनयलो : ही आल्फा-फेराइटे असून मुख्यतः फेरस सल्फेट विद्रावापासून बनविली जातात. तापमानातील बदल, विक्रिया घटकांचे प्रमाण व विक्रियेचा काळयांच्या नियंत्रणाने निरनिराळ्या छटा मिळविता येतात.
मिडल (मध्यम) यलो : ही लेपिडोक्रोसाइटे किंवा गॅमा-फेराइटे असून साधरणपणे फेरस क्लोराइड विद्रावापासून क्षाराने अवक्षेपण करून व हवेच्या झोतप्रक्रियेने ऑक्सिडीकरण करून बनविली जातात. क्षाराऐवजी चुना, व्हायटिंग, मॅग्नेशिया किंवा दाहक (कॉस्टिक)सोडा हे ही वापरता येतात.
ब्राउन ऑक्साइडे : ही फेरस ऑक्साइडाच्या गरम पाण्यातील संघारणाचे (द्रवात लोंबकळत्या अवस्थेतील कणांचे) सरळ ऑक्सिडीकरण करून मिळवतात. ही फेरस ऑक्साइडे फेरस क्लोराइडामध्ये क्षार टाकल्यास मिळतात. नेहमीची ब्राउन ऑक्साइडेही संश्लेषित यलो, रेड व ब्लॅक ऑक्साइडे कोरडी दळून तयार केलेल्या मिश्रणापासून बनवितात.
रेड ऑक्साइडे : ही कोणत्याही सजलयलोऑक्साइडापासून वा ब्लॅकऑक्साइडापासून भट्टीत तापविल्यास मिळतात. ४००°– ६००° से. तापमानावर टर्कीरेड आणि अधिक तापमानावर (९००°.) इंडियन रेड बनतात.
आयर्न ऑक्साइडांचे सर्वांत महत्वाचे गुणधर्म म्हणजे त्यांचा टिकाऊपणा व रंगधारणाशक्ती हे होत. रसायनांच्या विक्रियेसही रोधक असून तेल, विद्रावक रेझिने, कार्बनी अम्ले किंवा क्षार यांची त्यांच्यावर काहीही विक्रिया होत नाही. सिएना व अंबर सोडून बाकीच्या रंगद्रव्यांचे प्रणमनांक उच्च असल्याने त्यांचा उपयोग करून बनविलेल्या रंगलेपांची अपारदर्शकता चांगली असते. जंबुपारप्रकाशाचे शोषण करण्याची त्यांची (विशेषतःअभ्रकसदृशऑक्साइडांची) क्षमता असल्याने रंगलेप पटलास रासायनिक संरक्षण मिळते. सजल आर्यन ऑक्साइडे (उदा., यलो किंवा ब्राउन) उष्णतेच्या बाबतीत अस्थिर असून तापविल्यास लाल बनतात.
नैसर्गिक आयर्न ऑक्साइडे स्वस्त पडत असली, तरी त्यांची शुद्धता संश्लेषित ऑक्साइडांपेक्षा बरीच कमी असते. त्यामुळे रंगद्रव्य म्हणून वापरण्यास ती काही प्रसंगी निरुपयोगी ठरतात परंतु तयार करताना विशेष काळजी घेतल्यास ती संश्लेषित ऑक्साइडांइतकीच उपयोगी पडतात. साधारणपणे संश्लेषित ऑक्साइडांचे रंग तेजस्वी व गडद असतात.ही रंगद्रव्ये जास्त प्रमाणात एकसमान असून सामान्यतः त्यांचे कण अधिक लहान आकारमानाचे असतात व त्यांचा पोतही इतर अवक्षेपित रंगद्रव्यांप्रमाणे असतो.
पूढे पहा
”