प्रथिने :प्रथिन या शब्दाच्या ‘प्रोटीन’ या इंग्रजी प्रतिशब्दाची व्युत्पती proteios या ग्रीक शब्दापासून झालेली असून त्याचा अर्थ जीवनक्रियेसाठी लागणारा आद्य पदार्थ, असा आहे (मूळ ग्रीक शब्दाचा अर्थ ‘आद्य’ किंवा ‘प्रथम’ असा आहे) जे. जे. बर्झीलियस या स्वीडीश रसायनशास्त्रज्ञांच्या सूचनेवरून जी.जे. मल्डर यांनी १८३६ मध्ये ‘प्रोटीन्स’ हा शब्द प्रथम वापरला. प्रथिने ही नायट्रोजनयुक्त संयुगे असून त्यांची संरचना अत्यंत जटिल (गुंतागुंतीची) असते. प्राण्यांच्या पोषणातप्रथिनांना अतिशय महत्त्व असून प्राणिजीवनातील रासायनिक प्रक्रिया त्यांच्यावर अवलंबून असतात. कोशिकांच्या (पेशींच्या) वाढीसाठी प्रथिनांची गरज असते. प्रथिनांपासून कोशिकांना नायट्रोजन मिळतो. वनस्पतींच्या कोशिकांतील अंतर्गत द्रव्यातही मोठ्या प्रमाणावर प्रथिने असतात. प्रथिनांमध्ये जातिविशिष्टता आढळून येते.यामुळेच एका जातीच्या प्राण्याची प्रथिने दुसऱ्या जातीच्या प्राण्याच्या शरीरात गेली असता ⇨ ॲलर्जीसारखे विकार निर्माण होतात. तसेच प्राण्यामध्ये प्रथिनांची अवयवविशिष्टताही आढळते. एकाच प्राण्याच्या निरनिराळ्या अवयवांतील (उदा., स्नायू, मेंदू, आतडी इत्यादींतील) प्रथिने वेगवेगळ्या प्रकारांची असतात. प्रथिनांचे जलीय विच्छेदन (पाण्याच्या रेणूची H व OH या रूपाने विक्रिया घडवून संयुगाचे तुकडे करण्याची क्रिया) केले असता ही भिन्नभिन्न प्रथिने निरनिराळ्या २१ आल्फा ॲमिनो अम्लांपासून तयार झाल्याचे आढळते [⟶ ॲमिनो अम्ले]. ज्या ॲमिनो अम्लात COOH गटाच्या शेजारच्या कार्बन अणूला NH2 गट जोडलेला असतो, त्यालाआल्फा ॲमिनोअम्ल म्हणतात. कार्बोहायड्रेटे वा वसा (स्निग्ध पदार्थ) यांच्याशी तुलना करता प्रथिनाचा रेणू फार मोठा असतो. त्यांचा रेणूभार सु. ६,००० ते कित्येक लक्षापर्यंत आहे. एकाच प्रकारचे कार्य असलेल्या वेगवेगळ्या प्रथिमांतीलॲमिनो अम्लांचे प्रमाणव प्रथिनाच्या संरचनेतील त्यांचा क्रम सर्वसाधारणपणे सारखाच असतो. सामान्यतः प्रथिने ही कार्बन, हायड्रोजन, ऑक्सिजन, नायट्रोजन वगंधक या मूलद्रव्यांची बनलेली असतात तथापि काहींमध्ये फॉस्फरस, आयोडीन, मॅंगॅनीज, लोह, तांबे, जस्त इ. मूलद्रव्येही आढळतात.
इतिहास : प्रथिनासंबंधीची माहिती निरनिराळ्या संशोधकांनी केलेल्या प्रयत्नांतून मिळालेली आहे. एच्. रिटहौझेन यांनी १८६० मध्ये प्रथिनांतील घटक ॲमिनोअम्लांचा तक्ता प्रथम प्रसिद्ध केला. टी. बी. आस्बर्न, एमिल फिशर, एच्. बी. व्हिकरी व ए. सी. चिबनाल यांनीही प्रथिनांसंबंधी महत्त्वाचे संशोधन केले. १९५५ मध्ये फ्रेडरिक सँगर व त्यांचे सहकारी यांनी प्रथिनांतील सहसंयुजी (ज्यामध्ये जोडलेल्या दोन्ही अणूंनी एकेक इलेक्ट्रॉन देऊन तयार झालेली इलेक्ट्रॉन जोडी समाइक असल्यामुळे बंध बनलेला असतो अशी) संरचना शोधून काढली. याच सुमारास ई. जे. कोन त्यांच्या सहकाऱ्यांनी तापमान, pH मूल्य [⟶ पीच मूल्य], आयनी प्रबलता (विद्युत् भारित रेणू, अणू वा अणुगट यांच्यातील सरासरी विद्युत् स्थितिक परस्परक्रिया दर्शवणारी राशी), विद्युत् अपार्यता स्थिरांक [⟶ विद्युत् अपारक पदार्थ], विशिष्ट द्विसंयुजी (इतर अणूंशी संयोग पावण्याची क्षमता दर्शवणारा अंक दोन असणाऱ्या) ऋणायनांचा (धन विद्युत् भारित असलेल्या व विद्युत् विच्चेदनात ऋणाग्राकडे जाणाऱ्या आयनांचा) वापर इत्यादींमध्ये आवश्यक त्या सुधारणा करून विविध प्रथिने वेगवेगळी करण्याच्या पद्धती शोधून काढल्या. ⇨ वर्णलेखन, ⇨ विद्युत् संचारण इ. आधुनिक तंत्रांचा वापर करुन प्रथिनांविषयीच्या ज्ञानात अधिकाधिक भर पडत आहे.
वर्गीकरण : एमील फिशर व फ्रान्ट्स होफमाइस्टर यांनी स्वतंत्ररित्या १९०२ मध्ये प्रथिने ही पॉलिपेप्टाइडे [पेप्टाइड बंधांनी जोडल्या गेलेल्या ॲमिनो अम्लांच्या शृंखला ⟶ ॲमिनो अम्ले] असून त्यांत बरीच ॲमिनो अम्ले असतात असे सिद्ध केले. या शोधानंतरच प्रथिनांच्या रासायनिक व भौतिक गुणधर्मांनुसार प्रथिनांचे वर्गीकरणकरण्याचे प्रयत्न झाले. १९२० पर्यंत प्रथिनांच्या जैव कार्याबद्दल विशेष माहिती नव्हती. अगदी सुरुवातीचे वर्गीकरण हे विविध विद्रावकांमधील (विरघळविणाऱ्या पदार्थांमधील) प्रथिनांच्या विद्राव्यतेनुसार (विरघळण्याच्या क्षमतेनुसार) केलेले होते. तथापि हे वर्गीकरण तितकेसे समाधानकारक नव्हते. कारण सारखी संरचना व कार्ये असणाऱ्या प्रथिनांची विद्राव्यता भिन्न असते, तर वेगवेगळी संरचना व कार्ये असणाऱ्या प्रथिनांची विद्राव्यता सारखी असते, असे आढळून आले. तथापि ह्या वर्गीकरणात वापरण्यात आलेल्या संज्ञा अद्यापही वापरतात. इंग्लंड व अमेरिका येथील शरीरक्रियावैज्ञानिक संघटनांनी अनुक्रमे १९०७ व १९०८ मध्ये विद्राव्यता वसंरचना यांनुसार केलेले प्रथिनांचे वर्गीकरण बराच काळ वापरात होते. प्रथिनांच्या जैव कार्यानुसारही वर्गीकरण करण्यात आले होतेपण तेही नमुनेदार म्हणता येत नाही. कारण एकाच प्रथिनांची अनेक कार्ये असतात व त्यामुळे एखाद्या प्रथिनाचे विशिष्ट कार्य स्पष्टपणे माहीत नसते. यांशिवाय एंझाइमांवर(जीवरासायनिक विक्रिया घडवून आणण्यास मदत करणाऱ्या प्रथिनांवर) आधारित असेही वर्गीकरण करण्यात येते. तथापि वरील वर्गीकरणे व्यापक दृष्ट्या वापरता येत नाहीत. खाली दिलेली प्रथिनांची माहिती जुन्या वर्गीकरणानुसार आहे.
साधी प्रथिने : जलीयविच्छेदन केले असता ज्या प्रथिनांपासूनफक्त ॲमिनो अम्लेच मिळतात, त्यांना साधी प्रथिने असे म्हणतात. अल्ब्युमिने, ग्लोब्युलिने, प्रोटामिने, हिस्टोने इ. प्रथिने या प्रकारची आहेत. अंडी, दूध, रक्त इत्यादींमध्ये ह्यांतील अनेक प्रथिने असतात. उदा., दुधात अल्ब्युमीन,आल्फा लॅक्टाल्ब्युमीन, ग्लोब्युलीन, बीटा लॅक्टोग्लोब्युलीन, केसीन ही साधी प्रथिने असतात.
अल्ब्युमिने : स्नायू, दुध, अंडी, रक्तद्रव, वनस्पती इत्यादींमध्ये ही प्रथिने आढळतात. ही पाण्यात विरघळतात. उष्णतेने त्यांचे किलाटन होते (साखळतात). अमोनियम सल्फेट जास्त प्रमाणात असलेल्या विद्रावातून अल्ब्युमिने बाहेर फेकली जातात. जलीय विच्छेदन केल्यास त्यांपासून आल्फा ॲमिनो अम्ले वा त्यांचे अनुजात (एखाद्या संयुगापासून तयार करण्यात आलेली दुसरी संयुगे) मिळतात. रेणुभार सु. ६०,००० असतो.
ग्लोब्युलिने : दूध, रक्तद्रव, स्नायू, अंडी इत्यादींत अल्ब्युमिनांबरोबर तसेच वाटाणा, घेवडा, भुईमूग, बदाम इ. वनस्पतींत ही प्रथिने आढळतात. भिन्न रेणुभारांच्या प्रथिनांचे ते मिश्रण असते. उष्णतेने त्यांचे किलाटन होते. शुद्ध पाण्यात फारशी विरघळत नाहीत पण लवणांच्या उदासीन विरल विद्रावांत विरघळतात. एंझाइमे व अम्ले यांमुळे त्यांचे ॲमिनो अम्लांत अपघटन (घटक द्रव्ये अलग होणे) होते. विद्युत् संचारण तंत्राने ही प्रथिने अल्ब्युमिनापासून वेगळी करता येतात, तसेच त्यांचे आल्फा, बीटा व गॅमा या प्रकारांत वर्गीकरण करता येते. हे प्रकार विविध जैव व रासायनिक गुणधर्म असलेल्या प्रथिनांची मिश्रणे असतात. प्रतिरक्षात्मक विद्युत् संचारण तंत्राने ग्लोब्युलिनांचे विसाहून अधिक घटक वेगळे करता येतात. बहुतेक प्रतिपिंड गॅमा ग्लोब्युलिने आहेत [⟶ प्रतिपिंड]. बहुतेक ग्लोब्युलिनांचा रेणुभार सु. १,७०,००० च्या आसपास असतो. तथापि काहींचा (मॅक्रोग्लोब्युलिनांचा) ८,००,००० इतका उच्च असतो.
प्रोटामिने : ही काही विशिष्ट माशांच्या (उदा., सामन, हेरिंग) शुक्रकोशिकांत (पुं-जनन पेशीत) आढळतात. डीऑक्सिरिबोन्यूक्लिइक अम्लाशी [⟶ न्यूक्लिइक अम्ले] ही प्रथिने निगडित असतात. ही प्रथिने तीव्र क्षारकीय (अम्लाशी विक्रिया झाल्यास लवण देण्याचा गुणधर्म असलेली) असून जलीय विच्छेदनाने त्यांपासून प्रामुख्याने क्षारकीय ॲमिनो अम्ले मिळतात.यांत आर्जिनीन या ॲमिनो अम्लाचे प्रमाण जास्त असते. पाणी, विरल अमोनिया विद्राव, अम्ले, क्षारीय (अल्कालाइन) विद्राव यांत ती विरघळतात. उष्णतेने त्यांचे किलाटन होत नाही. रेणुभार सु. ६,००० इतका असतो.
हिस्टोने : ही प्रोटामिनांहून कमी क्षारकीय असतात. प्राणी व वनस्पती यांच्या शरीर कोशिकांच्या केंद्रकात (कोशिकेचे कार्य नियंत्रित करणाऱ्या जटिल गोलसर पुंजात) प्रमुख डीऑक्सिरिबोन्यूक्लिइक अम्लाबरोबर न्यूक्लिओहिस्टोन स्वरूपात आढळते मात्र प्राण्यांच्या शुक्रकोशिकांत आढळत नाहीत. जलीय विच्छेदनाने यांपासून मोठ्या प्रमाणावर क्षारकीय ॲमिनो अम्ले मिळतात.ट्रिप्टोफेन वगंधकयुक्त ॲमिनो अम्ले वगळताइतर ॲमिनो अम्ले त्यांत आढळतात. लायसीन वा आर्जिनीन यांचे प्रमाण जास्त असते. पाणी, विरल अम्ले व क्षारीय विद्राव यांत ती विरघळतात. विरल अमोनिया विद्रावात विरघळत नाहीत. उष्णतेने त्यांचे सहसा किलाटन होत नाही. रेणुभार सु. १०,००० ते २२,००० इतका असतो.
प्रोलामिने : ही वनस्पतीजन्य प्रथिने आहेत. बियांतून तेल काढल्यावर ५०-८०% अल्कोहॉलयुक्त पाण्याने ही प्रथिने वेगळी करतात. ही प्रथिने पाण्यात विरघळत नाही पण पाणी-एथॅनॉल मिश्रणात विरघळतात. त्यांतील प्रोलीन ग्लुटामीन यांच्या जास्त प्रमाणामुळे ती सजल एथॅनॉलामध्ये विरघळतात. या प्रथिनांमुळे भिजविलेले पीठ चिकट होते. उदा., मक्यातील झाईन व गव्हातील ग्लायडीन. कोणतेही प्रोलामीन अद्याप शुद्ध स्फटिकीय स्वरुपात मिळविता आलेले नाही.
ग्लोबिने : या प्रथिनांमध्ये हिस्टिडीन हे क्षारकीय ॲमिनो अम्ल अधिक प्रमाणात असते. सामान्यतः यांचा समावेश हिस्टोनांमध्ये करतात पण ती हिस्टोनांपेक्षा वेगळी आहेत. ती क्षारकीय नाहीत, तसेच हिस्टोनांप्रमाणे अमोनियम हायड्रॉक्साइडाने अवक्षेपित होत वा तत्सम रंगद्रव्यांशी संयोग होऊन हीमोग्लोबिन [⟶ रक्तारुण] इ. संयुगे तयार होतात. इन्शुलीन व ग्लोबिने यांचे मिश्रण मधुमेहात अंतःक्षेपणासाठी (इंजेक्शनसाठी) वापरतात.
ग्लुटेलिने : ही वनस्पतीज प्रथिने आहेत. अतिविरल अम्लात व क्षारांत ती विरघळतात पण उदासीन विद्रावकांत विरघळत नाहीत. गव्हातील ग्लुटेनीन आणि तांदळातील ओरिझेनीन ही या प्रथिनांची उदाहरणे होत.
स्क्लेरोप्रथिने (किंवा अल्ब्युमिनानॉइडे): ही प्रथिने तंतुमय असतात. ती सर्वसाधारण विद्रावकांत विरघळत नाहीत. तसेच त्यांवर प्रथिन-अपघटक (प्रथिनांचे अपघटन होण्यास साहाय्य करणाऱ्या) एंझाइमांची विक्रिया होत नाही. हे गुणधर्म शरीराचे रक्षण करण्यास उपयोगी पडतात. या प्रथिनांचे पुढील महत्त्वाचे प्रमुख उपप्रकार होतात : (१) कोलॅजेन, (२) इलॅस्टीन व (३) केराटिने.
कोलॅजेन : सर्व बहुकोशिकीय (अनेक पेशींनी बनलेल्या) प्राण्यांत, विशेषतः त्यांच्या संयोजी ऊतकांत (कार्यकारी कोशिकांना आधार देऊन त्यांना एकत्रित ठेवणाऱ्या कोशिका समूहांत), हे प्रथिन आढळते. त्वचा, हाडे, कंडरा (स्नायू हाडाला वा कूर्चेला घट्ट बांधणाऱ्या दोरीसारखा तंतुसमूह) व संधिबंध यांमध्ये हे प्रथिन सापडते. सर्व प्राणिज प्रथिनांमध्ये कोलॅजेन हे कदाचित सर्वांत विपुल आढळणारे प्रथिन आहे. सस्तन प्राण्यांतील एकूण प्रथिनांत याचे प्रमाण २०-२५% असते. ते पाण्यात अविद्राव्य असते, असे बरीच वर्षे मानले जात होते. याच्यावर एंझाइमांची क्रिया होत नाही पण उकळते पाणी, अम्ले व क्षार यांमुळे त्याचे जलविद्राव्य अशा जिलेटिनात रूपांतर होते. यात हायड्रॉक्सिप्रोलीन व प्रोलीन या ॲमिनो अम्लांचे प्रमाण इतर ॲमिनो अम्लांपेक्षा जास्त व भरपूर असते पण सिस्टीन, सिस्टाइन व ट्रिप्टोफेन ही ॲमिनो अम्ले नसतात. रेणूभार सु. २,८५,००० इतका असतो.
इलॅस्टीन : शरीरातील संयोजी ऊतकांतील पिवळसर लवचिक तंतूंमध्ये हे प्रथिन आढळते. संधिबंध, रक्तवाहिन्यांच्या भित्ती व जेथे लवचिकता आवश्यक असते अशा ऊतकांत ते असते. पाणी, विरल अम्ले, क्षार व लवणे, अल्कोहॉले यांत ते विरघळत नाही. पेप्सीन व ट्रिप्सीन या एंझाइमांद्वारे त्याचे पचन होते. कोलॅजेनापेक्षा यात हायड्रॉक्सिप्रोलिनाचे प्रमाण कमी आणि ल्युसीन व आयसोल्युसीन यांचे प्रमाण अधिक असते. जिलेटिनामध्ये त्याचे रूपांतर होत नाही.
केराटिने : ही प्रथिने केस, नखे, खूर, पिसे इत्यादींत आढळतात. थंड वा उष्ण पाण्यात ती विरघळत नाहीत. त्यांच्यावर प्रथिन-अपघटक एंझाइमांची विक्रिया होत नाही पण चूर्ण रूपात त्यावर विक्रिया होते. ही सर्वांत स्थिर प्रथिनेआहेत. यांत सिस्टीन व सिस्टाइन यांचे प्रमाण अधिक असते. त्यांचे पचन होत नाही. [⟶ केराटिने].
यांशिवाय रेशमात सेरिसीन व फायब्रोइन ही स्क्लेरोप्रथिने आढळतात. यांपैकी सेरिसीन गरम पाण्यात विरघळते पण फायब्रोइन विरघळत नाही. फायब्रोइनामध्ये ग्लायसीन, ॲलॅनीन, टायरोसीन व सेरीन ही ॲमिनो अम्ले मोठ्या प्रमाणावर आणि इतर ॲमिनो अम्लेअल्प प्रमाणात असतात मात्र त्यांत गंधक नसते. ते लिथियम थायोसायनेटाच्या संहत (प्रमाण जास्त असलेल्या) विद्रावात अथवा क्युप्रिक लवणे व एथिलिन-डाय-अमाइन यांच्या मिश्रणात अंशतः विरघळते.
संयुग्मित प्रथिने : अप्रथिनी गटाशी संलग्न असलेल्या साध्या प्रथिनांना संयुग्मित प्रथिने असे म्हणतात. या प्रकारात न्यूक्लिओप्रथिने, फॉस्फोप्रथिने, क्रोमोप्रथिने, वसाप्रथिने (लिपोप्रोटिने), धातुप्रथिने, कार्बोहायड्रेटयुक्त प्रथिने इत्यादींचा समावेश करतात.
न्यूक्लिओप्रथिने : न्यूक्लिइक अम्ले आणि साधी क्षारकीय प्रथिने (उदा., प्रोटामिन व हिस्टोन) यांच्या लवण संयुगांना न्यूक्लिओप्रथिने असे म्हणतात. यांत न्यूक्लिइक अम्ले हा अप्रथिनी गट असतो. ही मिठाच्या विरल विद्रावात विरघळतात. न्यूक्लिओप्रोटामिने, न्यूक्लिओहिस्टोने आणि काही आरएनए व डीएनए व्हायरस ही न्यूक्लिओप्रथिने महत्त्वाची आहेत. यांचे रेणुभार काही दशलक्ष इतके आहेत. [⟶ न्यूक्लिइक अम्ले].
फॉस्फोप्रथिने : फॉस्फोरिक अम्ल एस्टर बंधाने प्रथिनांशी जोडले जाऊन तयार होणाऱ्या प्रथिनांना फॉस्फोप्रथिने म्हणतात. दुधातील ⇨ केसीन व अंड्यातील व्हिटेलीन ही या प्रकारची सुपरिचित प्रथिने होत. काही विशिष्ट ॲमिनो अम्लांना (सेरीन व थिओनीन) फॉस्फोरिक अम्ल जोडले जाऊन तयार झालेली न्यूक्लिओप्रथिने ही फॉस्फोप्रथिनेच होत. ⇨ यौवनलोपी ग्रंथी व यकृत यांच्या कोशिकांतील केंद्रकांत फॉस्फोप्रथिने असतात.
वर्णप्रथिने : हीम वा इतर रंगद्रव्ये प्रथिनांना जोडली जाऊन तयार झालेल्या संयुगांना वर्णप्रथिने असे म्हणतात. हीमोग्लोबिने, सायटोक्रोमे व फ्लॅव्होप्रथिने ही या प्रकारातील महत्त्वाची प्रथिने असून त्यांतील पहिल्या दोहोत हीम व तिसऱ्यात रिबोफ्लाविन हे अप्रथिनी गट असतात. फायकोबिलीन या अप्रथिनी गटापासून मिळणारी शैवलातील हिरवी बिलिप्रथिने, मेलॅनीन या काळ्या रंगद्रव्याच्या संयोगाने मिळणारी प्राणिज तंतूंतील (उदा., काळी लोकर व केस यांतील) वर्णप्रथिने व कॅरोटिनॉइड या रंगद्रव्याच्या संयोगाने मिळणारे दृष्टिपटलातील जांभळे वर्णप्रथिन ही वर्णप्रथिनांची आणखी काही उदाहरणे होत.
वसाप्रथिने : ही प्रथिने वसायुक्त पदार्थांशी (उदा., लेसिथीन, सेफॅलीन, वसाम्ले इ.) प्रथिने जोडली जाऊन तयार झालेली असतात. ती रक्तद्रव, अंडी, वनस्पतींमधील हरितकण इत्यादींमध्ये आढळतात. सूक्ष्मजंतु-प्रतिजन [⟶ प्रतिजन] व व्हायरस यांतही वसाप्रथिने असतात. हृदयविकार आदि रोगांत ह्या प्रथिनांची जास्त चिकित्सा केली जाते. रंगीत वसाप्रथिने कॅरोटिनॉइडांशी संयुग्मित होऊन तयार होतात. हृदय, मेंदू, मूत्रपिंड, यकृत इत्यादींत आढळणाऱ्या प्रोटिओलिपिडे या संयुगांतही प्रथिन व वसा संयुग्मित रूपात असतात पण ती पाण्यात अविद्राव्य व कार्बनी विद्रावकांत विद्राव्य असून त्यात वसेचे प्रमाण वसाप्रथिनांपेक्षा जास्त असते.
धातुप्रथिने : प्रथिनांच्या हिस्टिडीन, सिस्टाइन इ. ॲमिनो अम्लांच्या पार्श्वशृंखलेशी जड धातवीय (उदा., लोह, कोबाल्ट, तांबे, जस्त, मॅग्नेशियम इ.) आयन जोडलेला असलेल्या प्रथिनांना धातुप्रथिने म्हणतात. रक्तद्रवात ट्रान्सफेरीन (रेणुभार ८४,०००) हे लोहयुक्त व सेऱ्युलोप्लाइमीन (रेणुभार १,५१,०००) हे ताम्रयुक्त प्रथिन असते. फेरिटीन हे यकृत व प्लीहा (पानथरी) यांमध्ये आढळणारे लोहयुक्त प्रथिन आहे. हिरव्या वनस्पतींत आणि काही प्रकाशसंश्लेषी (प्रकाश ऊर्जेचा उपयोग करून कार्बन डाय-ऑक्साइड व पाणी यांच्यापासून कार्बनी संयुगे तयार करणारे) व नायट्रोजन स्थिर करणाऱ्या सूक्ष्मजंतूंत फेरिडॉक्सिने ही लोहयुक्त धातुप्रथिने असतात. एरिथ्रोक्युप्रेइन हे ताम्रयुक्त प्रथिन लाल रक्तकोशिका, यकृत व मेंदू यांत आढळते. घोड्याच्या मूत्रपिंडातील मेटॅलोथायोनिनामध्ये जस्त व कॅडमियम असते, तर ट्यूनिकेट या सागरी अपृष्ठवंशी (पाठीचा कणा नसलेल्या) प्राण्यात व्हॅनेडियमयुक्त प्रथिन असते. हीमयुक्त वर्णप्रथिनांत लोह असल्यामुळे त्यांचा धातुप्रथिनांमध्येही समावेश करतात.
कार्बोहायड्रेटयुक्त प्रथिने : कार्बोहायड्रेटांशी साधी प्रथिने संयुग्मित होऊन तयार झालेल्या संयुगांचे म्युकोप्रथिने व ग्लायकोप्रथिने (किंवा ग्लुकोप्रथिने) हे प्रकार महत्त्वाचे आहेत. कार्बोहायड्रेटांचे प्रमाण ३ ते ४ टक्क्यांहून जास्त असलेल्या प्रथिनांना म्युकोप्रथिने आणि ३ टक्क्यांहून कमी असलेल्यांना ग्लायकोप्रथिने किंवा नुसतेच प्रथिने असे संबोधण्यात येते. काही म्युकोप्रथिनांत कार्बोहायड्रेटाचे प्रमाण २० टक्क्यांहूनही जास्त असते. म्युकोप्रथिनांतील कार्बोहायड्रेटापेक्षा ग्लायकोप्रथिनातील कार्बोहायड्रेट सामान्यतः जास्त दृढपणे बंधित असते (म्युकोप्रथिने व ग्लायकोप्रथिने यांच्या व्याख्यांमध्ये अद्यापही संदिग्धता आढळते).
म्युकोप्रथिने ही साधी प्रथिने व म्युकोपॉलिसॅकॅराइडांशी (उदा., हायलुरॉनिक अम्ल, काँड्राइटीन सल्फेटे) संयोग पावून तयार झालेली असतात. यांत मोठ्या प्रमाणावर N – ॲसिटिलीकृत हेक्झोसामीन (४ टक्क्यांपेक्षा जास्त), तसेच कमीअधिक प्रमाणात युरोनिक अम्ल, सिॲलिक अम्ल यांसारखी संयुगे व मोनोसॅकॅराइडे असतात. पाण्यात विरघळणारी म्युकोप्रथिने रक्तद्रव, अंड्यातील पांढरा बलक व मानवी मूत्र यांत आढळतात. त्यातील म्युकोपॉलिसॅकॅराइडे हेक्झोसामीन व हेक्झोज शर्करा या रूपांत असतात. पाण्यात न विरघळणारी म्युकोप्रथिने अंड्यातील पांढरा बलक, डोळ्यातीलसांद्रजलपिंड इत्यादींत आढळतात. म्युकोप्रथिने ही अतिशय श्यान (दाट) व बुळबुळीत असून लाळ, जठररस व इतर प्राणिज स्त्रावांत असतात. उपास्थी (कूर्चा), सांधे व कंडरा यांत वंगणासारखे कार्य करणाऱ्या द्रवात ती आढळतात. संयोजी ऊतकांतील आधारद्रव्यात म्युकोप्रथिने हे महत्त्वाचे घटक असतात. ती कंडरा, अस्थी व उपास्थी यांत अनुक्रमे टेंडोम्यूकॉइड, ॲसिओम्यूकॉइड व काँड्रोम्यूकॉइड म्हणून उपस्थित असतात. बरीच जनन ग्रंथिपोषक हॉर्मोने म्युकोप्रथिने असतात. [⟶ हॉर्मोने].
साधित प्रथिने : अम्ले, क्षार व रासायनिक विक्रियाकारक यांच्याशी प्रथिनांची विक्रिया झाल्यास यांच्या रेणूची पुनर्रचना होते. उष्णता, जोराने हालविणे वा तत्सम भौतिक प्रेरणांमुळेही अशी पुनर्रचना होते. त्यामुळे मिळणाऱ्या प्रथिनांना साधित वा विकृत प्रथिने असे म्हणतात. रासायनिक वा भौतिक कारकांमुळे प्रथिनाच्या मोठ्या रेणूचे अनियमित तुकडे होतात. अशी विक्रिया जसजशी पुढे प्रगत होत जाते तसतसे रेणूचे आणखी तुकडे होतात. मोठ्या तुकड्यांना प्रोटिओजे व लहानांना पेप्टोने असे म्हणतात. पेप्टाइड बंधांनी जोडल्या गेलेल्या व सापेक्षतः कमी ॲमिनो अम्ले असलेल्या लहान शृंखलांना पेप्टाइडे असे म्हणतात.
एंझाइमे आणि हॉर्मोने ही बहुतकरून प्रथिने असल्यामुळे एंझाइम प्रथिने, हॉर्मोने प्रथिने असेही वेगेवेगळे गट होऊ शकतात.
एंझाइम प्रथिने : यूरिएज व पेप्सीन ही एंझाइमे शुद्ध प्रथिने आहेत, असे प्रथमच आढळून आले. या एंझाइम प्रथिनांत अप्रथिनी घटक आढळत नाहीत. तथापि सर्वच एंझाइमे ही शुद्ध वा संयुग्मित प्रथिने आहेत की नाहीत, हे माहित झालेले नाही. एंझाइमे ही उत्प्रेरकी (विक्रियेत भाग न घेता विक्रियेची गती वाढविण्याचा गुणधर्म असणारी) प्रथिने आहेत. संयुग्मित प्रथिनांतील अप्रथिनी घटक हा उत्प्रेरकी असतो. ऑक्सिडोरिडक्टेजे, ट्रान्सफरेजे, हायड्रोलेजे इ. एंझाइम प्रथिनगट ज्ञात आहेत. कार्यकारी कोशिकेतील सु. ९०% प्रथिने एंझाइमांच्या स्वरूपात असतात.
हॉर्मोन प्रथिने :⇨ अंतःस्त्रावी ग्रंथीपासून मिळणारी काही हॉर्मोने ही प्रथिने आहेत. ⇨ अवटू ग्रंथी, ⇨ अग्निपिंड, ⇨ पोष ग्रंथी, यांतून स्त्रवणारी काही हॉर्मोने प्रथिने असतात. यांशिवाय ब्रॅडिकायनीन, गॅस्ट्रिन, सिक्रिटीन, पेप्सीन, कालिक्रिइन इ. पेप्टाइडे हॉर्मोनासारखेच कार्य करतात. [⟶ हॉर्मोने].
संरचना : प्रथिने ही अनेक ॲमिनो अम्ले एकत्रित येऊन बनलेली असतात. निसर्गात जरी शंभराहून अधिक ॲमिनो अम्ले आढळत असली, तरी प्रथिनांत प्रामुख्याने एकवीस ॲमिनो अम्ले असतात. त्यांपैकी ग्लायसीन, ॲलॅनीन, व्हॅलिन, ल्युसीन, आयसोल्युसीन, सेरीन, थ्रिओनीन, ॲस्परजिन, ग्लुटामीन, सिस्टीन, सिस्टाइन, मिथिओनीन, फिनिल-ॲलॅनीन, टायरोसीन, ट्रिप्टोफेन व प्रोलीन ही अम्ले उदासीन ॲस्पार्टिक व ग्लुटामिक ही अम्लीय आणि लायसीन, आर्जिनीन व हिस्टिडीन ही क्षारकीय आहेत. प्रथिनाच्या रेणूमध्ये ही ॲमिनो अम्ले एकमेकांशी पेप्टाइड बंधाने (-CONH-) जोडलेली असतात. पेप्टाइड साखळीच्या वा बंधाच्या एका टोकाला सुटा ॲमिनो गट, तर दुसऱ्या टोकाला सुटा कार्बॉक्सिल गट (COOH) असतो. संपूर्ण पेप्टाइड संरचना लिहिताना सुटा ॲमिनो गट असलेली ॲमिनो अम्ले साखळीच्या डाव्या बाजूला दाखवितात. याला पेप्टाइडाचे नायट्रोजन-अंत्यस्थान असे म्हणतात. सुटा कार्बॉक्सिल गट असलेली ॲमिनो अम्ले साखळीच्या उजव्या बाजूला दाखवितात. याला पेप्टाइडाचे कार्बन-अंत्यस्थान असे म्हणतात. बऱ्याचशा पेप्टाइड साखळ्यांत साधारण १०० ॲमिनो अम्ल घटक असतात.
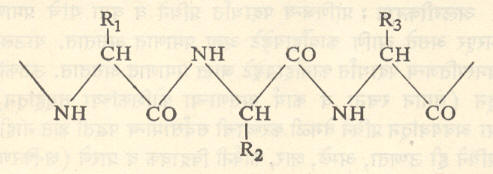
प्रथिनातील ॲमिनो अम्लांचा क्रम ठरविण्याची पद्धत : संहत हायड्रोक्लोरिक अम्लाने प्रथिनाचे ॲमिनो अम्लांत अपघटन करता येते. वर्णलेखन तंत्राच्या साहाय्याने मग त्या प्रथिनातील ॲमिनो अम्ले व त्यांचे एकंदर प्रमाण ठरवितात.
पेप्टाइड साखळीतील ॲमिनो अम्लांचा क्रम नक्की करताना त्या साखळीतील ॲमिनो अम्ले क्रमवार सुटी केली जातात. पेप्टाइड साखळीतील नायट्रोजन-अंत्यस्थानी असलेला ॲमिनो अम्लाचा मुक्त ॲमिनो गट व फिनिल आयसोथायोसायनेट यांचे संयुग्मन करतात व सौम्य जलीय विच्छेदनाने ते ॲमिनो अम्ल वेगळे करून वर्णलेखनाने ते ॲमिनो अम्ल ओळखतात. अशा तऱ्हेने या प्रक्रियेची पुनरावृत्ती करून पेप्टाइड साखळीतील ॲमिनो अम्ले व त्यांचा क्रम ओळखतात. यालाच पी. एडमन या शास्त्रज्ञांच्या नावावरून ‘एडमन निम्नीकरण’ म्हणतात. पेप्टाइड साखळीत जर ३०-३५ हून जास्त ॲमिनो अम्ले असतील, तर या पद्धतीने ॲमिनो अम्लांचे क्रम ठरविणे कठीण जाते. अशा वेळी प्रथिनावर ट्रिप्सिन या एंझाइमाची विक्रिया करतात. लायसीन आणि आर्जिनीन या ॲमिनो अम्लांच्या कार्बॉक्सिल गटाने तयार झालेल्या बंधावरच फक्त ट्रिप्सिनाची विक्रिया होते. अशा तऱ्हेने सुट्या झालेल्या साखळ्यांचे एडमन निम्नीकरण करून निरनिराळ्या साखळ्यांतील ॲमिनो अम्लांचा क्रम शोधला जातो. उरलेल्या पेप्टाइड साखळ्यांवर दुसऱ्या विशिष्ट एंझाइमांची विक्रिया करून त्यांचे अपघटन केले जाते. उदा., कायमोट्रिप्सीन हे एंझाइम मुख्यतः टायरोसीन, फिनिल-ॲलॅनीन आणि ट्रिप्टोफेन या ॲमिनो अम्लांनी तयार झालेल्या पेप्टाइड बंधाचे अपघटन करते. फ्रेडरिक सँगर यांनी १९४५ मध्ये दोन वा अधिक प्रथिन-अपघटकी एंझाइमांचा वापर करुन मिळालेल्या निष्कर्षावरून इन्शुलिनामधील ॲमिनो अम्लांचा क्रम निश्चित केला. फिनिल आयसोथायोसायानेटाऐवजी डायनायट्रोफ्ल्युओरोबेंझीन वापरूनही ॲमिनो अम्लांचा क्रम ठरविता येतो. स्वयंचलित ॲमिनो अम्ल विश्लेषक यंत्राचा १९५८ मध्ये शोध लागल्यापासून प्रथिनातील ॲमिनो अम्लांचे स्वरुप समजणे अतिशय सुलभ झाले आहे.
विश्लेषणात्मक आणि संश्लेषणात्मक (घटक एकत्र आणून संयुग मिळविण्याच्या) प्रक्रियांनी पेप्टाइड साखळ्यांतील ॲमिनो अम्लांची क्रमवार माहिती होते. या संरचनेस प्रथिनाची प्राथमिक संरचना म्हणतात.
पेप्टाइड साखळीतील एकमेकांजवळील कार्बन व नायट्रोजन अणू त्यांमधील बंधकोनामुळे एका सरळ रेषेत नसतात. हा बंधकोन सु. ११०° असतो. तसेच प्रत्येक नायट्रोजन व कार्बन अणू काही प्रमाणात चक्राकृती फिरतात, त्यामुळे साखळीला ठराविक प्रमाणात लवचिकपणा येतो. ग्लायसीन सोडून बहुतेक सर्व ॲमिनो अम्ले असममित (चार वेगवेगळ्या अणूंना वा गटांना जोडलागेलेला कार्बन अणू असलेली) ॲमिनो अम्ले असतात. त्यामुळे पेप्टाइड साखळ्यांची असममित मळसूत्री आकार घेण्याची प्रवृत्ती होते. काही तंतुमय प्रथिनांत सरळ मळसूत्री आसाभोवती लांबट मळसूत्रे असतात. पेप्टाइड साखळ्यांच्या सर्वसाधारण गुणधर्मांमुळे प्रथिनांना संरचनात्मक गुणधर्म प्राप्त होतात. या परिणामामुळे निर्माण होणाऱ्या प्रथिनांच्या संरचनेस द्वितीयक संरचना म्हणतात.
प्रथिनांची तृतीयक संरचना पुढील प्रकारच्या बंधावर अवलंबून असते. प्रथिनांत ॲमिनो अम्लांच्या पार्श्वशाखा (पार्श्वशृंखला) असतात. त्यांतील काही साखळ्यांत धन, तर काहींत ऋण विद्युत् भारित गट असतात. पार्श्वशाखेतील कार्बन अणूंची संख्या ही तिच्यातील ॲमिनो अम्लानुसार असते. ग्लायसीन असल्यास पार्श्वशाखेत शून्य कार्बन अणू असतात, तर ट्रिप्टोफेन असल्यास नऊ कार्बन अणू असतात. धन भारित पार्श्वशाखा ऋण भारित पार्श्वशाखांकडे आकर्षित होते, तर समान भारित शाखा एकमेकींपासून दूर होऊ पाहतात. ग्लुटामिक अम्ल वा ॲस्पार्टिक अम्ल यांच्या ऋण भारित व आर्जिनीन व लायसीन यांच्या धन भारित प्रेरणा यांमुळे तयार होणाऱ्या बंधांना ‘लवण सेतू’ असे म्हणतात. संलग्न असलेल्या पेप्टाइड साखळ्यांतील हायड्रोजन व ऑक्सिजन यांचे हायड्रोजन बंध तयार होऊन साखळ्या एकमेकींकडे आकर्षिल्या जातात. व्हॅलीन, ल्युसीन, आयसोल्युसीन, फिनिल-ॲलॅनीन इ. ॲमिनो अम्लांतील अध्रुवीय [ज्यांना स्थिर परिणामी विद्युत् द्विध्रुव परिबल नसते अशा ⟶ रेणवीय भौतिकी] पार्श्वशाखांत आकर्षण होऊन पाण्याच्या रेणूचे स्थलांतर होते. याला जलरोधी परस्परक्रिया असे म्हणतात. काही प्रथिनांत सिस्टीन या ॲमिनो अम्लाचे प्रमाण जास्त असते. त्यातील डायसल्फाइड (-S-S-) या बंधावरही पेप्टाइड साखळीची घडण अवलंबून असते. एका साखळीतील सिस्टाइन (सिस्टिनाचा अर्धा भाग) संलग्न असलेल्या दुसऱ्या साखळीतील सिस्टाइनाशी डायसल्फाइड बंधाने जोडले जाते. या डायसल्फाइड बंधाचे क्षपण करून [हायड्रोजनाचा समावेश करून ⟶ क्षपण] दोन सल्फाहायड्रिल (-SH) गटांत रूपांतर केले, तर प्रथिनांच्या संरचनेत मोठ्या प्रमाणावर बदल होऊन डायसल्फाइड बंध सुटा होतो व पेप्टाइड साखळ्या अलग होतात.
मानवी हीमोग्लोबिनामध्ये दोन आल्फा व दोन बीटा अशा एकंदर चार पेप्टाइड साखळ्या असतात. हीमोग्लोबिन हे चतुर्वारिक (चार साधे व एकसारखे रेणू एकत्र येऊन तयार झालेला रेणू असलेले संयुग) आहे पण चारही अपघट सहसंयुजी बंधाने जोडलेले नसतात, तर जलरोधी परस्परक्रियेने व हायड्रोजन बंधाने एकमेकांशी विशिष्टपणे जोडले जाऊन हीमोग्लोबिनाचा रेणू तयार होतो. अशा संरचनेला प्रथिनाची चतुर्थक संरचना असे म्हणतात. काही प्रथिनांची विशिष्ट संरचना उपघटक सहसंयुजी बंधाने जोडल्यामुळेही तयार झालेली असते.
विकृतीकरण : जर अंड्याच्या पांढऱ्या भागाचा विद्राव उकळला, तर त्यामधील प्रथिनांचे (अल्ब्युमीन व ग्लोब्युलीन) किलाटन होऊन ती ज्या मूळ उदासीन विद्रावांत विद्राव्य होती, त्यात अविद्राव्य होतात. अशा प्रक्रियेला प्रथिनांचे विकृतीकरण असे म्हणतात. हा विद्राव थंड केला, तरी प्रथिने अविद्राव्यच राहतात. अशा प्रथिनाची प्राथमिक संरचना मूळच्या सारखीच असते. बऱ्याच वेळा प्रथिनाचा रेणुभार तोच राहतो. कधीकधी विकृतीकरणात प्रथिनाचे दोन वा अधिक पॉलिपेप्टाइड साखळ्यांत अपघटन होते. तसेच विकृतीकरणास पेप्टाइड साखळ्या अलग न होता प्रथिनातील अनेक कमजोर हायड्रोजन बंध सुटे होतात आणि मूळ आखीव संरचना नष्ट होऊन अव्यवस्थित व स्वैर अशी प्रथिनाची संरचना होते. तापमान वाढविले असता विद्युत् भारित गट आणि अध्रुवीय गट यांतील परस्पर आकर्षणाचा दुर्बलप्रेरणा नष्ट होतात. त्यामुळे प्रथिनाची तृतीयक संरचना लोप पावते. असे विकृतिकरण अव्युत्क्रमी (मूळ स्थिती प्राप्त न होणारे) असते तथापि व्युत्क्रमी प्रकाराचेही विकृतिकरण आढळते. प्रथिनाच्या विरल विद्रावाचे विकृतीकरण जलद होते.
उष्णतेखेरीज क्ष-किरण, जंबुपार (दृश्य वर्णपटातील जांभळ्या रंगाच्या पलीकडील अदृश्य) किरण, उच्च दाब, यांत्रिक साधनांच्या साहाय्याने जोराने हालविणे व तत्सम भौतिक प्रेरणा या भौतिक कारकांमुळे विकृतीकरण होते. प्रकाशसंवेदी पदार्थाच्या उपस्थितीत दृश्य प्रकाशामुळेही विकृतीकरण होते.
अम्ले, क्षार, ऑक्सिडीकारक वा क्षपणकारक तसेच अल्कोहॉल, ॲसिटोन व इतर काही कार्बनी विद्रावक यांच्याबरोबर प्रथिनांची विक्रिया केल्यासही प्रथिनांचे विकृतीकरण होते. प्राथमिक संरचनेला धक्का न लावता द्वितीयक वा तृतीयक संरचनेवर परिणाम करणारी विकृतीकारकाची विक्रिया वैशिष्ट्यपूर्ण आहे. यासाठी यूरिया व ग्वानिडिनियम क्लोराइड हे विक्रियाकारक जास्त प्रमाणात वापरतात. यांना पेप्टाइड बंधांचे फार आकर्षण असून ते प्रथिनातील हायड्रोजन बंध आणि धन भारित व ऋण भारित पार्श्वशृंखलांचे लवण सेतू तोडतात व प्रथिमाची तूतीयक संरचना मोडतात. विद्रावातून विकृतीकारक काढून टाकल्यास काही प्रथिने मूळ स्थितीत परत येतात. प्रथिनांतील डायसल्फाइड बंधांचे क्षपण करून वा अध्रुवीय गटांतील परस्पर आकर्षण शक्तीवर कार्बनी विद्रावकांचा परिणाम होऊन प्रथिनांचे विकृतीकरण होते. विकृतीकरण होताना प्रथिनांच्या रेणूतील बदल हे सारखेच असतात असे नाही, पण प्रथिनांच्या जैव क्रियाशीलतेचा लोप (उदा., एंझाइम वा हॉर्मोन म्हणून कार्य करण्याच्या अथवा हीमोग्लोबिनाच्या ॲक्सिजन वाहून नेण्याच्या गुणधर्माच्या लोप) होणे हा समान गुणधर्म सर्व प्रकारच्या विकृतीकरणांत आढळतो.
ट्रिप्सीन या एंझाइमाची क्रिया काही प्रथिनांवर प्रथम होत नाही, तथापि ती विकृत झाल्यावर ट्रिप्सिनाकडून सहज जलीय विच्छेदित होतात. सुरुवातीला ट्रिप्सीन पेप्टाइड बंधांपर्यंत पोहोचू शकत नाही पण विकृतीकरणानंतर ते पेप्टाइड बंधांवर कार्य करते व बंध उघडे पडतात. तसेच विकृतीकरण केल्यानंतर प्रथिनांवर रासायनिक रंग-विक्रिया केल्यास टायरोसीन, आर्जिनीन व हिस्टिडीन या ॲमिनो अम्लांबाबत त्या जास्त तीव्र रंग देतात [⟶ ॲमिनो अम्ले]. विक्रियेत भाग घेणारे प्रथिनातील भाग विकृतीकरणामुळे मोकळे होतात व त्यामुळे वरील परिणाम दिसून येतो.
एम्. एल्. ॲन्सन व ए. ई. मर्स्की यांनी हीमोग्लोबिनावरील आपल्या संशोधनाद्वारे विकृतीकरण व्युत्क्रमी असू शकते, असे प्रथम दाखविले. उदासीन सोडियम सॅलिसिलेटामध्ये विरघळवून हीमोग्लोबिनाचे विकृतीकरण करता येते. त्यामुळे ज्या लवण विद्रावात मूळ हीमोग्लोबिन विद्राव्य असते, त्यात विकृत हीमोग्लोबिन अविद्राव्य होते तसेच ट्रिप्सिनाकडून त्याचे पचन होते. ॲलिसिलेट काढून टाकल्यानंतर विकृतीकरणाचे पूर्णपणे व्युत्क्रमण होते म्हणजे हीमोग्लोबिन पुन्हा विद्राव्य बनते व त्याचे ट्रिप्सिनाचे पचन होत नाही. आतापावेतो काही थोड्याच प्रथिनांच्या बाबतीत पूर्णपणे वा अंशतः व्युत्क्रमी विकृतीकरण शक्य झालेले आहे.
अलगीकरण : प्राणिजन्य पदार्थांत प्रथिने व वसा यांचे प्रमाण भरपूर असते आणि कार्बोहायड्रेटे अल्प प्रमाणात असतात. याउलट वनस्पतिजन्य पदार्थांत कार्बोहायड्रेटे जास्त प्रमाणात असतात. ऊतकांतून (समान रचना व कार्य असणाऱ्या कोशिकांच्या समूहांतून) वा अवयवांतून प्रथिने वेगळी करण्याची सर्वसामान्य पद्धती ज्ञात नाही. प्रथिने ही उष्णता, अम्ले, क्षार, कार्बनी विद्रावक व प्रारणे (क्ष-किरण, दृश्य प्रकाश इ. तरंगरूपी ऊर्जा) यांना संवेदनशील असल्याने कार्बनी पदार्थांच्या शुद्धीकरणाच्या रासायनिक पद्धती प्रथिनांसाठी वापरता येत नाही. सामान्यतः पुढील पद्धतींचा वापर प्रथिने वेगळी करण्यासाठी करण्यात येतो.
लवण अवक्षेपण : (अवक्षेपण म्हणजे न विरघळणाऱ्या साक्याच्या रूपात मिळविणे). अमोनियम सल्फेट, सोडियम सल्फेट वा मॅग्नेशियम सल्फेट यांचा सौम्य विद्राव प्रथिन विद्रावात मिसळला, तर प्रथिने तशीच राहतात. पाण्याचा विद्युत् अपार्यता स्थिरांक अती उच्च असल्यामुळे प्रथिनाच्या रेणूच्या विद्युत् भारित भागाभागांमधील परस्परक्रिया रोखली जाते पण वरील लवणांच्या संहत विद्रावात तो स्थिरांक बराचसा कमी होऊन प्रथिन रेणूच्या भागाभागांमधील परस्परक्रिया वाढते. याचा परिणाम म्हणजे प्रथिनांचा अवक्षेप सुटा होतो.
समविद्युत् भार बिंदू अवक्षेपण : समविद्युत् भार pH मूल्य (विद्युत् भाराच्या दृष्टीने उदासीन असलेल्या म्हणजे अम्ल व क्षारक समूहाची शक्ती सारखी असते ते pH मूल्य) असलेल्या विद्रावात प्रथिनावरील धन भार व ऋण भार सारखेच असतात. प्रथिनाच्या संरचनेत असलेल्या ॲमिनो अम्लांच्या एकंदर प्रमाणावर त्या प्रथिनाचा समविद्युत् भार बिंदू अवलंबून असतो. प्रत्येक प्रथिनाचा हा बिंदू वेगवेगळा असतो. या pH मूल्याला प्रथिनाची विद्राव्यता अत्यंत कमी असते. मेटा प्रथिने, केसीन इ. प्रथिनांचे या pH मूल्याला सहज अवक्षेपण होते, तर इतर प्रथिनांसाठी योग्य असा विक्रियाकारक वापरून त्यांचे अवक्षेपण करणे या वेळी शक्य होते.
लवणतृप्ती व अपोहन : प्रथिन विद्रावाची योग्य त्या प्रमाणात लवणतृप्ती करून प्रथिनाचा अवक्षेप मिळविता येतो. ग्लोब्युलीन, केसीन, जिलेटीन इ. प्रथिनांच्या विद्रावांची अमोनियम सल्फेटाने अर्धतृप्ती केली असताना त्या त्या प्रथिनाचा अवक्षेप मिळतो. अल्ब्युमिनाचा अवक्षेप मिळविण्यासाठी विद्रावाची लवणाने पूर्ण तृप्ती करावी लागते. विद्रावातून वेगळ्या काढलेल्या प्रथिनाच्या अवक्षेपाबरोबर लवणेही असतात. प्रथिनांपासून लवणे व इतर विद्युत् विच्छेद्य पदार्थ (विद्युत् प्रवाह विद्रावातून जाऊ दिल्यास ज्यातील घटक अलग होतात असे पदार्थ) व लहान रेणू वेगळे करण्यासाठी ⇨ अपोहन तंत्र वापरतात.
कार्बनी विद्रावकांच्या साहाय्याने अवक्षेपण : प्रथिनांच्या विद्रावात ॲसिटोन, एथॅनॉल वा अल्कोहॉल यांसारखा कार्बनी विद्रावक मिसळला असता द्रव माध्यमाचा विद्युत् अपार्यता स्थिरांक कमी होतो. त्यामुळे पाण्याची विद्राव्यता कमी होऊन प्रथिन रेणूच्या भागाभागांमध्ये परस्परक्रिया होऊन त्यांचे अवक्षेपण होते.
प्रथिन लवणे व इतर जटिल संयुगे : बऱ्याच आयनांची प्रथिनांबरोबर अविद्राव्य लवणे तयार होतात. प्रथिनांच्या अवक्षेपणासाठी याचा चांगलाच उपयोग होतो. विद्रावातून प्रथिने वेगळी करण्यासाठी फॉस्फोटंगस्टिक, ट्रायक्लोरोॲसिटिक, सल्फोसॅलिसिकिल, पिक्रिक ही अम्ले सर्वसाधारणपणे वापरतात. समविद्युत् भार बिंदूच्या अम्लीय माध्यमात ऋणायनी प्रथिनांची धनायनी (ऋण विद्युत् भारित असलेल्या व विद्युत् विच्छेदनात धनाग्राकडे जाणाऱ्या आयनांच्या स्वरूपातील) अम्लांबरोबर अविद्राव्य लवणे तयार होतात, तर क्षारीय माध्यमात प्रथिने धनायनी होतात. या प्रथिनांचे अवक्षेपण करण्यासाठी पारा, तांबे, चांदी, शिसे, जस्त, बेरियम इ. जड धातवीय आयनांचा उपयोग करतात.
अधिशोषण : कित्येक धन वा द्रव पदार्थांच्या अंगी त्यांच्या पृष्ठभागाशी संपर्क करणाऱ्या दुसऱ्या एखाद्या घन, द्रव वा वायुरूप पदार्थातील रेणू, अणू वा आयन यांसारखे घटक आकृष्टकरून घेऊन स्वतःच्या पृष्ठभागाशीसाचवून ठेवण्याचा गुणधर्म असतो. अशा पदार्थांना अधिशोषक व त्यांच्या पृष्ठभागाशी साचवून ठेवण्याच्या गुणधर्माला ⇨ अधिशोषण म्हणतात. प्रथिनांच्या शुद्धीकरणासाठी ही पद्धत वापरतात. अधिशोषकाच्या पृष्ठभागावर प्रथिने शोषली जातात. योग्य त्या कारकाचा उपयोग केल्यास, त्या कारकामुळे प्रथिन पृष्ठभागापासून सुटे होते व कारकच पृष्ठभागावर राहतो. pH मूल्य, आयनी प्रबलता व अधिशोषण यांचा योग्य उपयोग करून प्रथिनांच्या मिश्रणातून शुद्ध प्रथिन घटक मिळवितात. या पद्धतीने अनेक एंझाइमे व हॉर्मोने मिळविण्यात आली आहेत. केओलीन, कॅल्शियम फॉस्फेट जेल व कित्येक आयन-विनिमयक [आयनांची अदलाबदल करणारे पदार्थ ⟶ आयन-विनियम] अधिशोषक म्हणून वापरण्यात आले आहेत.
प्रतिप्रवाही वितरण : एका विद्रावकातील (उदा., पाणी) प्रथिनांचा विद्राव दुसऱ्या अविद्राव्य विद्रावकाबरोबर (उदा., हेप्टेन) क्रमशः निष्कर्षित करतात. मिळालेले निरनिराळे भाग वेगवेगळे ठेवले जातात. नंतर त्यांचे पृथक्करण करून परीक्षण केले जाते. प्रथिनांच्या मिश्रणातून घटक विभक्त करण्यासाठी ही पद्धत वापरतात.
प्रतिरोधक अवक्षेपण : एखाद्या प्राण्यामध्ये बाह्य (म्हणजे त्या प्राण्यात नसलेली) प्रथिने टोचली असता त्या प्राण्याच्या शरीरात विशिष्ट प्रतिपिंड तयार होतात. उदा., सशाला ठराविक दिवसांच्या अंतराने जर अंड्याच्या पांढऱ्या बलकाची अंतःक्षेपणे (इंजेक्शने) दिली, तर त्या सशाच्या रक्तात एक विशिष्ट गुणधर्म येतो. तो म्हणजे अंड्याच्या पांढऱ्या बलकाचा सशाच्या रक्तद्रवाशी अल्प प्रमाणात जरी संयोग झाला, तरी अवक्षेप तयार होतो. असा अवक्षेप इतर प्रथिनांबरोबर मिळत नाही. या विशिष्ट गुणधर्मामुळे प्रथिनांचा शोध घेण्यासाठी वा मापन करण्यासाठी या सूक्ष्मग्राही पद्धतीचा उपयोग करतात.
वेगळे केलेले प्रथिन शुद्ध व अशुद्ध आहे हे विद्युत् संचारण, जेल विसरण [जेलातील म्हणजे कलिल विद्राव्याच्या एका अवस्थेतील रेणू वा आयन स्वयंस्फूर्त गतीमुळे वा विखुरले गेल्यामुळे एकमेकांत मिसळले जाण्याची क्रिया ⟶ जेल], अतिकेंद्रोत्सारित्र [भिन्न घनतेच्या व एकमेकांत न मिसळणाऱ्या द्रवांच्या मिश्रणातील निरनिराळे घटक वेगळे करणाऱ्या आणि गुरुत्वाकर्षणाच्या सु. दोन लक्ष पट केंद्रोत्सारी प्रेरणा निर्माण करणारे यंत्र ⟶केंद्रोत्सारण]), जैव क्रियाशीलता इ. तंत्रांच्या कसोट्या वापरून ठरविण्यात येते.
भौतिक-रासायनिक गुणधर्म : निरनिराळ्या प्रथिनांच्या गुणधर्मांत अतिशय विविधता आढळते. काही प्रथिनांच्या (उदा., रक्तातील तेजस्वी तांबड्या रंगाचे हीमोग्लोबिन) रेणूंत रंगद्रव्य असते. इतर प्रथिने रंगहीन असतात. शुद्ध प्रथिने सामान्यतः चवहीन असतात. तथापि त्यांच्या जलीय विच्छेदनाने मिळणारी संयुगे (प्रोटिओजे, पेप्टोने, पेप्टाइडे, ॲमिनो अम्ले) प्रामुख्याने कडू असतात. शुद्ध प्रथिने गंधहीन असतात. काही प्रथिने (उदा., केस, लोकर, रेशीम) लांब, बारीक तंतूंच्या रूपात असून ती सामान्य विद्रावकांत पूर्णपणे अविद्राव्य आहेत. काही (उदा., अंड्याच्या पांढऱ्या बलकातील अल्ब्युमीन) पाण्यात अतिशय विद्राव्य आहेत पण तापविल्यास घनरूप होतात. स्नायुकोशिकांतील प्रथिनांपासून बनलेलेतंतू कोशिका उद्दीपित केल्यास आकुंचित वा शिथिल होतात. प्रथिनांना उष्णता दिल्यास ती प्रथम तपकिरी होतात व नंतर ती करपून त्यांना जळणाऱ्या केसासारखा वा पिसासारखा विशिष्ट वास येतो. उष्णता, प्रारणे, अम्ले, क्षारक व कार्बनी विद्रावक यांना प्रथिने संवेदनाशील आहेत. जड धातूंच्या लवणांनी प्रथिनांचे अवक्षेपण होते. काही रंजकद्रव्याबरोबर (उदा., पिक्रिक अम्ल, फ्लाव्हिॲनिक अम्ल) प्रथिने संयुग्मित होतात. तांबे व जस्त यांच्याबरोबर प्रथिने बंधित होतात व हा प्रथिनांचा महत्त्वाचा गुणधर्म मानला जातो.
रेणुभार : रासायनिक संयुगाचा रेणुभार ठरविण्याच्या सर्वसाधारण पद्धती [⟶ रेणुभार] प्रथिनांबाबत उपयोगी पडत नाहीत, कारण प्रथिनांचे रेणुभारफार मोठे असतात. त्यामुळे दिलेला रेणुभाराचा आकडा हा त्या विशिष्ट प्रथिनाचा अंदाजी रेणुभारच असतो. हीमोसायानीन या ताम्रयुक्त श्वसन प्रथिनाचा (ऑक्सिजन वाहून नेणाऱ्या प्रथिनाचा) रेणुभार कित्येक लाख असतो.
प्रथिनाच्या रेणूत समजा ॲमिनो अम्लांपैकी एकच ॲमिनो अम्ल किंवा लोह, तांबे किंवा दुसऱ्या एखाद्या मूलद्रव्याचा फक्त एकच अणू असेल, तर त्या प्रथिनाचा रेणुभार सहज काढता येतो. उदा., १०० ग्रॅ. मायोग्लोबिनामध्ये ०·३४ ग्रॅ. लोह असते. लोहाचा अणुभार ५६ आहे. त्यामुळे
|
मायोग्लोबिनाचा रेणुभार |
५६ X १०० |
= सु. १६,५०० |
|
०·३४ |
असतो, असे सांगता येते. रेणुभार प्रत्यक्ष मोजला असतानासुद्धा तो तेवढाच येतो. मायोग्लोबिनाप्रमाणेच हीमोग्लोबिनामध्ये लोहाचे प्रमाण १०० ग्रॅ. मध्ये ०·३४ ग्रॅ. असते पण हीमोग्लोबिनाच्या रेणूत लोहाचे चार अणू असतात असे दिसून आले आहे. त्यावरून हीमोग्लोबिनाचा रेणुभार ४X १६,५०० = ६६,००० असतो, हे सांगता येते.
प्रथिनांचे विद्राव कलिलधर्मी [⟶ कलिल] असल्याने त्यांचे रेणुभार काढण्यासाठी अतिकेंद्रोत्सारित्राचा उपयोग करतात. या यंत्राच्या साहाय्याने प्रथिन विद्रावाला दर मिनिटाला ६०,००० फेरे इतका वेग देता येतो. या वेगामुळे प्रथिन रेणूवर असलेल्या गुरुत्वीय प्रेरणेच्या २,००,००० पटींनी अधिक केंद्रोत्सारी प्रेरणा कार्यान्वित होते. या केंद्रोत्सारी प्रेरणेमुळे केंद्रोत्सारी नळीच्या तळाशी बसणाऱ्या विद्रावातील प्रथिनाच्या कणांचा वेग (१) वापरण्यात आलेली शक्ती, (२) कणाचे आकारमान, आकार व घनता आणि (३) विद्रावकाची घनता व श्यानता यांवर अवलंबून असतो. मोठे रेणू लहानरेणूंपेक्षा जास्त वेगाने साका धरतात. अतिकेंद्रोत्सारित्रात रेणुभाराच्या प्रमाणात प्रत्येक घटक तळाशी साचतो. जास्त रेणुभाराची प्रथिने तळाशी तर कमी रेणुभाराची प्रथिने सर्वांत वर अशा क्रमाने निरनिराळ्या टप्प्यांत साचतात. या साचणाऱ्या प्रथिनांची माहिती विशिष्ट प्रकाशयंत्रणेच्याद्वारे होते. त्यामुळे प्रथिनांची सजातीयता व रेणुभार ठरविता येतो. प्रथिन विद्रावाचा तर्षण दाब [⟶ तर्षण] मोजूनही रेणुभाराचा अंदाज सांगता येतो.
रेणूचा आकार, आकारमान व संरचना : विद्रावातील प्रथिन रेणूचा आकार निश्चित करणे महत्त्वाचे आहे. हे आकार गोलाकार (उदा., घोड्याच्या हृदयातील सायटोक्रोम सी) ते अतिशय लांबट गोलाभ (दीर्घवर्तुळ त्याच्या एका अक्षाभोवती फिरवून मिळणारा पृष्ठभाग उदा., फायब्रिनोजेन) असे विविध प्रकारचे असतात. विद्रावातील प्रथिन रेणूच्या आकाराचीनिश्चिती करण्यासाठी पुढील गुणधर्मांसारख्या गुणधर्मांवर आधरलेल्या पद्धती वापरतात : (१) प्रथिनाचा विद्रावातील विसरणाचा दर [किंवा त्वरा ⟶ विसरण], (२) प्रथिन विद्रावाची श्यानता (प्रथिन रेणू जसेजसे लांबट वा चपटे होत जातात तसतशी त्यांच्या विद्रावाची श्यानता वाढत जाते), (३) प्रथिन विद्रावाचे प्रवाहजन्य द्विप्रणमन (एका आपाती किरणापासूनदोन प्रणमन किरण-दुसऱ्या माध्यमात शिरल्यानंतर दिशेत बदल झालेले किरण-मिळण्याचा आविष्कार द्विप्रणमनाचे मूल्य प्रथिन रेणूंच्या प्रवाह दिशेच्या सापेक्ष असलेल्या दिक्स्थितीच्या परिमाणावर अवलंबून असून हे दिक्स्थितीचे परिमाण प्रवाहाचा वेग व रेणूची असममिती यांवर अवलंबून असते), (४) प्रत्यावर्ती (ज्याच्या दिशेत व मूल्यात सतत पुनरावर्ती बदल होतात अशा) विद्युत् प्रवाह क्षेत्रातील रेणूंची दिक्स्थिती (याकरिता विद्रावात प्रत्यावर्ती प्रवाह सोडून त्याचा विद्युत् अपार्यता स्थिरांक मोजतात).
मायोग्लोबीन, हीमोग्लोबिन यांसारख्या प्रथिनांची संरचना ठरविताना ‘क्ष-किरण विवर्तन’ (स्फटिकातून जाताना क्ष-किरणांचा होणारा विशिष्ट प्रकारचा दिशाबदल) पद्धत वापरतात. क्ष-किरणांचा झोत प्रथिनाच्या रेणूवर सोडून मिळालेल्या विवर्तन आकृतिबंधाचा अभ्यास करून प्रथिनाची संरचना व त्यातील ॲमिनो अम्लांची स्थाने निश्चित करतात. क्ष-किरण व इलेक्ट्रॉन सूक्ष्मदर्शक यांच्या साहाय्याने गोलाकार, तसेच तंतुमय प्रथिनांच्या रेणूंचे आकार व आकारमान यांसंबंधी माहिती मिळते. विशेषतः क्ष-किरण पद्धतीने स्फटिकातील व शुष्क स्थितीतील प्रथिन रेणूंच्या परिमाणांचे गणन करता येते.
प्रथिनांच्या संरचनांचीमाहिती करून घेण्यासाठी इतर पद्धतीही वापरल्या जातात पण ह्या पद्धतींमुळे मिळालेली माहिती क्ष-किरण विवर्तन पद्धतीएवढी सविस्तर नसते. तथापि या पद्धतीक्ष-किरण विवर्तन पद्धतीच्या मानाने कमी क्लिष्ट असतात. हिमोग्लोबिने, मेलॅनीन, रोडॉप्सीन, सेरूलोप्लाझ्मीन इत्यादींसारख्या वर्णप्रथिनांच्या संरचनेची माहिती मिळविण्यासाठी वर्णपट प्रकाशमापन [⟶ प्रकाशमापन] पद्धतउपयोगात आणतात. विशिष्ट तरंगलांबीच्या प्रकाशाचा झोत वर्णप्रथिनाच्या विद्रावातून जाऊ दिल्यास त्या प्रथिनाच्या संरचनेप्रमाणे प्रकाशाचे शोषण होते. याचे मापन करून प्रथिनाच्या संरचनेसंबंधी अनुमाने काढतात. प्रथिनाच्या प्रकाशीय सक्रियतेचा [ध्रुवित म्हणजे एकाच प्रतलात कंप पावणाऱ्या, प्रकाशाचे कंपन प्रतल फिरविण्याच्या क्षमतेचा ⟶ ध्रुवणमिति] अभ्यास करुनही प्रथिनाच्या आकारमानाची माहिती मिळू शकते.
प्रथिनांच्या रासायनिक विक्रियांचा अभ्यास करुनही त्यांच्या संरचनेबद्दल बरीच माहिती मिळते. एखादा घटक प्रथिन रेणूच्या पृष्ठभागावर आहे की रेणूतील असंख्य पेप्टाइड बंधांच्या आवरणाखाली झाकलेला आहे, हे त्या घटकाची क्रियाशीलता पाहून ठरविता येते. उदा., रिबोन्यूक्लिएज या एंझाइमाच्या एका रेणूत ६ टायरोसीन घटक असतात. या एंझाइमाची आयोडिनाशी विक्रिया केली असता त्यांपैकी तीन टायरोसीन घटक आयोडिनाशी संलग्न होतात व उरलेले तीन घटक तसेच राहतात. यावरून आयोडिनाशी संलग्न होणारे तीन टायरोसीन घटक रिबोन्युक्लिएजाच्या पृष्ठभागावर असतात, तर उरलेले तीन घटक रेणूच्या पेप्टाइड बंधाच्या आवरणाखाली दडलेले असतात, असे अनुमान निघते. या दडलेल्या टायरोसिनांपर्यंत आयोडिन पोहोचू शकत नाही.
जलसंयोग : दमट हवेतील पाण्याशी प्रथिनांचा सहज संयोग होतो. निरनिराळ्या प्रथिनांत हा गुणधर्म वेगवेगळ्या प्रमाणात असतो. साधारणतः प्रथिनाच्या वजनाच्या १० ते २०% पाण्याशी त्याचा संयोग होतो. प्रथिनांचा हा जलस्नेही गुणधर्मधन भारित लायसीन व आर्जिनीन आणि ऋण भारित ग्लुटामिक अम्ल व ॲस्पार्टिक अम्ल या ॲमिनो अम्लांमुळे असतो, असे आढळून आले आहे. सेरीन व थ्रिओनीन यांच्या हायड्रॉक्सिल (-OH) गटापाशी आणि ॲस्परजिन व ग्लुटामीन यांच्या अमाइड [- (CONH2)] गटापाशीही जलसंयोग होतो. प्रथिनांचे स्फटिक तयार होण्यासाठी संयोगित पाण्याची आवश्यकता असते. प्रथिनाचे संपूर्ण निर्जलीकरण केल्यास स्फटिकी स्वरूप नाहीसे होते. काही प्रथिनांच्या बाबतीत त्यांचे विकृतीकरण होऊन त्यांची जैव क्रियाशीलताही नष्ट झाल्याचे दिसून येते. प्रथिनांतील संयोगित पाण्यामुळे ती पाण्यात विरघळतात. अशा पाण्यात अमोनियम सल्फेटासारखी संयुगे मिसळल्यास प्रथिनांची विद्राव्यता कमी होते व ती अवक्षेपित होतात.
रंग-विक्रिया: प्रथिनाच्या विद्रावावर ठराविक विक्रियाकारकांची विक्रिया केली असता निरनिराळ्या रंगांचे विद्राव मिळतात. प्रथिनांतील पेप्टाइड बंधामुळे किंवा विशिष्ट ॲमिनो अम्लामुळे हे रंग मिळतात. प्रथिनांच्या रंग-विक्रिया म्हणून या विक्रिया ओळखण्यात येतात आणि प्रथिने व त्यांतील घटक ॲमिनो अम्ले यांचे गुणात्मक अभिज्ञान (उपस्थिती ओळखणे) व परिमाणात्मक गणन करण्याच्या दृष्टीने या विक्रिया महत्त्वाच्या आहेत. बाययुरेट (पेप्टाइड बंध), निनहायड्रीन (ॲमिनो अम्ल), झँथोप्रोटेइक (टायरोसीन, फिनिल ॲलॅनीन, ट्रिप्टोफेन), मिलॉन (टायरोसीन) इ. विक्रिया प्रसिद्ध आहेत. [⟶ ॲमिनो अम्ले].
विद्युत् रासायनिक गुणधर्म : प्रथिनातील ॲमिनो अम्लांचे आल्फा ॲमिनो गट व आल्फा कार्बॉक्सिल गट यांचे पेप्टाइड बंधांत रूपांतर झालेले असते. पेप्टाइड साखळीत नायट्रोजन-अंत्यस्थानापाशी एक आल्फा ॲमिनो गट व कार्बन-अंत्यस्थानापाशी एक आल्फा कार्बॉक्सिल गट एवढेच सुटे गट असतात पण प्रथिनाच्या विद्युत् रासायनिक गुणधर्मावर या दोन सुट्या गटांचा विशेष परिणाम होत नाही. लायसीन व आर्जिनीन यांचे धन भारित अमोनिया गट (-NH3+) आणि ॲस्पार्टिक व ग्लुटामिक अम्ले यांचे ऋण भारित कार्बॉक्सिल (-COO-) गट हे त्या दृष्टीने अत्यंत महत्त्वाचे गट आहेत. प्रथिनाच्या शंभर ॲमिनो अम्लांत धन भारित व ऋण भारित गटांचे प्रमाण १०-२० इतके असते.
प्रथिनांच्या विद्युत् रासायनिक गुणधर्मांचा उपयोग त्यांचे विद्युत् अनुमापन [⟶ अनुमापन] व विद्युत् संचारण करण्याच्या तंत्रांमध्ये करण्यात येतो. विद्युत् अनुमापनाने प्रथिनाच्या प्रत्येक रेणुतील कार्बॉक्सिल गट, अमोनियम गट, हिस्टिडिने व टायरोसिने यांची अंदाजी संख्या काढता येते.
प्रथिनांच्या धन व ऋण भारित पार्श्वशाखांमुळे त्यांचे गुणधर्म विद्युत् क्षेत्रात ॲमिनो अम्लांप्रमाणे असतात म्हणजेच विद्युत् संचारणात pH मूल्य नीच असताना प्रथिने ऋणाग्राकडे स्थलांतर करतात, तर pH मूल्य उच्च असताना ती धनाग्राकडे स्थलांतर करतात. अनेक प्रथिनांचा समविद्युत् भार बिंदू (म्हणजे ज्या pH मूल्याला प्रथिन रेणू स्थलांतर करीत नाही ते pH मूल्य) ५ ते ७ यांच्या दरम्यान असतो. मात्र लायसोझोम, सायटोक्रोम सी, हिस्टोन यांसारख्या प्रथिनांच्या बाबतीत आणि ज्यांत लायसीन व आर्जिनीन यांचे प्रमाण उच्च आहे अशा प्रथिनांच्या बाबतीत समविद्युत् भार बिंदू ८ ते १० यांच्या दरम्यान असतो. क्षारकीय ॲमिनो अम्लांचे प्रमाण अत्यल्प असलेल्या पेप्सिनाचा समविद्युत् भार बिंदू एकाच्या जवळपास असतो.
जैव महत्त्व : प्राण्यांना त्यांच्या वाढीसाठी अन्नातून प्रथिने (ॲमिनो अम्ले) मिळवावी लागतात. त्यांना वनस्पतींप्रमाणे नायट्रोजनयुक्त अकार्बनी संयुगांपासून प्रथिनांचे संश्लेषण करता येत नाही. माणसाच्या दैनंदिन आहारात ४५-५५ ग्रॅ. प्रथिने असणे आवश्यक आहे. तसेच ही प्रथिने परिपूर्ण (म्हणजे आवश्यक असलेली ॲमिनो अम्ले योग्य त्या प्रमाणात असलेली) असली पाहिजेत. दैनंदिन क्रियाशीलता व वाढ यांसाठी कोशिकेला या नायट्रोजनाची गरज असते. योग्य त्या प्रमाणात पुरवठा नझाल्यास प्रथिन-अपपोषणजन्य विकार [⟶ क्वाशिओरकोर त्रुटिजन्य रोग] होतात. या विकारांत योग्य ती प्रथिने दिल्यास नंतर थोडीफार सुधारणा झालेली दिसून येते पण प्रथिन-त्रुटी जर लहानपणापासूनच असेल आणि तिचे दुष्परिणाम शरीरावर होऊन गेले असतील, तर पुढील आयुष्यात आहारामध्ये भरपूर प्रथिने देऊनही ही प्रथिन-त्रुटीची लक्षणे पूर्णपणे नाहीशी करता येत नाहीत. दूध, अंडी, मासे, मांस यांमध्ये प्रथिने भरपूर असतात. वाढत्या लोकसंख्येबरोबर प्रथिनांची कमतरता दिवसेंदिवस वाढत आहे. त्यामुळे टाकाऊ पदार्थांतून गरीबांना परवडतील अशी खाण्यायोग्य प्रथिने मिळविण्याचे प्रयत्न अनेक देशांत चालू आहेत. शिंबावंत (शेंगा येणाऱ्या) वनस्पती, सोयाबीन, शेवाळ, तेलबिया, झाडाची पाने, कोंडा-भुस्सा, बुरशी, यीस्ट, खनिज तेलातील टाकाऊ पदार्थ इत्यादींचा उपयोग प्रथिने मिळविण्यासाठी वा त्यांचे संश्लेषण करण्यासाठी प्रयत्न करण्यात येत आहेत.
अन्नातील प्रथिनांचे पचन होऊन ॲमिनो अम्लांच्या स्वरूपांत ती आतड्यामध्ये शोषली जातात. शारीरिक गरजेप्रमाणे शरीरातील प्रथिनांचे संश्लेषण होते. प्रथिनांच्या संश्लेषणामध्ये कोशिकेतील डीऑक्सिरिबोन्यूक्लिइक अम्ल व रिबोन्यूक्लिइक अम्ल महत्त्वाचे कार्य करतात [⟶ न्यूक्लिइक अम्ले]. कोशिकांमध्ये न्यूक्लिइक अम्लांच्या मदतीने विशिष्ट प्रथिनांचे संश्लेषण होताना त्या प्रथिनातील एकंदर ॲमिनो अम्लांहून अधिक ॲमिनो अम्ले या संश्लेषित प्रथिन रेणूमध्ये असतात, असे अलीकडे आढळून आले आहे. या संश्लेषित प्रथिनांनी कुठल्या मार्गांनी जावयाचे यासंबंधीच्या सूचना जणू काही जादा ॲमिनो अम्लांच्या साखळीद्वारे रेखाटलेल्या असतात. एंझाइमे, हॉर्मोने ही प्रथिनेच असून त्यांचेही मार्गदर्शन असेच होत असावे. ॲमिनो अम्लांच्या रेणूतील कार्बनी सांगाडासुद्धा शरीरोपयोगी असतो [⟶ चयापचय]. त्यापासून कार्बोहायड्रेटे, अनावश्यक ॲमिनो अम्ले इ. संयुगे तयार होतात वा त्यांचे अपघटन होऊन शरीराला ऊर्जा मिळते.
औद्योगिक उपयोग : वनस्पतींतील ऊतकांपेक्षा प्राण्यांतील ऊतकांत प्रथिनांचे प्रमाण पुष्कळच जास्त असल्याने औद्योगिक महत्त्व असलेली बहुतेक प्रथिने प्राण्यांपासून मिळविण्यात येतात. अन्नातील प्रथिनांखेरीज सर्वांत अधिक प्रमाणात उपयोग करण्यात येत असलेली प्रथिने म्हणजे कापड उद्योगात मिळणारी लोकरीतील केराटीन व रेशमातील फायब्रोइन आणि चर्मोद्योगात प्रक्रियित कातड्यांपासून मिळणारे कोलॅजेन ही होत. ⇨ केसीन, जनावरांच्या रक्तातील प्रथिने व उकळलेल्या हाडांपासून मिळणारे कच्चे जिलेटीन यांपासून सरस व खळ तयार करतात. हाडातील ऑक्सीन हे प्रथिन कोलॅजेनासारखेच असते. कातड्यांचे तुकडे, संयोजी ऊतक व कंडरा यांपासून खाद्योपयोगी जिलेटीन मिळविण्यात येते [⟶ जिलेटीन]. खाटीकखान्यात मिळणाऱ्या रक्त, शिंगे, खूर, हाडे इ. प्रथिनयुक्त टाकाऊ पदार्थांचा कार्बनी (सेंद्रिय) नायट्रोजनयुक्त खत म्हणून उपयोग करतात.
मक्यापासून स्टार्च तयार करण्याच्या उद्योगात झाईन हे प्रथिन उपउत्पादन म्हणून मिळते. त्याचे औद्योगिक उपयोग केसिनासारखेच आहेत. ही दोन्ही प्रथिने सूत तयार करण्याच्या प्रक्रियेत वापरतात. सोयाबीन व भुईमूग यांसारख्या बियांपासून मिळणाऱ्या प्रथिनांचे प्लॅस्टिकांत रूपांतर करण्यात आले आहे. पपयांपासून मिळणारे ⇨ पेपेन हे एंझाइम मांस शिजविण्यापूर्वी ते मृदू करण्यासाठी वापरतात. सोयाबीन प्रथिन संश्लेषित खाद्यपदार्थ तयार करण्यासाठी वाढत्या प्रमाणावर वापरण्यात येत आहे. याकरिता प्रथिनाचे नाजूक तंतू कातून एकत्र करतात आणि मांस व इतर नैसर्गिक पदार्थासारखे दिसावेत म्हणून त्यांची योग्य रचना करतात व त्यांना कृत्रिम स्वाद देतात.
पहा : अन्न, ॲमिनो अम्ले आहार व आहारशास्त्र चयापचय त्रुटिजन्य रोग न्यूक्लिइक अम्ले पोषण.
संदर्भ : 1. Haurowitz, F. The Chemistry and Function of Proteins, New York, 1963.
2. Kleiner, I. S. Orten, J. M. Biochemistry, Tokyo, 1966.
3. Leach, S. J. Ed., Physical Principles and Techniques of Protein Chemistry, Part A, New York, 1969.
4. Neurath, H. Ed., The Proteins, 5 Vols., New York 1963-70.
5. Schroeder, W. A. The Primary Structure of Proteins, New York, 1968.
आयरन, जे. डब्ल्यू. (इं) मिठारी, भू. चिं. (म.) हेगिष्टे, म. द.
“