ग्लुकोज व फ्रुक्टोज : ही दोन्ही ⇨कार्बोहायड्रेट वर्गातील मोनोसॅकॅराइड गटातील संयुगे आहेत. दोघांचेही रेणुसूत्र C6H12O6 आहे, परंतु ग्लुकोजाच्या संघटनेत एक आल्डिहाइडी गट ![]() व फ्रुक्टोजाच्या संघटनेत एक कीटो गट
व फ्रुक्टोजाच्या संघटनेत एक कीटो गट ![]() आहे.
आहे.
ग्लुकोज : ग्लुकोजालाच ग्रेप शुगर, कॉर्न शुगर व डेक्स्ट्रोज अशीही नावे आहेत. निसर्गात ग्लुकोज द्राक्षे, मध व फळे यांमध्ये असते. रक्ताचाही तो एक घटक आहे. मधुमेह झालेल्या रोग्यांच्या रक्तात त्याचे प्रमाण जास्त असते. ग्लुकोज या नावावरून हे संयुग कार्बोहायड्रेट वर्गातील असून चवीस गोड आहे हे ध्वनित होते.
संरचना : उसाच्या साखरेचा रेणू एक ग्लुकोज एकक व एक फ्रुक्टोज एकक यांच्या संयोगाने बनलेला आहे. ग्लुकोजाची अनेक एकके संयोगित होऊन स्टार्च व सेल्युलोज यांचे रेणू बनतात.
⇨ग्लुकोसाइडनामक संयुगांच्या वर्गात ग्लुकोज हे अल्कोहॉले किंवा फिनॉले यांच्याशी संयोग झालेल्या रूपात असते. जलीय विच्छेदनाने (पाण्याच्या विक्रियेने रेणूचे तुकडे होण्याने) त्यांपासून ग्लुकोज व ती ती संयुगे निर्माण होतात.
ग्लुकोजाचे दक्षिण वलनी (+) आणि वाम वलनी (-) एकाच पातळीत कंप पावणाऱ्या म्हणजे ध्रुवित प्रकाशाची पातळी उजवीकडे वळविणारे व डावीकडे वळविणारे) असे दोन प्रकाशीय समघटक [रेणूतील अणूंचे प्रकार व संख्या तीच पण त्यांची मांडणी भिन्न असलेले प्रकार, → समघटकता] आहेत. कित्येकदा त्यांचा उल्लेख D व L ही अक्षरे प्रारंभी लावून केला जातो. तथापि ही अक्षरे कार्बोहायड्रेटांचे त्रिमितीय विन्यास (रेणूतील अणूंची अवकाशातील मांडणी) दाखविण्यासाठी वापरण्याचाही प्रघात असल्यामुळे प्रकाशीय वलन दर्शविण्यासाठी (+) व (-) या चिन्हांचा उपयोग करणे अलीकडे रूढ होत आहे [→ कार्बोहायड्रेटे].
नैसर्गिक ग्लुकोज दक्षिण वलनी आहे व यावरूनच त्याला डेक्स्ट्रोज हे नाव पडले आहे. याचा त्रिमितीय विन्यासही D आहे. या लेखात हेच रूप अभिप्रेत आहे.
विश्लेषण आणि रेणुभारमापन यांस अनुसरून ग्लुकोजाचे रेणुसूत्र C6H12O6 असे ठरते. ॲसिटिक ॲनहायड्राइडाच्या विक्रियेने ग्लुकोजापासून पेंटाॲसिटेट मिळते. ब्रोमीन जलाने ऑक्सिडीकरण [→ ऑक्सिडीभवन] केल्याने ग्लुकोजापासून एक ग्लुकॉनिक (पेंटाहायड्रॉक्सिल) अम्ल मिळते. या विक्रियांवरून ग्लुकोजाच्या रेणूत पाच हायड्रॉक्सिल गट (-OH) आहेत हे स्पष्ट होते. ग्लुकोजाचे फेलिंग विद्रावांचे (क्युप्रिक सल्फेट, सोडियम पोटॅशियम टार्टरेट आणि सोडियम हायड्रॉक्साइड एकत्र मिसळून तयार केलेल्या ताज्या विद्रावाचे) ⇨क्षपण होते. यावरून त्याच्या संघटनेत आल्डिहाइडी गट आहे हे दिसून येते. हायड्रोसायनिक अम्लाची समावेशन विक्रिया होऊन ग्लुकोजांचे ग्लुकोजसायनोहायड्रीन बनते. त्याचे जलीय विच्छेदन केले म्हणजे जे अम्ल मिळते त्याचे हायड्रोजन आयोडाइडाने क्षपण केले म्हणजे सर्व हायड्रॉक्सिल गटांच्या जागी हायड्रोजन अणू येतात व n-हेप्टिलिक अम्ल बनते. यावरून ग्लुकोजामध्ये सहा कार्बन अणूंची शृंखला असली पाहिजे असे अनुमान निघते. हा पुरावा लक्षात घेतला म्हणजे ग्लुकोजाची संरचना OH·C-CH·OH-CH·OH-CH·OH-CH·OH-CH2·OH अशी ठरते.
परंतु या विवृत शृंखला (जिची टोके एकमेकांस जोडलेली नाहीत अशा कार्बन अणूंची साखळी) सूत्राने ग्लुकोजाच्या सर्व रासायनिक गुणधर्मांचे स्पष्टीकरण होत नाही. उदा., ग्लुकोज हे आल्डिहाइडांच्या सर्व विक्रिया दाखवीत नाही. मिथिल अल्कोहॉलाच्या विक्रियेने त्यापासून दोन मिथिल ग्लुकोसाइडे मिळतात. त्याचप्रमाणे ग्लुकोजाच्या जलीय विद्रावाचे प्रकाशीय वलन प्रथम असते तेवढेच राहत नाही, कालांतराने ते बदलते आणि मग स्थिरावते (प्रकाशीय वलनांतर). या गुणधर्माचे स्पष्टीकरण ग्लुकोजाला वलयी (जिची टोके एकमेकांना जोडलेली आहेत अशी कार्बन अणूंची साखळी असलेली) संरचना दिल्याने होते. एका वलयी संरचनेत पाच कार्बन अणू व एक ऑक्सिजन अणू यांचे षट्पदी वलय आहे. त्याला ग्लुकोपायरॅनोज संरचना म्हणतात. दुसऱ्या वलयी संरचनेत चार कार्बनाचे अणू व एक ऑक्सिजन अणू असलेले पंचपदी वलय आहे. या संरचनेला ग्लुकोफ्यूरॅनोज म्हणतात. वलयी संरचना झाली म्हणजे पाच कार्बन अणू असममित (ज्याला वेगवेगळे चार अणू अथवा अणुसमुच्चय जोडलेले आहेत असे) होतात. विवृत शृंखलेत चारच अणू असममित असतात. त्यामुळे ग्लुकोजाची आल्फा आणि बीटा अशी दोन प्रकारची वलयी ग्लुकोसाइडे संभवतात व ती माहीत आहेत. ग्लुकोजाच्या विद्रावात विवृत शृंखलारूप व ह्या वलयी संरचना समतोलावस्थेत असतात असे दिसून आले आहे.
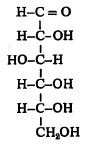
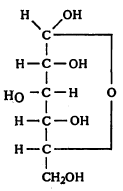
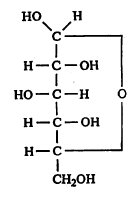
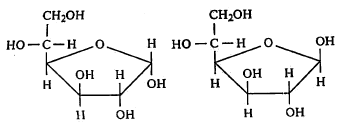
(२) व (३) ही रूपे अनुक्रमे पुढीलप्रमाणे दाखविण्याचा प्रघात आहे.



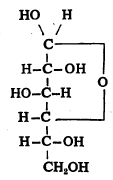
(४) व (५) या संरचना खालीलप्रमाणे दाखवितात.
गुणधर्म : ग्लुकोज हा एक वर्णहीन आणि C6H12O6·H2O या रूपात स्फटिकमय असलेला घन पदार्थ असून तो चवीस गोड आहे, परंतु त्याचा गोडपणा साखरेपेक्षा कमी आहे. ग्लुकोज पाण्यात विद्राव्य (विरघळणारे), अल्कोहॉलात अल्प विद्राव्य आणि ईथरात अविद्राव्य आहे. पाण्यातून स्फटिकीकरण केल्यास ५०° ते ११५° से. या तापमान मर्यादेत आल्फा D- ग्लुकोज मिळते. त्याचा वितळबिंदू १४६° से. असून त्याच्या जलीय विद्रावाचे प्रकाशीय वलन प्रथम [α] D + ११३° असते (येथे [α] D हे सोडियम D प्रकाशाच्या ध्रुवण पातळीचे वलन दर्शविते, हे वलन एक डेसिमीटर लांबीच्या व एक ग्रॅम प्रती घ.सेंमी. प्रकाशीय क्रियाशील पदार्थ असणाऱ्या विद्रावाच्या स्तंभातून जाणाऱ्या सोडियम D- प्रकाशासाठी मोजतात ) ते वलनांतराने + ५२·२° होते. ११५° ते १४६° से.या तापमानांच्या दरम्यान स्फटिकीकरणाने बीटा D- ग्लुकोज मिळते. त्याचा वितळबिंदू १४८°–१५०° से. असतो. त्याच्या जलीय विद्रावाचे प्रकाशीय वलन प्रथम [α] D + १९° असते ते वलनांतर होऊन + ५२·२° होते.
ग्लुकोजाच्या काही रासायनिक विक्रिया त्याच्या संरचना निश्चितीच्या संबंधात वर वर्णिल्या आहेत. त्याशिवाय नायट्रिक अम्लाने ग्लुकोजाचे ऑक्सिडीकरण होऊन D- सॅकॅरिक अम्ल [COOH – (CHOH)4 – COOH] बनते. पारदमेलाने (धातूच्या पाऱ्यातील विद्रावाने) क्षपण केले असता ग्लुकोजापासून सहा हायड्रॉक्सिल गट असलेले सॉर्बिटॉल [CH2OH – (CHOH)4 – CH2OH] हे संयुग तयार होते.
ग्लुकोजामधील प्राथमिक व द्वितीयक अल्काहॉली [→ अल्कोहॉल] गटांपासून अनुरूप अनुजात ( एका संयुगापासून बनविलेली दुसरी संयुगे) तयार होतात. उदा., एस्टरे व ईथरे.
विरल क्षारीय (अम्लांशी विक्रिया झाल्यास लवण देणाऱ्या पदार्थाचे गुणधर्म असणाऱ्या, अल्कलाइन) विद्रावांमुळे ग्लुकोजावर अनेक रासायनिक विक्रिया होतात व विघटन होऊन लॅक्टिक आणि तत्सम हायड्रॉक्सी अम्ले बनतात.
फिनिल हायड्रॅझिनाच्या विक्रियेने ग्लुकोज फिनिल हायड्रोझोन व ग्लुकोसाझोन ही संयुगे बनतात (फ्रुक्टोजासंबंधीची माहिती पहा). किण्वनाने (सूक्ष्मजंतूच्या क्रियेमुळे वा जटिल नायट्रोजनयुक्त संयुगांमुळे होणाऱ्या अपघटनाच्या म्हणजे संयुगांच्या रेणूचे तुकडे होण्याच्या प्रक्रियेने) ग्लुकोजापासून एथिल अल्कोहॉल मिळते. धातवीय हायड्रॉक्साइडांच्या विक्रियेने ग्लुकोसेटे बनतात.
अन्नातील कार्बोहायड्रेटांचे पचनक्रियेत ग्लुकोजामध्ये रूपांतर होते व ते ऊतकांमध्ये (समान रचना व कार्य असणाऱ्या पेशींच्या समूहांमध्ये) वापरले जाते.
उत्पादन : मका, बटाटा, टॅपिओका, रताळी इत्यादींच्या स्टार्चाचे जलीय विच्छेदन करून मोठ्या प्रमाणावर ग्लुकोज तयार करतात. जो स्टार्च स्वस्त पडेल तो वापरला जातो. अमेरिकेत मक्यापासून त्याचे उत्पादन करतात. स्टार्च पाण्यात मिसळून आणि त्यामध्ये हायड्रोक्लोरिक अम्ल विशिष्ट प्रमाणात घालून मिश्रण दाबाखाली (सु. ३५ किग्रॅ.) तापविले म्हणजे सु. अर्ध्या तासात ग्लुकोज तयार होते. नंतर उरलेल्या अम्लाचे सोड्याच्या साहाय्याने उदासिनीकरण (अम्लीय व क्षारीय गुणधर्म नसलेला पदार्थ बनविण्याची विक्रिया) करतात व तो विद्राव निर्वात पात्रात उकळून संहत (विद्रावातील विरघळलेल्या पदार्थांचे प्रमाण जास्त करणे) बनवितात. या क्रियेने जे स्फटिक मिळतात ते पाण्यात विरघळविले व अवश्य तर सक्रियित (अधिक क्रियाशील बनविलेल्या) कार्बनाच्या क्रियेने विद्राव वर्णहीन केला म्हणजे ग्लुकोजाचे स्फटिक मिळतात.
उपयोग : ग्लुकोजाचा उपयोग औषधोपचारात आणि पाव, केक इत्यादींसारख्या ज्यांमध्ये किण्वन क्रिया होते अशा उद्योगधंद्यांत होतो. त्याचप्रमाणे पेनिसिलीन, स्ट्रेप्टोमायसीन इ. प्रतिजैव (अँटिबायॉटिक) पदार्थ व यीस्ट बनविण्याच्या कृती, हवाबंद डब्यातील फळे, मुरंबे, सरबते यांमध्ये व आइसक्रिमामध्ये ग्लुकोज वापरतात.
लिक्विड (द्रव) ग्लुकोज नामक द्रव पूर्णपणे ग्लुकोज नसतो. त्यामध्ये काही भाग ग्लुकोज असून बाकीचा डेक्स्ट्रीन, माल्टोज इत्यादींचा असतो.
फ्रुक्टोज : याचे रेणुसूत्रही C6H12O6 हेच आहे. कार्बोहायड्रेट वर्गातील कीटो हेक्झोज वर्गात हे मोडते. यालाच D- फ्रुक्टोज, D- फ्रुक्टोपायरॅनोज किंवा लेव्ह्युलोज असेही म्हणतात. फळात, मधात आणि मधुरसात हे असते. वीर्यातील ही प्रमुख शर्करा आहे.
संरचना : फ्रुक्टोजाच्या रेणूत पाच हायड्रॉक्सिल गट पाच वेगवेगळ्या कार्बन अणूंना जोडलेले असून एक कीटो (CO) गट आहे, असे त्याच्या रासायनिक विक्रियांवरून सिद्ध झाले आहे. त्यावरून त्याचे संरचना सूत्र पुढीलप्रमाणे मांडले जाते.
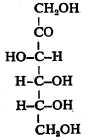
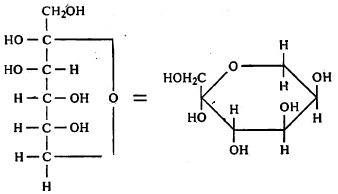
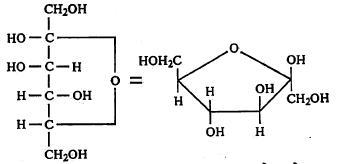
ग्लुकोजाप्रमाणे फ्रुक्टोजाचाही विवृत शृंखला संरचना त्याच्या सर्व गुणधर्माचे स्पष्टीकरण करू शकत नाही. त्याची दोन वलयी रूपे आहेत. ती मागील पृष्ठावर दाखविल्याप्रमाणे असतात.
ग्लुकोजाप्रमाणेच या वलयी संरचनांचे आल्फा आणि बीटा असे दोन प्रकार होतात.
गुणधर्म : फ्रुक्टोजाचे पिवळसर रंगाचे स्फटिक असून ते पाणी, अल्कोहॉल व ईथर यांमध्ये विरघळतात. वितळबिंदू १०३° –१०५° से. जलविद्रावाचे प्रकाशीय वलन [α]D प्रथम – १३२·२° असते ते वलनांतर होऊन –९२·२° होते. फ्रुक्टोज ग्लुकोजापेक्षा जास्त विद्राव्य व गोड आहे.
हायड्रॉक्सिल गट व कीटो गट यांच्या लाक्षणिक विक्रिया फ्रुक्टोज दाखविते.
फिनिल हायड्रॉझिनाच्या आधिक्यात ग्लुकोज व फ्रुक्टोज यांपासून एकच ओसाझोन वर्गाचे संयुग बनते. यातील विक्रिया परंपरेत प्रथम फिनिल हायड्राझोन बनते. त्यानंतर आल्डिहाइड वा कीटो गटाशेजारच्या एका हायड्रॉक्सिल गटाचे ऑक्सिडीभवन होऊन त्यांचे कार्बोनिल गटात रूपांतर होते. या कार्बोनिल गटांची नंतर फिनिल हायड्राझोनाशी विक्रिया होते व ओसाझोन बनते.
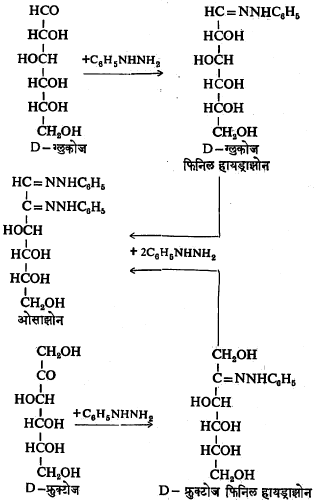
ओसाझोन वर्गाची संयुगे स्फटिकरूप आणि अत्यल्प विद्राव्य असतात. या संयुगांच्या शोधामुळे कार्बोहायड्रेटांच्या संशोधनास फार मदत झाली आहे.
उत्पादन व उपयोग : डेलिया, जेरूसलेम आर्टिचोक इ. कंपॉझिटी कुलातील वनस्पतींपासून मिळणाऱ्या इन्युलीन या पॉलिसॅकॅराइडाचे जलीय विच्छेदन करून फ्रुक्टोज बनवितात. उसाच्या साखरेच्या एका रेणूच्या जलीय विच्छेदनाने एक फ्रुक्टोजाचा व एक ग्लुकोजाचा रेणू निर्माण होतो.
मधुमेहाच्या रोग्यांना ही शर्करा काही प्रमाणात वापरता येते. खाद्यपदार्थ आणि औषधे यांत फ्रुक्टोज वापरतात.
ग्लिसरिनापासून संश्लेषण क्रियांनी ग्लुकोज व फ्रुक्टोज तयार करता येतात. परंतु या क्रिया सैद्धांतिक दृष्ट्याच महत्त्वाच्या आहेत.
पहा : कार्बोहायड्रेटे स्टार्च.
संदर्भ : 1. Fieser, L. Fieser, M. Organic Chemistry, New Delhi, 1962.
2. Finar, I. L. Organic Chemistry, Vol. I, London, 1962.
3. Riegel, E. R. Industrial Chemistry, New York, 1949.
4. West, E. S. Todd, W. R. Textbook of Biochemistry, New York, 1961.
सरदेशपांडे, भि. भु.
“