ग्लिसरीन : एक द्रवरूप कार्बनी संयुग. याच्या शुद्ध रूपाला ग्लिसरॉल म्हणतात. रेणुसूत्र (रेणूमध्ये असलेल्या मूलद्रव्यांचे प्रकार आणि संख्या दाखविणारे सूत्र) C3H8O3. संरचना सूत्र (रेणूतील अणूंची मांडणी दाखविणारे सूत्र) 1CH2OH – 2CHOH – 3CH2OH. याच्या रेणूत तीन हायड्रॉक्सिल गट (- OH) असल्यामुळे हे ट्रायॉल या अल्कोहॉलाच्या प्रकारात पडते. त्यावरून त्याचे रासायनिक नाव १, २, ३ – प्रोपेन ट्रायॉल असे होते. याचा रेणुभार ९२·०९ आहे.
शेले या शास्त्रज्ञांनी ऑलिव्ह तेलावर लिथार्जाची (लेड मोनॉक्साइडाची) रासायनिक क्रिया करून १७७९ मध्ये हे प्रथम बनविले व त्यास ऑल्सस हे नाव दिले. शव्हरल यांनी १८१३ मध्ये त्याला ग्लिसरीन ही संज्ञा दिली. याची रासायनिक संरचना व सूत्र १८३६ मध्ये पेलौझी, बर्थेलॉट व त्यांचे सहकारी यांनी निश्चित केली.
उपस्थिती : निसर्गात ग्लिसरीन मुक्त रूपात आढळत नाही. निरनिराळ्या कार्बनी अम्लांशी संयोग पावून बनलेल्या एस्टरांच्या रूपाने (यांना ग्लिसराइडे म्हणतात) ते वनस्पतिज तेले आणि प्राण्यांतील वसा (चरब्या, स्निग्ध पदार्थ) यांमध्ये तसेच प्राण्यांच्या शरीरातील ग्लिसरोफॉस्फेटांत (उदा., लेसिथिनात) असते.
उत्पादन : ग्लिसरिनाचे उत्पादन पुढील कच्च्या मालापासून करता येते. (१) तेले आणि वसा यांपासून साबण बनविण्याच्या प्रक्रियेत किंवा त्यापासून वसाम्ले (फॅरी ॲसिड्स) वेगळी करण्याच्या प्रक्रियेत उरणारी मिश्रणे, (२) प्रोपिलीन वायू आणि (३) शर्करा. यांपैकी पहिल्या दोहोंपासून याचे औद्योगिक प्रमाणावरील उत्पादन करण्यात येते.
(१) साबण बनविण्यासाठी वनस्पतिज तेले आणि वसा यांचे मिश्रण दाहक सोड्याच्या विद्रावाबरोबर तापवितात. त्यामुळे रासायनिक विक्रिया होते आणि तेले व वसा यांमधील वसाम्लांची सोडियम लवणे (म्हणजेच साबण) बनतात व ग्लिसरीन मोकळे होते. ते मिश्रणरूपाने राहते. साबण पाण्यात थोडा विरघळतो पण मिठाच्या विद्रावात तो जवळजवळ अविद्राव्य (न विरघणारा) आहे. म्हणून मिश्रणातून साबण वेगळा व्हावा यासाठी विक्रिया मिश्रणात मीठ घालतात व वेगळा झालेला साबण काढून घेतात. खाली राहिलेल्या मिश्रणात (याला सोप स्पेंट लाय किंवा स्पेंट लाय म्हणतात) ग्लिसरीन सु. १० ते १५ टक्के असून ते मीठ, क्षारके (अम्लाशी विक्रिया झाल्यास लवणे देणारे पदार्थ) व प्रथिने यांत मिसळलेले असते. या मिश्रणातून ग्लिसरीन काढून घेण्याच्या वेगवेगळ्या प्रक्रिया आहेत. एका प्रक्रियेत स्पेंट लायमध्ये थोडे वसाम्ल मिसळून मिश्रण तापवितात. त्यामुळे अतिरिक्त असलेल्या क्षारकाचा साबण बनतो. मिश्रण थंड करून तो काढून टाकतात. राहिलेल्या विद्रावात विरल हायड्रोक्लोरिक अम्ल आणि तुरटीसारखा एखादा किलाटक (तरंगणारा पदार्थ आळवून द्रवाच्या तळाशी बसविणारा पदार्थ) योग्य प्रमाणात मिसळून मिश्रण चांगले ढवळतात आणि अविद्राव्य पदार्थ गाळून काढून टाकतात. राहिलेला विद्राव नंतर दाहक (कॉस्टिक) सोडा मिसळून किंचित क्षारधर्मी (अल्कलाइन) करतात आणि पंपाच्या साहाय्याने निर्वात पात्रात भरून कमी दाबाच्या वाफेने तापवून मिश्रण संहत करतात (मिश्रणातील विरघळलेल्या पदार्थाचे प्रमाण जास्त करतात). यावेळी बरेचसे मीठ अलग होते ते काढून टाकतात. सु. ८० टक्क्यापर्तं ग्लिसरीन असलेला विद्राव याप्रकारे मिळतो. तो सक्रियित (अधिक क्रियाशील बनविलेल्या) कोळशाच्या थरातून गाळून घेतला म्हणजे जे ग्लिसरीन मिळते त्याला गवताच्या रंगाचे ग्लिसरीन म्हणतात. हे अशुद्ध असून निर्वात बाष्पनाने शुद्ध करता येते.
तेले आणि वसा यांतील वसाम्ले वेगळी करण्यासाठी पाण्याने त्यांचे जलीय विच्छेदन (पाण्याच्या विक्रियेने संयुगाचे तुकडे करणे) करतात. ही रासायनिक क्रिया उत्प्रेरक (विक्रिया जलद किंवा कमी तापमानास घडावी यासाठी वापरण्यात येणारा पदार्थ) वापरून नेहमीच्या वातावरण दाबास किंवा उच्च दाब व उच्च तापमान यांचा उपयोग करून, उत्प्रेरकाने किंवा उत्प्रेरकाशिवाय घडवून आणता येते. विक्रियेनंतर वसाम्ले वेगळी काढली म्हणजे जो विद्राव उरतो त्याला ‘स्वीट-वॉटर’ म्हणतात. त्यात ग्लिसरीन असते. स्वीट-वॉटरमध्ये चुना मिसळून मिश्रण चांगले ढवळतात व गाळतात. जो विद्राव मिळतो तो निर्वात बाष्पित्राने (बॉयलरने) संहत केला म्हणजे ग्लिसरीन मिळते. ते नंतर शुद्ध करतात.
(२) इ.स. १९४९ पर्यंत ग्लिसरीन वरील प्रक्रियांनीच मुख्यतः मिळविले जात असे. त्यानंतर संश्लेषणानेही (रासायनिक विक्रियांनी साध्या संयुगापासून पदार्थ बनविण्यानेही) ते बनविण्यात येऊ लागले आणि १९६५ च्या सुमारास एकंदर उत्पादनाच्या सु. ६० टक्के इतके उत्पादन या पद्धतीने होऊ लागले.
या पद्धतीत खनिज तेलाच्या शुद्धीकरणात मिळणारा प्रोपिलीन वायू कच्चा माल म्हणून वापरला जातो. पुढील तीन मार्गांनी प्रोपिलिनापासून ग्लिसरीन बनविता येते.
( अ ) कोरड्या प्रोपिलिनावर क्लोरिनाची विक्रिया करून प्रथम ॲलिल क्लोराइड बनवितात. त्यावर हायपोक्लोरस अम्लाची विक्रिया केली म्हणजे डायक्लोरोहायड्रिनांचे मिश्रण मिळते. कॅल्शियम हायड्रॉक्साइडाने त्यापासून एपिक्लोरोहायड्रीन बनवून त्याचे जलीय विच्छेदन केले म्हणजे ग्लिसरीन बनते.
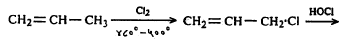
प्रोपिलीन ॲलिल क्लोराइड
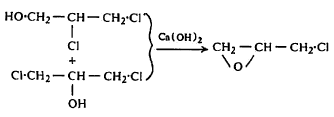
डायक्लोरोहायड्रिनांचे मिश्रण एपिक्लोरोहायड्रीन

ग्लिसरीन
(आ) या पर्यायात प्रोपिलिनाचे उत्प्रेरकाच्या सान्निध्यात प्रथम ॲक्रोलीइनात रूपांतर करण्यात येते. ऑस्मियम टेट्राऑक्साइडाच्या (OsO4) उपस्थितीत हायड्रोजन पेरॉक्साइडाने त्यापासून ग्लिसराल्डिहाइड बनवितात व त्याच्या हायड्रोजनीकरणाने (संयुगात हायड्रोजनाचा समावेश करण्याच्या क्रियेने) ग्लिसरीन मिळवितात.
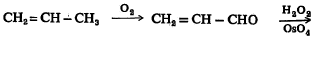
प्रोपिलीन ॲक्रोलीइन
![]()
ग्लिसराल्डिहाइड ग्लिसरीन
(इ) या प्रक्रियेत दमट क्लोरिनाचा उपयोग करून प्रोपिलिनाचे प्रथम ऑक्साइड बनवितात. ट्रायलिथियम फॉस्फेट या उत्प्रेरकाने त्याचे समघटकीकरण (रेणूतील अणूंची मांडणी बदलण्याची क्रिया) केले म्हणजे ॲलिल अल्कोहॉल बनते. त्याचे ग्लायसिडॉल बनवून नंतर जलीय विच्छेदन केले म्हणजे ग्लिसरीन तयार होते.
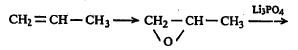
प्रोपिलीन प्रोपिलीन ऑक्साइड
![]()
ॲलिल अल्कोहल ग्लायसिडॉल

ग्लिसरीन
(३) शर्करांपासून किण्वनाने (सूक्ष्मजंतूंच्या क्रियेमुळे वा जटिल नायट्रोजनयुक्त संयुगांमुळे होणाऱ्या अपघटनाच्या म्हणजे संयुगाच्या रेणूचे तुकडे होण्याच्या क्रियेने) जेव्हा अल्कोहॉल बनते. त्याचवेळी अल्प प्रमाणात ग्लिसरीनही निर्माण होते. पण सोडियम सल्फाइटाचा समावेश करून किण्वन केले, तर ग्लिसरिनाचे प्रमाण वाढते असे न्यूबर्ग यांनी १९१६ मध्ये प्रथम दाखविले. त्यानंतर यासंबंधी बरेच संशोधन झाले असून काही प्रक्रियांनी ग्लिसरिनाचे प्रमाण साखरेच्या ३० टक्क्यांपर्यंत वाढविता येते असे दिसून आले आहे. पहिल्या महायुद्धाच्या वेळी जर्मनीने या पद्धतीचा उपयोग करून टनावारी ग्लिसरीन युद्धखात्यासाठी बनविले. दुसऱ्या महायुद्धाच्या वेळीही किण्वन पद्धत वापरण्यात आली. तथापि अडीअडचणीच्या काळीच ही पद्धत वापरतात.
भारतात पहिल्या पद्धतीनेच ग्लिसरीन बनविले जाते. ते तीन प्रतींचे असते. (१) व्यापारी प्रतीचे, (२) अभिस्फोटक (डायनामाइट) प्रतीचे व (३) रासायनिक दृष्ट्या शुद्ध (C. P.) प्रतीचे.
अशुद्ध ग्लिसरिनाचे एकदा ऊर्ध्वपातन (वाफ करून व मग ती थंड करून घटक अलग करण्याची क्रिया) करून मिळणाऱ्या ग्लिसरिनात लवणे, वसा, अम्ले वगैरे पदार्थ अशुद्ध नमुन्यापेक्षा कमी प्रमाणात असतात. हेच व्यापारी प्रतीचे ग्लिसरीन होय.
अशुद्ध ग्लिसरीन दोनदा ऊर्ध्वपातित केले म्हणजे ते जास्त शुद्ध रूपात मिळते. नायट्रोग्लिसरीन तयार करण्यासाठी हे वापरीत असल्यामुळे हे विशिष्ट कसोट्यांस उतरेल असे असावे लागते. नायट्रीकरण केल्यावर हे अम्लमिश्रणापासून त्वरित वेगळे झाले पाहिजे, त्यामध्ये तरंगणारी अशुद्ध द्रव्ये नसली पाहिजेत आणि त्याची सापेक्ष घनता १५·५° से.ला १·२६२ पेक्षा कमी असली पाहिजे, या त्यांपैकी काही कसोट्या होत. त्यामध्ये कोणत्या अशुद्धी व त्या किती प्रमाणात असल्या, तरी चालतील याविषयी विनिर्देश (इष्ट गुणधर्मांचे तपशील) उपलब्ध आहेत.
रासायनिक दृष्ट्या शुद्ध प्रतीचे ग्लिसरीन ब्रिटिश फार्माकोपियानुसार किंवा युनायटेड स्टेट्स फार्माकोपियानुसार मान्य होईल अशा गुणवत्तेचे असते. त्याकरिता ते पुढील कसोट्यांस उतरावे लागते. (१) त्यामध्ये ग्लिसरिनाचे प्रमाण किमान ९८ टक्के असावे, (२) सापेक्ष घनता २०° से.ला १·२५५ ते १·२६०, (३) प्रणमनांक (निर्वातातील प्रकाशवेग व माध्यमातील, येथे ग्लिसरिनातील, प्रकाशवेग यांचे गुणोत्तर) २०° से.ला १·४६९६ ते १·४७२६, (४) शिसे १ दशलक्षांशापेक्षा व आर्सेनिक २ दशलक्षांशापेक्षा कमी व राख १ शतांशापेक्षा कमी असावी, (५) ते पाण्यात व ९५ टक्के अल्कोहॉलात पूर्ण विद्राव्य व ईथर, क्लोरोफॉर्म व तेले यांत अविद्राव्य असले पाहिजे व (६) ते पाण्यात १० टक्क्यांपर्यत मिसळले, तर लिटमसवर क्रिया होऊ नये.
भौतिक गुणधर्म : शुद्ध ग्लिसरीन वर्णहीन, साखरेच्या पाकासारखे दाट, चवीला गोड आणि आर्द्रताशोषक असते. पाण्यात व अल्कोहॉलात ते विरघळते. त्याचे स्फटिक २०° से. तापमानाला वितळतात. २९०° से.पेक्षा जास्त तापविले, तर त्याचे विघटन (संयुगाचे तुकडे पडणे) होते पण दाब कमी करून (निर्वातनाने), विघटन होऊ न देता, त्याचे ऊर्ध्वपातन करता येते.
रासायनिक गुणधर्म : सोडियम धातूच्या विक्रियेने ग्लिसरिनातील तीन हायड्रॉक्सिल गटांपैकी प्रथम कडेच्या एका हायड्रॉक्सिल गटातील हायड्रोजन अणू सुलभतेने प्रतिष्ठापित (एका अणूच्या वा अणुगटाच्या ठिकाणी दुसरा अणू वा अणुगट येणे) होतो, त्यानंतर कडेच्या दुसऱ्या हायड्रॉक्सिल गटातील होतो पण मधला हायड्रॉक्सिल गट प्रतिष्ठापित होत नाही.
ग्लिसरिनाचे ऑक्सिडीकरण [→ ऑक्सिडीभवन] अनेक प्रकारे होते. ऑक्सिडीकरणाने बनणारी संयुगे ऑक्सिडीकारक कोणता आहे यावर अवलंबून असतात. उदा., संहत नायट्रिक अम्लाने ग्लिसरिक
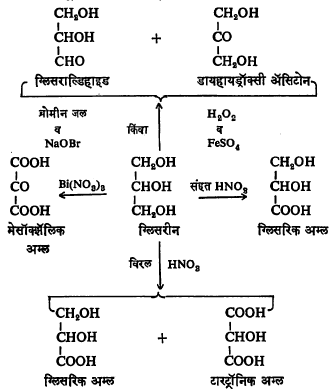
अम्ल बनते, पण विरल नायट्रिक अम्ल वापरले, तर ग्लिसरिक व टारट्रॉनिक ही अम्ले मिळतात. बिस्मथ नायट्रेटाने मुख्यतः मेसॉक्झॅलिक अम्ल बनते तर ब्रोमीन जल व सोडियम हायपोब्रोमाइट यांनी किंवा हायड्रोजन पेरॉक्साइड व फेरस सल्फेट यांच्या मिश्रणाने ऑक्सिडीकरण झाल्यास ग्लिसराल्डिहाइड व डायहायड्रॉक्सी ॲसिटोन यांचे मिश्रण मिळते. त्याला ग्लिसराेज म्हणतात.
पोटॅशियम हायड्रोजन सल्फेटाने ग्लिसरिनाचे निर्जलीकरण होऊन ॲक्रिलाल्डिहाइड (ॲक्रोलीइन) बनते.
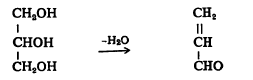
ॲक्रिलाल्डिहाइड
किंवा ॲक्रोलीइन
हायड्रोजन क्लोराइडच्या विक्रियेने ग्लिसरिनापासून आल्फा क्लोरोहायड्रीन, बीटा क्लोरोहायड्रीन, आल्फा बीटा डायक्लोरोहायड्रीन व आल्फा आल्फा ’ डायक्लोरोहायड्रीन ही संयुगे बनतात पण फॉस्फरस पेंटाक्लोराइडाने ग्लिसरॉल ट्रायक्लोरोहायड्रीन बनते.
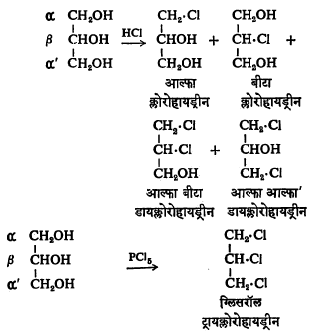
हायड्रोजन ब्रोमाइड आणि फॉस्फरस ट्रायब्रोमाइड यांच्या विक्रिया अनुक्रमे हायड्रोजन क्लोराइड व फॉस्फरस पेंटाक्लोराइड यांच्या विक्रियांसारख्याच होतात परंतु हायड्रोजन आयोडाइट (हायड्रिआयोडिक अम्ल) व फॉस्फरस ट्रायआयोडाइट यांच्या विक्रिया, विक्रियाकारक किती वापरले आहेत यावर अवलंबून असतात. ते कमी प्रमाणात असतील, तर ॲलिल आयोडाइड मुख्यतः बनते. पण प्रमाण जास्त असेल, तर ॲलिल आयोडाइडापासून अखेरीस आयसोप्रोपिल आयोडाइड (CH3 – CHI – CH3) तयार होते.
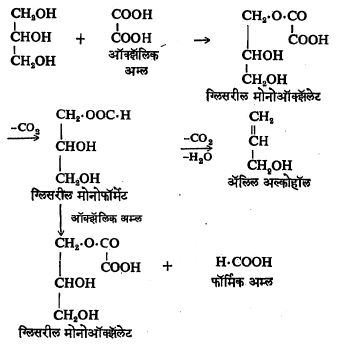
ऑक्झॅलिक अम्लाच्या विक्रियेने ग्लिसरिनापासून ॲलिल अल्कोहॉल हे संयुग मिळते.
ग्लिसरीन मोनोफॉर्मेट बनेपर्यंत विक्रिया होऊ देऊन त्यात स्फटिकी ऑक्झॅलिक अम्ल घातले व मिश्रण तापविले, तर फॉर्मिक अम्ल आणि ग्लिसरील मोनोऑक्झॅलेट निर्माण होतात.
प्रयोगशाळेत फॉर्मिक अम्ल बनविण्यासाठी ही प्रक्रिया फार सोयीची ठरते.
ॲलिल अल्कोहॉल बनविण्यासाठी ही विक्रिया वापरताना ऑक्झॅलिक अम्लाऐवजी फॉर्मिक अम्ल वापरल्यास ॲलिल अल्कोहॉलाचा उतारा जास्त येतो.
वरील सर्व विक्रिया पुढील सूत्रात दाखविल्याप्रमाणे घडतात.
नायट्रिक व सल्फ्यूरिक अम्लांचे मिश्रण थंड करून त्यात तापमान २-३° से. तापमानाच्या वर जाणार नाही अशा बेताने ग्लिसरिनाची धार सतत सोडून नायट्रोग्लिसरीन हे संयुग बनवितात. ते तेलकट व पिवळसर रंगाचे असून विक्रिया- मिश्रणाच्या पृष्ठावर तरंगते. तापमान ०° से. करून ते वेगळे काढून घेतात व कोरडे करून साठवितात.
हे ग्लिसरिनापासून बनलेले एस्टर आहे म्हणून त्याचे नाव ग्लिसरीन ट्रायनायट्रेट असे वास्तविक हवे. हे नायट्रोसंयुग नसल्यामुळे नायट्रोग्लिसरीन ही संज्ञा यथार्थ नाही, परंतु नायट्रोसंयुगे बनविताना जे अम्ल मिश्रण वापरतात तेच येथेही वापरीत असल्यामुळे ही संज्ञा त्याला दिली गेली व ती रूढ झाली आहे.

एक कार्बॉक्सिल गट ( —COOH ) असलेल्या अम्लांच्या विक्रियेने ग्लिसरिनापासून एक-एस्टर, द्वि-एस्टर किंवा त्रि-एस्टर जातीची संयुगे मिळू शकतात [→ एस्टरे]. उच्च तापमान आणि विक्रिया मिश्रणात अम्लाचे प्रमाण अधिक ठेवल्यास त्रि-एस्टरे बनतात.
अल्कोहॉले किंवा फिनॉले यांच्याशी संयोग होऊन ग्लिसरिनाची ईथरे बनतात. ग्लिसरिनाचे दोन अथवा अधिक रेणूही एकमेकांशी अशा तऱ्हेने संयोग पावतात. त्यायोगाने मिळणाऱ्या संयुगांना ‘पॉलिग्लिसरॉल’ असे वर्गनाव आहे. उदा., डायग्लिसरॉल
CH2OH·CHOH·CH2·O·CH2·CHOH·CH2OH.
वेगवेगळ्या किण्वन क्रियांनी ग्लिसरिनापासून प्रोपिऑनिक, ब्युटिरिक, लॅक्टिक आणि सक्सिनिक ही अम्ले आणि n-ब्युटेनॉल व ट्राययमिथिलीन ग्लायकॉल ही संयुगे निर्माण होतात.
अभिज्ञान : (अस्तित्व ओळखणे). पोटॅशियम हायड्रोजन सल्फेटाबरोबर तापविल्यास ग्लिसरिनापासून ॲक्रोलीइन तयार होते. याचा वास विशिष्ट, उग्र व झोंबणारा आहे. त्यावरून ग्लिसरिनाचे अस्तित्व जाणता येते.
ग्लिसरिनापासून ट्रायबेंझोएट, ट्रिस ( ३,५- डायनायट्रो बेंझोएट) व ट्रिस (पॅरानायट्रो बेंझोएट) हे घनरूप अनुजात (एका संयुगापासून बनलेली दुसरी संयुगे) बनविता येतात आणि त्यांच्या वितळबिंदुंवरून ग्लिसरिनाची उपस्थिती सिद्ध करता येते.
परिमाणात्मक विश्लेषणासाठी ग्लिसरीन असलेल्या नमुन्याचे परआयोडिक अम्लाने ऑक्सिडीकरण करून त्याचे प्रमाण निश्चित करतात. ग्लिसरिनाचे ट्रायॲसिटीन (ग्लिसरील ट्रायॲसिटेट) करून किंवा पोटॅशियम डायक्रोमेटाने ऑक्सिडीकरण करून त्यावरून प्रमाण निश्चित करण्याच्या पद्धतीपेक्षा, परआयोडिक अम्ल पद्धत जास्त समाधानकारक आहे.
उपयोग : ग्लिसरिनात आर्द्रताशोषणाचा गुण असल्यामुळे ते धूम्रपानाच्या व खाण्याच्या तंबाखूत मिसळतात. त्यामुळे तीमध्ये इष्ट प्रमाणात आर्द्रता टिकते.
खाद्यपदार्थात वापरण्याचे रंग व स्वाद आणि कित्येक औषधे यांकरिता ग्लिसरीन विद्रावक म्हणून उपयोगी पडते. काही प्रकारच्या यंत्रसामग्रीत (उदा., खाद्यपदार्थाच्या निर्मितीसाठी वापरण्याची) ग्लिसरीन वंगण म्हणून वापरतात. सौंदर्यप्रसाधने, दंतधावन इ.मध्येही ते घालतात. ग्लिसरिनाची अनेक संयुगेही उपयुक्त आहेत.
ग्लिसरीन व थॅलिक ॲनहायड्राइड आणि इतर द्विक्षारीय अम्ले यांच्या संयोगाने ‘अल्किड रेझिने’ नामक वर्गाची संयुगे बनतात. त्यांचा उपयोग वस्तूंच्या पृष्ठभागास संरक्षक असा थर देण्याच्या मिश्रणात मोठ्या प्रमाणावर होतो.
नायट्रोग्लिसरीन हे आघाताने तत्काल स्फोट होणारे संयुग आहे. परंतु कीझेलगूर या मृत्तिकेत शोषण करून स्फोटक (डायनामाइट) म्हणून त्याचा उपयोग करता येतो. ब्लास्टिंग जिलेटीन, कॉर्डाइट इ. स्फोटकांमध्ये नायट्रोग्लिसरिनाचा अंतर्भाव केलेला असतो.
फॉस्फोरिक अम्लाशी संयोग होऊन झालेल्या ग्लिसरोफॉस्फेटाचा उपयोग औषधात केला जातो. पॉलिग्लिसरॉल संयुगे पृष्ठप्रभावकारके (द्रव पदार्थांचा पृष्ठभाग ताणलेल्या पापुद्र्यासारखा असतो व त्यामुळे त्यावर ताण असतो हा ताण कमी करण्याचा गुण असलेली संयुगे), पायसकारके (न मिसळणाऱ्या द्रव पदार्थाचे मिश्रण घडवून आणणारी-संयुगे), आसंजके (पदार्थ एकमेकांस चिकटविणारी संयुगे) व वंगणे म्हणून उपयोगी पडतात.
भारतीय उत्पादन : भारतात सोप स्पेंट लाय यापासूनच ग्लिसरिनाचे उत्पादन केले जाते. पहिल्या महायुद्धाच्या काळापासून उत्पादनास सुरुवात झाली. प्रारंभी अशुद्ध ग्लिसरीन शुद्धीकरणासाठी निर्यात होत असे, पण आता ग्लिसरीन शुद्ध करणारे कारखाने भारतात आहेत. १९५१ मध्ये भारताची शुद्ध ग्लिसरिनाची उत्पादनक्षमता ३,२१९ टन होती व प्रत्यक्ष उत्पादन २,४६८ टन होते व १९६९ मध्ये उत्पादनक्षमता १४,९२८ टन व प्रत्यक्ष उत्पादन ८,७८० टन होते.
पहा : नायट्रोग्लिसरीन.
संदर्भ : 1. CSIR, The Wealth of India, Industrial Products, New Delhi, 1957.
2. Faith, W. L. Keyes, D. B. Clark, R. L. Industrial Chemicals, London, 1957.
3. Riegel, E. R. Industrial Chemistry, New York, 1959.
दीक्षित, व. चिं.
“