तर्षण : मनुका पाण्यात बुडवून ठेवल्या असता त्यांच्या अंतर्भागात पाणी प्रवेश करते आणि काही वेळाने त्या तट्ट फुगलेल्या दिसतात. याउलट सोडा–साबणाने कपडे धुतले असता आपल्या बोटांची अग्रे सुरकुतलेली दिसतात, कारण त्यांच्या आतील पाण्याचा अंश बाहेर खेचून घेतला जातो. नेहमीच्या व्यवहारात दिसून येणारे हे दोन परिणाम तर्षणामुळे होतात. जलचर प्राण्याच्या शरीरात पाणी फार शोषले जाऊ नये किंवा आतील पाणीही बाहेर येऊ नये म्हणून एक तर्षण–नियामक कार्य करीत असतो.
त्याच प्रमाणे रक्तातील तांबड्या कोशिका (पेशी) शुद्ध पाण्यात सोडल्या असता इतके पाणी शोषून घेत जातात की, शेवटी त्या अती फुगून फुटतात परंतु त्याच कोशिका मिठाच्या विद्रावात बुचकळून ठेवल्या असता त्यांतील पाण्याचा अंश बाहेर खेचला जातो आणि त्यामुळे त्या सुरकुततात. डॉक्टर जेव्हा रोग्याच्या शरीरात एखादे औषध टोचतात तेव्हा औषधामुळे असा प्रकार होता कामा नये, हे उघडच आहे. पचनेंद्रिये, उत्सर्जनेंद्रिये यांच्या कार्यात, तसेच वनस्पतींच्या पोषणामध्ये तर्षण प्रेरणा महत्त्वाचे कार्य करीत असतात.
अर्धपार्य पटल : काही विशेष प्रकारच्या पडद्यांच्या बाबतीत असे दिसून येते की, त्यांच्या एका बाजूला एखादा विद्राव (विरघळलेला पदार्थ असलेला द्रव) किंवा कलिल (सूक्ष्म कण तरंगत असलेला द्रव) ठेवले, तर त्या पडद्यातून शुद्ध विद्रावक (पदार्थ विरघळविणारा द्रव) पलीकडे जाऊ शकतो, परंतु विद्रुत (विरघळलेला पदार्थ) किंवा कलिलवृत्ती पदार्थ मात्र त्यांतून पलीकडे जाऊ शकत नाहीत. ज्या पातळ पडद्यातून फक्त शुद्ध द्रव पलीकडे जाऊ शकतो पण विरघळलेले पदार्थ किंवा कलिल (अजिबात) पलीकडे जाऊ दिले जात नाहीत, त्या पडद्याला (आदर्श) अर्धपार्य पटल असे म्हणतात. प्रारंभीच्या उदाहरणात मनुकांच्या वरची साल व रक्तातील तांबड्या कोशिकांवरील आवरण ही अर्धपार्य पटले आहेत.
येथे एक गोष्ट लक्षात ठेवली पाहिजे की, आपणास नेहमी मिळणाऱ्या अर्धपार्य पटलांतून थोड्या प्रमाणात विद्रुताचे रेणूही पलीकडे जाऊ शकतात म्हणजे ती अंशतः अर्धपार्य आहेत. आदर्श अर्धपार्य पटलांतून विद्रुताचे रेणू अजिबात पलीकडे जाऊ शकणार नाहीत. तसेच जीवसृष्टीत व वनस्पतिसृष्टीत अशी काही अर्धपार्य पटले आढळतात की, त्यांमधून काही प्रकारच्या विद्रुताचे रेणू पलीकडे जाऊ शकतात, तर काही प्रकारचे (विशेषतः रेणुभार जास्त असणाऱ्या) विद्रुताचे रेणू पलीकडे जाऊ शकत नाहीत.
एखाद्या अर्धपार्य पटलाच्या दोन बाजूंना दोन वेगवेगळ्या संहतींचे (एकक घनफळात असणाऱ्या विद्रुतांच्या वस्तुमानाचे) विद्राव ठेवल्यास त्या पटलातून फक्त शुद्ध विद्रायक कमी संहतीच्या विद्रावाकडून जास्त संहतीच्या विद्रावाकडे विसरित (एकमेकांत आपोआप मिसळणे) होतो, या विसरणास तर्षण असे म्हणतात.
वायूंच्या बाबतीतही तर्षण अनुभवास येते. उदा., पॅलॅडियम धातूच्या तप्त पत्र्यातून तर्षणामुळे हायड्रोजन वायू पलीकडे जाऊ शकतो.
आदर्श अर्धपार्य पटलाच्या एका बाजूला शुद्ध द्रव आणि दुसऱ्या बाजूला विद्राव ठेवला असता विद्रावावर जो जादा दाब देऊन तर्षण थांबविता येते, त्या जादा दाबाला वरील समूहाचा तर्षण दाब असे म्हणतात.
संहती, तापमान व तर्षण दाब : समजा विद्राव केल्यामुळे विद्रुताच्या रेणूंचे संगमन (एकमेकांजवळ येणे) किंवा विदलन (विद्युत् भारित घटकांत म्हणजे आयनांत विघटन होणे) होत नाही व विद्रावाची संहती नीच आहे, अशा विद्रावाचे तापमान जर स्थिर असेल, तर त्याचा तर्षण दाब (π) हा विद्रावाच्या संहतीच्या सम प्रमाणात असतो.
π = KC … … … (१)
येथे π तर्षण दाब मानक (प्रमाण) वातावरण दाबाच्या एककात मांडलेला आहे. C ही विद्रावाची संहती आहे (ग्रॅमरेणू /लिटर) आणि K हा स्थिरांक आहे. विद्रावाचे घनफळ V असून त्यात ν ग्रॅमरेणू विद्रुत विरघळलेले असले, तर
∴ π V = Kν … … … (२)
विद्रावाची संहती स्थिर ठेवून तापमान बदलले, तर त्याचा तर्षण दाब निरपेक्ष तापमानाशी (T) सम प्रमाणात बदलतो, असे दिसून येते.
π = K´ T … …. …. (३)
येथे K´ हा एक स्थिरांक आहे. समी. (२) हे वायूंना लागू पडणाऱ्या बॉइल ह्यांच्या नियमाशी सदृश असून समी. (३) हे चार्ल्स यांच्या नियमासारखे आहे. ही दोन समीकरणे एकत्र केल्यास,
π V = ν R’ T … …. …. (४)
हे समीकरण मिळते. हे समीकरण PV = NRT या वायूंच्या सार्वत्रिक समीकरणासारखेच आहे (येथे V = वायुचे घनफळ N वायूचे वस्तुमान, ग्रॅमरेणूमध्ये R वायु–स्थिरांक). इतकेच नव्हे तर प्रत्यक्ष प्रयोगावरून असे दिसून येते की, R व R´ या गुणकांकांची मूल्ये एकच (०·०८२ लिटर/ वातवरण दाब / अंश/ ग्रॅमरेणू) येतात.
या गोष्टीवरून जे. एच्. व्हांट हॉफ यांनी अशी कल्पना मांडली की, विद्रुत अवस्थेत विद्रुताच्या रेणूंना वायु–रेणूंचे सर्व नियम लागू होतात म्हणजे ते जणू काही वायुरूप असल्याप्रमाणे वागतात.
यावरून साहजिकच असा निष्कर्ष काढता येतो की ०° से. तापमानाला कोणत्याही पदार्थाची संहती २२·४ लिटर विद्रावात एक ग्रॅम–रेणू असली, तर त्याचा तर्षणीय दाब १ वातावरण दाबाइतका असेल. मात्र हा नियम पुढील परिस्थितींत लागू पडत नाही : (१) विद्रावात विद्राव्याचे विदलन किंवा संगमन होत असल्यास (२) विद्रावाची संहती जास्त (दशांश सममूल्य विद्रावापेक्षा जास्त म्हणजे ज्यातील विद्रुताचे प्रमाण प्रती लिटर एक सममूल्य ग्रॅमरेणूभाराच्या दशांशापेक्षा जास्त नाही अशा विद्रावाच्या संहतीपेक्षा जास्त) असल्यास (३) विद्रावाचे तापमान जास्त असल्यास (सु. २५° से. पेक्षा जास्त).
तर्षण दाबाचे मापन : वरील समी. (४) वरून असे लक्षात येईल की, तर्षण दाबाचे मापन करून त्यावरून विद्रुताचा रेणुभार काढता येईल. विशेषतः मोठा रेणुभार असलेल्या द्रव्यांच्या बाबतीत हीच एक अचूक अशी पद्धती आहे व म्हणून तर्षण दाबाचे अचूक मापन करणे फार जरूरीचे आहे.
याबाबत पहिली आवश्यक गोष्ट म्हणजे आदर्श अर्धपार्य पटल मिळवणे ही होय. एम्, ट्राउबे यांनी १८६४ मध्ये कॉपर फेरोसायनाइड या अर्धपार्य पदार्थाचा शोध लावला, आतापर्यंत ज्ञात असलेल्या सर्व अर्धपार्य पदार्थात तो जास्त कार्यक्षम आहे. प्रयोगासाठी या पदार्थाचे अर्धपार्यपटल तयार करण्याची आधुनिक पद्धती पुढीलप्रमाणे आहे.
अगदी सूक्ष्म छिद्रे असलेली चिनी मातीचे भांडे प्रथम स्वच्छ धुवून नंतर त्याच्या छिद्रांतील हवा काढून टाकली जाते. नंतर त्या भांड्यात मोरचुदाचा सौम्य विद्राव्य भरून ते भांडे पॉटेशियम फेरोसायनाइडाच्या तशाच सौम्य विद्रावात ठेवतात. मोरचुदाच्या विद्रावात तांब्याची व फेरोसायनाइड विद्रावात प्लॅटिनमाची सळई घालतात आणि त्या सळया विद्युत घटाच्या (अनुक्रमे) धन व ऋण विद्युत् अग्रांना जोडतात. विद्युत् प्रवाहामुळे तांब्याचे व फेरोसायनाइडाचे आयन (विद्युत् भारित अणू वा रेणू) चिनी मातीच्या भांड्याच्या छिद्रांत (उलट-सुलट दिशेने) जोरात दाबले जातात. अशा तऱ्हेने त्या छिद्राछिद्रांत त्या दोन्ही प्रकारच्या आयनांचा संयोग होऊन कॉपर फेरोसायनाइडाचे पटल तयार होते. नंतर ते भांडे काढून स्वच्छ धुतात. पटल जास्त बळकट करण्यासाठी वरील क्रिया पुनःपुन्हा करतात. अशा तऱ्हेने अर्धपार्य पटलयुक्त कोश तयार करतात. वेगवेगळ्या शास्त्रज्ञांनी बनविलेले वेगवेगळ्या तत्त्वावर आधारलेले तऱ्हेतऱ्हेचे तर्षणमापक प्रचारात आहेत. त्यांपैकी बर्कली व हार्टली यांनी सिद्ध केलल्या तर्षणमापकाची थोडक्यात रूपरेषा खाली दिली आहे.
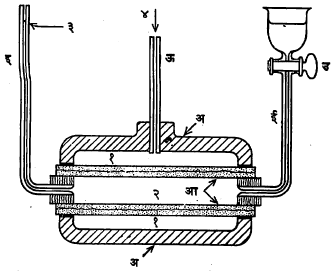 अ हे एक ब्रॉझचे बळकट भांडे असून त्यात आ ही अर्धपार्य चिनी मातीची नळी आडवी बसविली आहे. त्या नळीला इ व ई या दोन उभ्या नळ्या जोडलेल्या आहेत. अ ला ऊ ही बळकट नळी जोडलेली असून तिच्याद्वारे अ मधील विद्रावावरील दाब जलस्थितिक पद्धतीने (द्रवाद्वारे दाब संक्रामित करण्याच्या पद्धतीने) वाढवता येतो.
अ हे एक ब्रॉझचे बळकट भांडे असून त्यात आ ही अर्धपार्य चिनी मातीची नळी आडवी बसविली आहे. त्या नळीला इ व ई या दोन उभ्या नळ्या जोडलेल्या आहेत. अ ला ऊ ही बळकट नळी जोडलेली असून तिच्याद्वारे अ मधील विद्रावावरील दाब जलस्थितिक पद्धतीने (द्रवाद्वारे दाब संक्रामित करण्याच्या पद्धतीने) वाढवता येतो.
ज्या विद्रवाचा तर्षण दाब मोजावयाचा तो विद्राव अ मध्ये भरतात. आ मध्ये इतपत शुद्ध पाणी भरतात की, त्याची पातळी इ या निरीक्षणनलिकेत अगदी वर येईल. मग उ ही तोटी बंद करतात.
तर्षणामुळे जसजसे आ मधील पाणी बाहेर अ मध्ये येईल तसतशी इ मधील पाण्याची पातळी खाली येईल. ऊ मधून दाब हळूहळू असा वाढवत नेतात की, शेवटी त्यामुळे तर्षण बंद पडेल म्हणजेच इ मधील पाण्याची पातळी खाली जाण्याचे थांबेल, आता ऊ मधून दिलेला जादा दाब हा बरोबर त्या विद्रावाच्या तर्षण दाबाइतका असेल.
या मापकाच्या साहाय्याने तर्षण दाब खूप थोड्या वेळात मोजता येतो. अधिकात अधिक १५० वातावरण दाबापर्यंतचे तर्षण दाब या मापकाच्या साहाय्याने मोजता येतात.
तर्षणाशी संबंधित परिणाम : (अ) प्रयोगावरून असे दिसून येते की, शुद्ध विद्रावकापेक्षा विद्रावावरील बाष्पदाब कमी असतो. बाष्पदाबातील ही घट विद्रावाच्या तर्षण दाबावर अवलंबून असते. ⇨ ऊष्मागतिकीच्या साहाय्याने असे सिद्ध करता येते की,
|
π V1 = RT log
|
p0
p
|
… … …. (५)
|
येथे V1 हे विद्रावकाचे त्या विद्रावातील आंशिक रेणवीय घनफळ (१ मोल विद्रावकाचे घनफळ) असून P0 व P हे अनुक्रमे शुद्ध विद्रावक आणि विद्राव यांवरील बाष्पदाब आहेत. विद्रावाची संहती फार कमी असेल, तर [मॅक्लॉरिन सूत्र वापरून, → अवकलन व समाकलन] वरील समीकरण
|
π V1
|
=
|
P0 – p
|
…. …. …. …. (६)
|
|
RT
|
P0
|
असे लिहीता येते.
(आ) त्याचप्रमाणे शुद्ध विद्रावकापेक्षा विद्रावाचा उकळबिंदू काहीसा उच्च होतो व वितळबिंदू काहीसा नीच होतो, हे दोन्ही फरक तर्षण दाबाशी संलग्न आहेत.
|
π
|
=
|
L T
|
. Δ T …. …. …. …. (७)
|
|
V1 T02
|
येथे L ही उकळण्याची किंवा वितळण्याची सुप्त उष्णता (तापमान न बदलता १ ग्रॅम घन पदार्थ वितळविण्यासाठी किंवा १ ग्रॅम द्रवाची वाफ करण्यासाठी लागणारी उष्णता), T हे तर्षण दाब π असतानाचे तापमान, T0 हा शुद्ध विद्रावकाचा वितळबिंदू किंवा उकळबिंदू आणि ΔT ही विद्रावाच्या उकळबिंदूतील (किंवा वितळबिंदूतील) वाढ वा घट होय.
विद्युत् विच्छेद्यांचा तर्षण दाब : संगमन (दोन वा अधिक रेणू एकत्र होणे) किंवा विदलन (रेणूचे दोन वा अधिक तुकडे होणे) न होणाऱ्या विद्रावांचा तर्षण दाब विद्रुताच्या रेणु–संख्येशी सम प्रमाणात असतो परंतु विद्युत् विच्छेद्यांच्या (ज्यांतून विद्युत् प्रवाह नेला असता त्यांचे वहन ज्यांतील आयनांच्या प्रत्यक्ष स्थानांतरणाने होते अशा विद्रावांच्या) बाबतीत तर्षण दाब त्यापेक्षा जास्त असतो. ह्याचे कारण उघड आहे. विद्युत् विच्छेद्यामध्ये काही रेणूंचे आयनांमध्ये आधीच विदलन झालेले असते. अशा तऱ्हेने विद्रावातील मुक्त कणांची संख्या वाढल्याने तर्षण दाबही वाढतो. मंद विद्युत् विच्छेद्यात विदलन झालेल्या रेणूंचे प्रमाण कमी असते त्यामुळे तर्षण दाबातील वाढही कमी असते तर तीव्र विद्युत् विच्छेद्यात जवळजवळ सर्वच रेणू विदलित होतात त्यामुळे त्याचा तर्षण दाब जवळजवळ दुप्पट झालेला आढळतो.
तर्षण परिणामांची उपपत्ती : तर्षणाची उपपत्ती देताना प्रथम अर्धपार्यता कशी आणि का उत्पन्न होते, हे पाहिले पाहिजे परंतु या आविष्काराचा संपूर्णपणे समाधानकारक असा खुलासा अद्याप कोणाला देता आला नाही.
ट्राउबे यांच्या मताप्रमाणे अर्धपार्य पटल एखाद्या गाळण्याप्रमाणे कार्य करते. त्याच्यातील छिद्रांच्या आकारापेक्षा मोठे रेणू त्यातून पलीकडे जाऊ शकत नाहीत पण त्यापेक्षा लहान जाऊ शकतात. सकृतदर्शनी सहज पटणारी ही उपपत्ती सोडून देणे भाग पडते, कारण अर्धपार्य पटलातील छिद्रांपेक्षा कित्येक पटींनी लहान असे विद्रुताचे रेणू पलीकडे जाऊ शकत नाहीत, हे प्रयोगाने सिद्ध झाले आहे. एम्. लेरमीट यांनी सुचविलेली दुसरी उपपत्ती असे मानते की, अर्धपार्य पटलात विद्रावकाचे रेणू एकप्रकारे विरघळतात व मग त्या पटलातून ते पुढे जातात परंतु विद्रुताचे रेणू अशा तऱ्हेने विरघळत नाहीत म्हणून ते पलीकडे जाऊ शकत नाहीत. परंतु ही विरघळण्याची कल्पना फारच कृत्रिम वाटते व म्हणून ही उपपत्तीही मागे पडली आहे.
फार पूर्वी युस्टुस फोन लीबिक यांनी सुचविलेल्या अधिशोषणाच्या (पृष्ठभागावर होणाऱ्या शोषणाच्या) कल्पनेवर आधारलेली तिसरी उपपत्ती जास्त ग्राह्य वाटते. या उपपत्ती प्रमाणे अर्धपार्य पटलावर विद्रावकाच्या रेणूंचे अधिशोषण होते व विद्रुताच्या रेणूंचे होत नाही. अधिशोषित रेणू पटलातून क्रमशः पुढे जाऊ शकतात पण अशोषित रेणू असे जाऊ शकत नाहीत. या उपपत्तीला काही प्रमाणात प्रयोगाने पुष्टी मिळाली आहे.
वायूंच्या नियमांशी असलेल्या तर्षणाच्या नियमांच्या साम्यामुळे गत्यात्मक सिद्धांतावर [→ द्रव्याचा गत्यात्मक सिद्धांत] आधारलेल्या कल्पनांना अनुसरून तर्षण दाबाची उपपत्ती देण्याचा प्रथम प्रयत्न झाला परंतु ती कल्पना या बाबतीत संपूर्णपणे समाधानकारक ठरली नाही.
तर्षण दाबाची हल्ली सर्वमान्य झालेली उपपत्ती रासायनिक वर्चसाच्या (एका प्रावस्थेतून दुसऱ्या प्रावस्थेत एखादा पदार्थ जाण्याची निश्चिती करणाऱ्या भौतिक राशींच्या रा. व.) कल्पनेवर आधारलेली आहे.
अर्धपार्य पटलाच्या एका बाजूला विद्रावक आणि दुसऱ्या बाजूला तितक्याच दाबावर विद्राव असेल, तर ते समतोलात राहू शकत नाहीत कारण विद्रावक व विद्राव यांची रासायनिक वर्चसे सारखी नसतात. ती सारखी होण्यासाठी विद्रावावरचा दाब वाढवावा लागतो. समजा, विद्रावकावरील दाब P0 आणि या दाबाखाली त्याचे रा. व. μ० आहे आणि त्याच दाबाखाली विद्रावाचे रा. व. μ आहे. समजा की, विद्रावावरील दाब P इतका वाढविल्यास त्याचे रा. व. μ0 इतके होईल.
|
μ0 = μ +
|
∫
|
p
po
|
(
|
∂ μ
∂ p
|
)
|
T
|
dp … … … (८)
|
परंतु हा बदल समतापी (त्याच तापमानात होणारा) असून द्रवाची संपीड्यता (दाबामुळे संकोच पावण्याची क्षमता) अत्यल्प आहे.
म्हणून ( ∂ μ / ∂ p ) = V1
|
म्हणून p0 – p =
|
∫
|
p
|
V1 dP
|
… … … (९)
|
|
po
|
विद्राव आदर्श आहे आणि त्याची संहती अतिशय कमी आहे असे धरल्यास व ऊष्मगतिकीय सिद्धांतानुसार अखेर समी. (६) च्या आधारे
V1 (P – P0) = RT
हे सिद्ध करता येते, परंतु P – Po = π = तर्षण दाब.
म्हणून π V1 = RT
म्हणून π V = V R T
हेच व्हॉट हॉफ यांचे प्रसिद्ध समीकरण होय.
व्युत्क्रमी तर्षण : नेहमीच्या तर्षणात विद्रावक अर्धपार्य पटलातून कमी संहतीच्या विद्रावाकडून जास्त संहतीच्या विद्रावाकडे जात असतो. जास्त संहतीच्या विद्रावावर त्याच्या तर्षण दाबापेक्षा जास्त बाह्यदाब लावल्यास विद्रावकाचे चलन जास्त संहतीकडून कमी संहतीकडे म्हणजे नेहमीच्या उलट दिशेने होते, याला व्युत्क्रमी तर्षण असे म्हणतात.
खाऱ्या पाण्यापासून पिण्यायोग्य गोडे पाणी मिळविण्यासाठी ही पद्धत मोठ्या प्रमाणावर वापरली जात आहे. त्याचप्रमाणे फळांचे रस किंवा इतर पेयांची संहती वाढवणे, औषधी द्रव्ये शुद्ध करणे, कारखान्यांच्या सांडपाण्यातून वाहून जाणारी मूल्यवान द्रवे काढून घेणे, मैलापाणी वगैरेंमुळे होणारे प्रदूषण थांबविणे इ. अनेक क्षेत्रांत या पद्धतीचा उपयोग होऊ शकतो.
पुरोहित, वा. ल.
अर्धपाय पटलासंबंधींच्या समतोलपणाचा डॉनन सिद्धांत : सजीव ऊतकामध्ये (समान रचना व कार्य असणाऱ्या कोशिकांच्या म्हणजे पेशींच्या समूहामध्ये) कोशिकावरण हे अर्धपार्य पटल आहे, असे मानण्यात येते. त्यामुळे काही ठराविक आकारमानाचे आयन व पाण्याचे रेणू कोशिकावरणामधून पार होऊ शकतात. अशा आयनांना विसरणशील आयन असे म्हणतात. उदा., सोडियम, पॉटेशियम, हायड्रोजन, क्लोरीन, सल्फेट वगैरे. परंतु काही आयनांचे आकारमान कोशिकावरणामध्ये असणाऱ्या छिद्रापेक्षा मोठे असते. त्यामुळे ते कोशिकावरणामधून पार होत नाहीत. अशा आयनांना अविसरणशील आयन म्हणतात. उदा., प्रथिनाचे आयन. जेव्हा अर्धपार्य पटलाच्या दोन्ही बाजूंस विसरणशील आयनाचे विद्राव असतात, तेव्हा समतोल पाण्याच्या तत्त्वानुसार विद्राव्य आयनांची संहती कोशिकावरणाच्या दोन्ही बाजूंस समान होते परंतु कोशिकावरणाच्या एका बाजूस धन अथवा ऋण अविसरणशील आयन असतात, तेव्हा या आयनांचा अविसरणशील आयनांच्या संहतीवर कोशिकावरणाच्या दोन्ही बाजूंस काय परिणाम होतो, याचा अभ्यास १९११ मध्ये एफ्.जी. डॉनन या शास्त्रज्ञांनी केला व एक सिद्धांत मांडला.
समजा कोशिकावरणाच्या एका (१) बाजूला NaR चा विद्राव आहे. त्यामध्ये R— हा प्रथिनाप्रमाणे आयन असून तो अविसरणशील आहे. NaR विद्रावाची सुरुवातीची संहती अ आहे. कोशिकावरणाच्या दुसऱ्या (२) बाजूला आ संहिता असलेला विसरणशील आयनांचा, NaCI चा विद्राव आहे. प्रयोगाच्या सुरुवातीची स्थिती खाली दाखविल्याप्रमाणे आहे.
|
|
कोशिकावरण
|
|
|
|
↓
|
|
(१)
|
:
:
:
:
|
(२)
|
|
(अ)
|
Na+
|
Na+
|
(आ)
|
|
(अ)
|
R—
|
Cl—
|
(आ)
|
Na+ व CI— आयन हे विसरणशील असल्यामुळे ते (२) मधून (१) मध्ये येतील. तसेच (१) मधून (२) मध्येही जातील. काही वेळाने त्यांचा (२) कडून (१) कडे जाण्याचा अगर (१) कडून (२) कडे जाण्याचा वेग सारखा होऊन समतोल स्थिती प्राप्त होईल. या एकंदर घटनेत NaCI ची जेवढी संहती (२) मधून कमी होते तेवढीच (१) मध्ये वाढते. समतोलावस्थेत, समजा क्ष संहतीचे NaCI (२) मधून (१) कडे विसरित झालेले आहे. त्या वेळचे आयनांचे वाटप खालीलप्रमाणे दाखविता येईल.
|
(१)
(अ + क्ष) Na+
(अ) R—
(क्ष) Cl—
|
∶
∶
∶
∶
∶
|
(२)
Na+ (आ – क्ष)
Cl— ( आ – क्ष)
|
(२) कडून (१) कडे NaCI च्या विसरणाचा वेग (२) मध्ये असलेल्या Na+ व CI— आयन संहतीच्या गुणाकारावर अवलंबून असतो. म्हणजे (२) कडून (१) कडे
विसरणाचा वेग α (आ — क्ष) x (आ — क्ष)
तसेच (१) पासून (२) मध्ये NaCI चा विसरण वेग (१) मध्ये असलेल्या Na+ व CI— आयनांच्या सांद्रता गुणाकारावर अवलंबून असतो. म्हणजे (१) कडून (२) कडे
विसरणाचा वेग α (अ + क्ष) x क्ष
समतोलावस्थेत हे दोन्हीही वेग सारखे असल्यामुळे खालील समीकरण लिहिता येईल.
(आ — क्ष)२ = (अ + क्ष) x क्ष … … (१०) (२) (१)
हे डॉनन यांचे मूलभूत समीकरण पुढीलप्रमाणे लिहीता येईल.
[Na
+]
2 X [Cl
—]
2 = [Na
+]
1 X [Cl
—]
1 … (११)
(२) मध्ये सर्व आयन विसरणशील आहेत, तर (१) मध्ये विसरणशील आयनांबरोबर R— हा अविसरणशील आयनही आहे. त्यामुळे (१) मध्ये [Na+]1 ची संहती [CI—]1 पेक्षा जास्त आहे. कारण (१) मध्ये R— व CI— असे दोन प्रकारचे आयन ऋण भारित आहेत. (१) बाजू विद्युत् निर्भार करण्यासाठी Na+ ची संहती R— किंवा CI— यापेक्षा जास्त असणे जरूर आहे. पण (२) मध्ये मात्र [Na+]2 ची संहती [CI—]2 च्या बरोबर आहे. म्हणजे जेव्हा आपण विसरणशील आयनांचा गुणाकार म्हणतो तेव्हा (२) मध्ये तो वर्ग असतो, तर (१) मध्ये अविसरणशील आयनांच्या अस्तित्वामुळे तो वर्ग असू शकत नाही.
ह्याचाच दुसरा अर्थ म्हणजे (१) मधील [Na+] आयन संहती (२) मधील [Na+] आयन संहतीपेक्षा जास्त असते आणि (२) मधील [CI—] आयन संहती (१) मधील [CI—] आयन संहतीपेक्षा जास्त असते.
थोडक्यात डॉनन यांचे पटल समतोलत्वाचे संबंध पुढीलप्रमाणे मांडता येतील. (१) पटलाच्या एका बाजूला जेव्हा प्रथिनासारखे अविसरणशील ऋण भारित आयन असतात तेव्हा त्या बाजूस विसरणशील धन भारित आयनांची संहती दुसऱ्या बाजूपेक्षा जास्त असते. (२) पटलाच्या ज्या बाजूला अविसरणशील ऋण भारित आयन नसतात त्या बाजूला पारगम्य (पटलातून आरपार जाऊ शकणाऱ्या) ऋण भारित आयनांची संहती जास्त असते.
जेव्हा एखाद्या बाजूला अविसरणशील धन भारित आयन असतात तेव्हा विसरणशील आयनांची संहती वर सांगितल्याच्या विरूद्ध असते.
ह्या सिद्धांताच्या आधारे शरीरात निरनिराळ्या ठिकाणी आयनांची भिन्न भिन्न संहती का असते, हे समजून येईल, शरीरातील तर्षण दाबाच्या अभ्यासातही डॉनन नियमांचा उपयोग होतो.
हेगिष्टे, म. द.
सजीवांतील तर्षण नियमन : शरीरातील आंतरिक तर्षण दाब सापेक्षतेने स्थिर रहावा म्हणून प्राणी पाणी व आपल्या शरीरातील विरघळलेले पदार्थ (लवणे, प्रथिने इ.) यांच्यात जो योग्य समतोल राखतात त्याला तर्षण नियमन म्हणता येईल, वनस्पतींच्या शरीरातही पाण्याचा व आवश्यक पोषक खनिजांचा प्रवेश तर्षणाच्या प्रक्रियेने घडून येतो [ → वनस्पति व पाणी वनस्पतींचे खनिज पोषण].
जीवसृष्टी ही समुद्रात निर्माण झाली असे शास्त्रज्ञांचे मत आहे. या मताला आधारभूत असणारे एक प्रमुख उदाहरण म्हणजे समुद्रात राहणाऱ्या प्राण्यांचे रक्त आणि समुद्राचे पाणी यांचे पृथकरण केले असता त्या दोहोंमध्ये आढळणाऱ्या पदार्थांचे प्रमाण एकसारखे असल्याचे आढळते. हे प्राणी आपल्या शरीरात निर्माण होणारे अनेक टाकाऊ आणि निरुपयोगी पदार्थ आपल्या रक्तात राहू न देता ते शरीराच्या निरनिराळ्या अवयवांमार्फत शरीराबाहेर सोडून देतात. हे पदार्थ भोवतालच्या समुद्राच्या पाण्यात मिसळतात. अमोनिया, कार्बन डाय–ऑक्साइड यांसारखे निरुपयोगी वायू रक्तात विरघळले गेले, तरी वरील क्रियेमुळे शरीराबाहेर सोडले जातात. याच वेळी भोवतालचे समुद्राचे पाणी शरीरात हळूहळू शिरत असते परंतु या क्रियेमुळे त्या प्राण्याला अजिबात त्रास होत नाही.
समुद्राच्या पाण्याची लवणता जास्त असते, नदीतील किंवा तळ्यातील गोड्या पाण्याची लवणता कमी असते. जेथे नदी समुद्राला मिळते त्या नदीमुखातील पाण्याची लवणता मध्यम असते. जर समुद्रातील प्राणी गोड्या पाण्यात ठेवला, तर या प्राण्याच्या रक्तात जास्त प्रमाणात असलेल्या लवण पदार्थांमुळे गोडे पाणी शरीरात शोषून घेतले जाते व शरीरातील रक्ताचे आणि भोवतालच्या गोड्या पाण्याचे रासायनिक गुणधर्म समान होईपर्यंत ही क्रिया चालते. या क्रियेमुळे या प्राण्याच्या रक्तातील लवणता कमी होते आणि ही स्थिती प्राण्याला धोक्याची ठरते. याउलट गोड्या पाण्यातील प्राणी जर समुद्राच्या जास्त लवणता असलेल्या पाण्यात ठेवला, तर त्याच्या शरीरातील आणि रक्तातील पाणी शरीराबाहेर झिरपून भोवतालच्या खारट पाण्यात मिसळते. या क्रियेमुळे या प्राण्याला धोका निर्माण होऊन तो जगू शकत नाही परंतु अशा तऱ्हेने बाह्य परिस्थितीप्रमाणे आपल्या शरीरातील रक्ताचे गुणधर्म न बदलून ते तसेच कायम रहावेत अशा तऱ्हेची एक क्षमता या प्राण्यांमध्ये नैसर्गिकपणे निर्माण झालेली असते. या क्षमतेमुळे शरीरातील व रक्तातील पाणी, लवणे इत्यादींना शरीराबाहेर जाण्यास आणि बाहेरील पाणी व लवणे शरीरात येण्यास प्रतिबंध केला जातो, ही क्रिया म्हणजेच तर्षण नियमन होय.
समुद्रातील अनेक प्राणी नदीमुखाजवळील पाण्यात येतात तेव्हा या पाण्याच्या कमी लवणतेमुळे या प्राण्यांच्या शरीरद्रव्यातील लवण पदार्थ शरीराबाहेर झिरपतात. जर या पाण्याची लवणता काही कारणाने वाढली, तर ही लवणे परत शरीरात शोषली जातात. अशा प्राण्यांत तर्षण नियमनाची क्षमता निर्माण झालेली नसते. ज्या प्राण्यांच्या शरीरात तर्षण नियमनाची क्षमता निर्माण झालेली असते, असे सागरी प्राणी भोवतालच्या पाण्याची लवणता कमी अगर जास्त झाली तरी आपल्या शरीरद्रवाचे प्रमाण बदलू न देता आपले सर्व व्यवहार करू शकतात. यामुळे लवणांचे शरीराबाहेर उत्सर्जन किंवा शरीरात शोषण होऊ शकत नाही. अशा प्रकारे तर्षण नियमन करू शकण्याची पात्रता प्रथम या सागरी प्राण्यांत निर्माण झाली. समुद्रातील एककोशिक प्राणी संकोचशील रिक्तिकेवाटे (पोकळीवाटे), वलयी प्राणी वृक्ककांवाटे (निरूपयोगी द्रव्ये शरीराबाहेर टाकणाऱ्या इंद्रियांवाटे), कवचधारी प्राणी शृंगिका ग्रंथींवाटे व मासे वृक्कांवाटे तर्षण नियमन करतात. सीलेंटेरेट आणि एकायनोडर्म प्राणी कमी प्रमाणात तर्षण नियमन करतात. खेकड्यासारखे कवचधारी प्राणी आपल्या कवचात कायटिनासारखे पदार्थ साठवितात. हे पदार्थ पाण्याला आणि इतर पदार्थांना शरीरात शिरण्यास किंवा शरीराबाहेर जाण्यास विरोध करतात. माशांच्या शरीरावर असणाऱ्या खवल्यांमुळे किंवा बुळबुळीत चिकट पदार्थामुळे तर्षण नियमन केले जाते. या प्राण्यांत कार्बन डाय–ऑक्साइड किंवा अमोनियासारख्या विषारी वायुंचा व शरीरात जास्त साठलेल्या पाण्याचा निचरा व्हावा म्हणून उत्सर्जक इंद्रिये कार्यक्षम होतात.
शार्क सारखे उपास्थियुक्त मासे समुद्रात असतात. त्यांच्या रक्ताची संहती भोवतालच्या पाण्यापेक्षा जास्त असते. रक्तात ५० टक्क्यांहून अधिक भाग यूरिया हे द्रव्य असते. या द्रव्यावाटे शरीरातील अनावश्यक नायट्रोजन वायू शरीराबाहेर टाकला जातो. वास्तविक इतर प्राण्यांत इतक्या प्रमाणावर रक्तात यूरिया असणे धोक्याचे असते. सामन आणि ईल यांसारखे अस्थियुक्त मासे समुद्रातून नद्यांमध्ये व नद्यांतून समुद्रामध्ये सहजपणे संचार करू शकतात. हा संचार तर्षण नियमनाच्या पात्रतेमुळे सुलभ होतो. टेलिऑस्ट (अस्थिमत्स्य) जातीचे मासे प्रामुख्याने गोड्या पाण्यात राहतात परंतु त्यांच्या काही जाती समुद्रातही आढळतात. या माशांच्या शरीरद्रव्याची संहती खाऱ्या पाण्यापेक्षा जास्त असते. यावरून टेलिऑस्ट माशांचे मूळ निवासस्थान गोड्या पाण्यात असावे, असे अनुमान काढता येते. गोड्या पाण्यात राहणारे मासे शरीरातील जास्त प्रमाणात साठलेले पाणी मूत्रावाटे शरीराबाहेर टाकतात. खाऱ्या पाण्यात राहणारे मासे भक्ष्य खाताना भोवतालचे खारे पाणी पोटात घेतात. या पाण्यातील लवणांचा निचरा त्यांच्या कल्ल्यांच्या साह्याने केला जातो.
गोड्या पाण्यात राहणाऱ्या प्राण्यांना तर्षण नियमन करणाऱ्या अवयवांची अत्यंत गरज असते कारण त्यांच्या शरीरद्रव्यापेक्षा भोवतालच्या पाण्याची लवणता कमी असते. या प्राण्यांचे तर्षण नियमन करणारे अवयव उत्सर्जनाचे कार्यही करतात. आपल्या सागरी बांधवाप्रमाणेच एककोशिक प्राणी संकोचशील रिक्तिकेवाटे, वलयी व मृदुकाय प्राणी वृक्ककांवाटे, कवचधारी प्राणी शृंगिका ग्रंथींवाटे आणि मासे वृक्कांवाटे तर्षण नियमन व टाकाऊ पदार्थांचे उत्सर्जन करतात. अमोनिया व प्यूरिन यांसारखे टाकऊ पदार्थ क्लोमांमार्फत (कल्ल्यांमार्फत) शरीराबाहेर टाकले जातात.
जमिनीवर राहणाऱ्या प्राण्यांनाही शरीरात घेतलेले पाणी व शरीराबाहेर पडणारे पाणी यांचा समतोल कसा राखावयाचा, हा मोठा प्रश्न असतो. अत्यंत कोरड्या प्रदेशात राहणारे अनेक प्राणी पुष्कळ वेळा शरीरात अत्यंत कमी प्रमाणात पाणी राखू शकतात. जमिनीवर राहणारे पक्षी आणि सस्तन प्राणी उन्हाळ्यात बाष्पीभवनाने शरीराबाहेर जादा उष्णता टाकून देतात व शरीराचे तापमान कायम राखतात. शरीरातील आणि शरीराबाहेरील पाणी यांचा समतोल राखण्याचे काम या प्राण्यांचे वृक्क करतात. शरीरात लवणांचे व पाण्याचे प्रमाण वाढू लागले, तर वृक्क मूत्रावाटे या लवणांचा व पाण्याचा निचरा करतात. अन्नग्रहण करताना पाणी आणि लवणे शरीरात घेतली जातात. बाष्पीभवनामुळे व घामाच्या निर्मितीने शरीरातील पाणी कमी होते. वृक्कांच्या कार्यामुळे शरीरातील लवणे आणि पाणी यांचा निचरा होतो.
युरोमॅस्टिक्स ह्या प्राण्याला जेव्हा कोरड्या प्रदेशात रहावे लागते तेव्हा त्याच्या अवस्कराजवळ (ज्यात गुद, युग्मक–जनन कोशिकावाहिन्या आणि मूत्रवाहिन्या उघडतात अशा पश्चभागातील कोष्ठाजवळ) काही प्रमाणात पाणी साठविले जाते. सुप्तावस्थेत गेलेले उभयचर (जमिनीवर व पाण्यात राहणारे) आणि सरपटणारे प्राणी शरीरातील ५० टक्के पाणी कमी झाले, तरी ही स्थिती सहन करू शकतात. उन्हाळ्यात वलयी प्राण्यांच्या शरीरातील पाण्यात २० टक्के घट होते. परंतु ही घट पावसाळ्यात भरून काढली जाते. कोरड्या प्रदेशात राहणाऱ्या प्राण्यांच्या शरीरात पाण्याची कमीत कमी घट व्हावी या दृष्टीने अनेक योग्य बदल झालेले आढळतात. रेताड प्रदेशात आढळणारे भेक आणि सरपटणारे प्राणी मूत्रामधून शक्य तितके कमी पाणी शरीराबाहेर टाकतात. तसेच भोवतालच्या वातावरणात असणारे थोडेफार बाष्परूपी पाणी अवस्कराच्याद्वारे शरीरात शोषून घेतात. पक्षी शरीराचे तापमान ३° सें. इतके कमी करून पाण्याचा शरीराबाहेर होणारा निचरा टाळतात व मूत्रावाटे शक्य तितके यूरिक अम्ल शरीराबाहेर टाकतात. सस्तन प्राणी मूत्रावाटे शक्य तितके कमी पाणी शरीराबाहेर टाकून पाण्याचा समतोल राखतात.
देवमासा, सील आणि पॉरपॉइज (शिंशुक) यांसारख्या समुद्रात राहणाऱ्या सत्तन प्राण्यांच्या रक्ताची संहती भोवतालच्या समुद्राच्या पाण्याच्या मानाने कमी असली तरी या प्राण्यांच्या जमिनीवर राहणाऱ्या इतर जातीबांधवांच्या रक्ताच्या संहतीपेक्षा जास्त असते. हे प्राणी समुद्राचे खारे पाणी पितात व या पाण्यातील लवणांचा निचरा वृक्कांवाटे करतात. समुद्रात राहणाऱ्या टेलिऑस्ट जातीच्या माशाप्रमाणेच हे प्राणी त्यांच्या पूर्वजांच्या निवासस्थानी म्हणजेच समुद्रात परत रहावयास आले आहेत परंतु त्यांचे अवयव आणि ऊतके गोड्या पाण्यात राहणाऱ्या प्राण्यांप्रमाणेच कार्यक्षम असतात. म्हणून भोवतालच्या खाऱ्या पाण्यात रहावे लागले, तरी त्याच्या रक्ताचे गुणधर्म कायम टिकवणे त्यांना भाग पडते. क्रमविकासी (उत्क्रांतीच्या) प्रक्रियेच्या उघड अव्युत्क्रमतेचे हे एक उदाहरण आहे.
रानडे, द. र.
संदर्भ : 1. Durrant, P. J. General and Inorganic Chemistry, London. 1964.
2. Glasston, S. Thermodynamics for Chemists, New York, 1963.
3. Potts, W. T. W. Parry, G. Osmotic and Ionic Regulation in Animals, NewYork, 1964.
4. West, E. S. Todd, W. R. Textbook of Biochemistry, New York, 1961.
“
आपल्या मित्रपरिवारात शेअर करा..
 अ हे एक ब्रॉझचे बळकट भांडे असून त्यात आ ही अर्धपार्य चिनी मातीची नळी आडवी बसविली आहे. त्या नळीला इ व ई या दोन उभ्या नळ्या जोडलेल्या आहेत. अ ला ऊ ही बळकट नळी जोडलेली असून तिच्याद्वारे अ मधील विद्रावावरील दाब जलस्थितिक पद्धतीने (द्रवाद्वारे दाब संक्रामित करण्याच्या पद्धतीने) वाढवता येतो.
अ हे एक ब्रॉझचे बळकट भांडे असून त्यात आ ही अर्धपार्य चिनी मातीची नळी आडवी बसविली आहे. त्या नळीला इ व ई या दोन उभ्या नळ्या जोडलेल्या आहेत. अ ला ऊ ही बळकट नळी जोडलेली असून तिच्याद्वारे अ मधील विद्रावावरील दाब जलस्थितिक पद्धतीने (द्रवाद्वारे दाब संक्रामित करण्याच्या पद्धतीने) वाढवता येतो.