धातु–१ : निसर्गात सापडण्याऱ्या मूलद्रव्याचे भौतिक व रासायनिक गुणधर्मानुसार स्थूलमानाने धातू आणि अधातू असे दोन वर्ग पाडतात. त्यांतील पहिल्या वर्गाच्या मूलद्रव्यास (धातूला) घासून पृष्ठभागावर चकाकी आणता येते. त्यावर हातोडा मारला तर नाद उत्पन्न होतो. सर्व धातू स्फटिकमय आहेत. पारा ही धातू सोडल्यास सर्व धातू कठीण असून सामान्य तापमानास घन अवस्थेत राहतात. कथिल, शिसे, जस्त अशा काही थोड्या धातू सोडल्या तर धातू वितळण्याचे तापमान (वितळबिंदू) बरेच जास्त असते. बहुतेक धातू चांगल्या उष्णता आणि विद्युत् संवाहक आहेत. सर्व धातू अपारदर्शक आहेत. त्या धन विद्युत् भारधारक असून विद्युत् विश्लेषणात (विजेच्या साहाय्याने रेणूचे तुकडे करण्याच्या क्रियेत) उत्पन्न होणारे धातूंचे आयन (विद्युत् भारित अणू वा रेणू) ऋणाग्रावर जाऊन भारमुक्त होतात. बहुतेक धातू चांगल्या प्रसरणशील आणि आकार्य (आकार देण्यायोग्य) आहेत. बहुतेक धातूंचा अम्लांबरोबर सहज संयोग होत असल्याने त्या निसर्गात संयुगांच्या रूपात आढळतात. ही सर्व वैशिष्ट्ये सर्व धातूंत सारख्या प्रमाणात नसतात. धातूंचे काही गुणधर्म अधातवी द्रव्यांतही आढळतात. त्या द्रव्यांना धातुसदृश द्रव्ये (मेटलॉइड) म्हणतात.
सोने, तांबे आणि प्लॅटिनम या धातू अल्प प्रमाणात शुद्ध अवस्थेतही सापडतात. ज्या खनिजांपासून शुद्ध धातू व्यापारी पद्धतीने म्हणजे कमी खर्चाने मिळविता येतात, त्याला धातुक म्हणतात. धातुकामध्ये धातूचे प्रमाण फार कमी असले, तर प्रथम त्यामधील मलखनिजे अलग करतात व बाकीच्या भागातील धातूचा अंश क्रमाक्रमाने वाढवितात. या क्रियेला सांद्रण म्हणतात. धातूकाचे सांद्रण करण्यासाठी त्याला पाण्याने धुणे, पाखडणे, चुंबकीय अलगीकरण इ. विधी वापरतात.
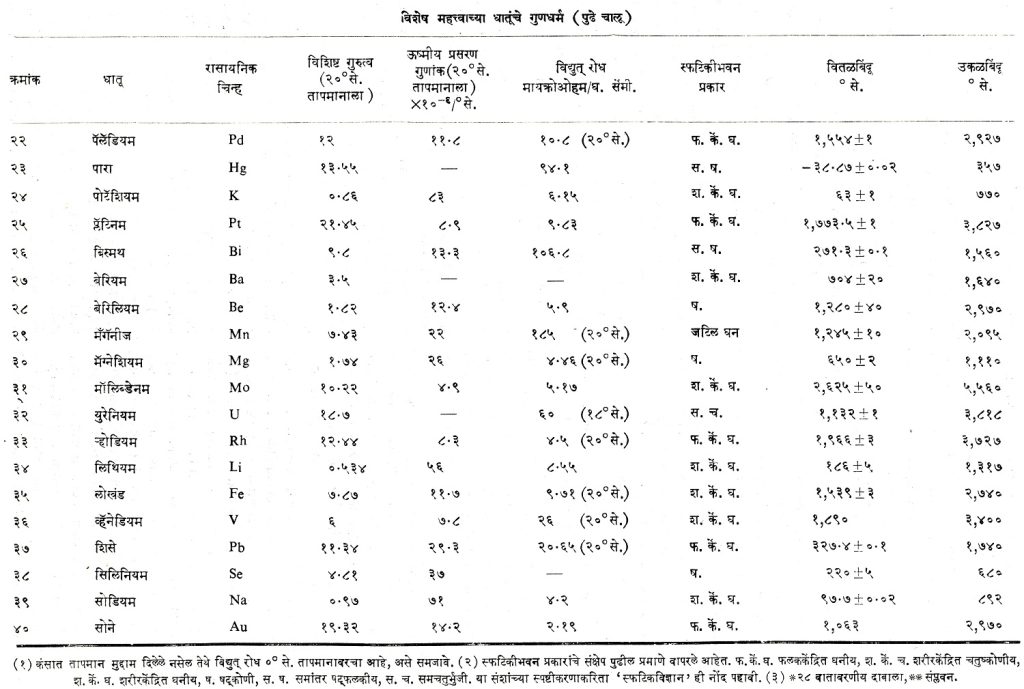
धातूंच्या अभ्यासाकरिता ⇨ आवर्त सारणी हे एक सोपे आणि सोईस्कर साधन आहे. या कोष्टकावरून धातूच्या गुणधर्मांची चांगली कल्पना येऊ शकते. आतापर्यंत माहीत असलेल्या १०४ मूलद्रव्यांमध्ये ८४ धातू आणि धातुसदृश मूलद्रव्ये आहेत. यांपैकी १० मूलद्रव्ये म्हणजे अमेरिसियम, बर्केलियम, कॅलिफोर्नियम, क्यूरियम, आइन्स्टाइनियम, फेर्मियम, मेंडेलेव्हियम, ॲस्टटीन, टेक्नेशियम आणि फ्रॅन्सियम निर्माण करण्यात आलेली आहेत. एकूण ८४ धातूंपैकी नेहमी उपयोगात येणाऱ्या ४० धातूंची विशेष माहिती पृष्ठ क्रमांक ५२ व ५३ वरील कोष्टकात दिली आहे.
रंग आणि घनता : आकर्षक पिवळ्या रंगाचे सोने, चमकदार पांढरी चांदी आणि लालसर तांबे या धातू सोडल्या, तर इतर बहुतेक धातू राखेसारख्या करड्या रंगाच्या पण कमीअधिक गडद छटांच्या आढळतात. लिथियम ही सर्वांत हलकी धातू असून ती पाण्यावर तरंगते. ऑस्मियम ही धातू सर्वांत जड आहे. ॲल्युमिनियम व मॅग्नेशियम या धातू हलक्या आहेत आणि त्यांच्यात इतरही पुष्कळ चांगले गुणधर्म आहेत. त्यामुळे त्यांना उद्योगधंद्यात विशेष महत्त्व आले आहे.
पारा ही धातू फार जड असून द्रवरूपात असल्यामुळे तापमापकामध्ये आणि हवेच्या दाबमापकात तिचा चांगला उपयोग होतो. लोखंड व त्यापासून मिळणारे पोलाद विपुल प्रमाणात मिळू शकतात आणि त्यामुळे किंमतीने स्वस्त असतात. त्या फार टिकाऊ व मजबूत असल्याने सर्व तऱ्हेच्या बांधकामात, यंत्रसामग्रीत व वाहने बनविण्याच्या कामात फार मोठ्या प्रमाणात वापरण्यात येतात.
वितळबिंदू आणि उकळबिंदू : बहुतेक धातू उच्च तापमानाला वितळत असल्या, तरी निरनिराळ्या धातूंच्या वितळबिंदूंत व उकळबिंदूंत पुष्कळ फरक असतो. पारा ही धातू सामान्य तापमानात द्रवरूपातच असते. टंगस्टन ही धातू सु. ३,४१०° से.ला वितळते. पारा ३५७° से.ला उकळतो. कॅडमियम ही धातू ७६५° से.ला उकळते व टंगस्टन ही धातू उकळण्यासाठी सु. ५,९३०° से. तापमान लागते.
उष्णता व प्रसरण : धातूचा तुकडा वा तार तापविल्यास त्याचे आकारमान वाढते. ही वाढ तापमान वाढीच्या प्रमाणात असते. या गुणाचा उपयोग उद्योगधंद्यात अनेक प्रकारे करून घेतात. चाकावर बसविण्याचे पोलादी कडे (धाव) लाल होईपर्यंत तापवितात. त्यामुळे त्याचा व्यास वाढतो व ते चाकाभोवती सहज बसविता येते. धाव थंड केली म्हणजे चांगली आकसते व चाकावर आवळून बसते. निरनिराळ्या दोन धातूंच्या तारांचा जोड तापविला आणि दुसरा जोड थंड ठेवला, तर त्या तारांच्या मंडलात विद्युत् प्रवाह सुरू होतो. हा प्रवाह थंड व गरम जोड यांच्या तापमानांतील फरकावर अवलंबून असतो. या गुणाचा उपयोग करून तपयुग्म जातीचे तापमापक बनवितात. दोन निरनिराळ्या धातूंच्या पट्ट्या जोडून तयार केलेली जोड पट्टी तापविली, तर ती तात्पुरती वाकते व थंड झाल्यावर पुन्हा पूर्वस्थितीत येते. या गुणाचा उपयोग करून विद्युत् मंडलातील स्विचांची उघडझाप करतात. बिस्मथ गटातील धातुमिश्रणे घन अवस्थेतून द्रव अवस्थेत जाताना आकुंचन पावतात व द्रवातून घन होताना प्रसरण पावतात. या गुणाचा उपयोग करून छपाईचे खिळे तयार करतात.
उष्णता आणि विद्युत संवाहकता : धातूंच्या अंगी असलेल्या काही विशेष गुणधर्माचे कारण त्यांच्या स्फटिकांच्या अंतर्रचनेत आहे. अधातवी द्रव्यांपेक्षा धातूंच्या स्फटिकातील अणूंची रचना भरीव असते. त्यांच्या अणूतील सर्वांत बाहेरच्या कक्षेतील इलेक्ट्रॉनांची संख्या नील्स बोर यांच्या अणुसिद्धांतानुसार [⟶ अणु व आणवीय संरचना] स्थिर राहण्यासाठी पुरेशी नसते. त्यामुळे धातूच्या अणूंच्या बाहेरील कक्षेतील इलेक्ट्रॉन सर्वत्र फिरत असतात. या मुक्त इलेक्ट्रॉनांमुळेच उष्णतेचे आणि विद्युत् प्रवाहाचे संवहन साध्य होते. धातूचे तापमान वाढले, तर संवाहकता कमी होते व तापमान कमी केले, तर तिची विद्युत् संवाहकता वाढते. धातूचे तापमान -१००° से. पेक्षा जितके कमी करावे त्या मानाने विद्युत् संवाहकता पुष्कळ जास्त प्रमाणात वाढत जाते [⟶ अतिसंवाहकता]. या गुणाचा उपयोग करून मोठ्या शक्तीचे चुंबकीय क्षेत्र उत्पन्नक करतात. धातूची विद्युत् संवाहकता तिच्या शुद्ध अवस्थेत सर्वांत जास्त असते धातू अशुद्ध असेल, तर त्या प्रमाणात ती कमी होते. चांदी ही धातू सर्वांत उत्तम विद्युत् संवाहक आहे. चांदीच्या खालोखाल तांबे व तांब्याच्या खालोखाल ॲल्युमिनियम या धातू आहेत. ॲल्युमिनियम ही धातू तांब्यापेक्षा बरीच हलकी असल्यामुळे तेवढ्याच विद्युत् प्रवाहासाठी तांब्यापेक्षा कमी वजनाची ॲल्युमिनियमची संवाहक तार पुरते. तांबे, पितळ, चांदी, निष्कलंक (स्टेनलेस) पोलाद इ. धातू व मिश्रधातू उष्णतेचे उत्तम प्रकारे संवहन करीत असल्यामुळे व्यवहारात (खाद्यपदार्थ शिजवावयाची पात्रे, रासायनिक प्रक्रियांत लागणारी पात्रे इत्यादींसाठी) या धातूंचा व मिश्रधातूंचा मोठ्या प्रमाणावर उपयोग होतो.
चुंबकीय गुणधर्म : लोखंड, कोबाल्ट आणि निकेल या धातू चांगल्या चुंबकीय जातीच्या आहेत. त्या मानाने इतर बहुतेक धातू अचुंबकीय आहेत परंतु काही धातूंची मिश्रणे चुंबकीय असतात. उदा., ॲल्युमिनियम, तांबे व मँगेनीज यांचे मिश्रण चुंबकीय आहे [⟶ चुबंकत्व].
धातूंच्या स्फटिकांचे प्रकार : धातुस्फटिकातील अणूंची रचना मुख्यतः तीन प्रकारची असते. (१) शरीरकेंद्रित घनीय, (२) फलककेंद्रित घनीय व (३) षट्कोणी. काही धातूंचे स्फटिक अगदी पातळ पण चतुष्कोणी असतात. आवर्त सारणीच्या उपगटांतील धातूंचे स्फटिक बहुधा एकाच प्रकारचे असतात. काही धातूंचे स्फटिक अनेक प्रकारचे असतात. अशा प्रकारांना बहुरूपे म्हणतात. अशा बहुरूपतेमुळे धातूच्या गुणधर्मातही थोडा फरक पडतो [⟶ स्फटिकविज्ञान].
यांत्रिक गुणधर्म : आपल्या जीवनात धातूंना जे महत्त्वाचे स्थान मिळाले आहे, त्याचे कारण म्हणजे धातूंच्या अंगी असलेले यांत्रिक गुणधर्म हेच आहे. आकार बदलाला धातू चांगला प्रतिकार करतात. तन्यता, ताणसामर्थ्य, कठिनता, स्थितिस्थापकत्व (लवचिकपणा), प्रसरणशीलता, आकार्यता वगैरे गुणधर्म धातूच्या प्रतिकार शक्तीची रूपेच आहेत. याबाबतीत स्फटिक सीमांच्या प्रभावामुळे धातूच्या स्फटिक समूहाचे वर्तन एकट्या स्फटिकापेक्षा निराळ्या प्रकारचे असते. बहुतेक धातू बळकट व चांगल्या प्रसरणशील आहेत. धातूचा रस करून पाहिजे त्या आकाराचे ओतीव तयार करता येते. धातूचे पंच तयार करून पाहिजे त्या आकाराची भांडी घडविता येतात [→ धातूंचे यांत्रिक गुणधर्म]. प्रत्येक धातूसंबंधीचा इतिहास, गुणधर्म इ. माहिती त्या त्या धातूच्या स्वतंत्र नोंदीत दिलेली आहे.

संदर्भ : 1. The American Society for Metals, Metals Handbook, New York, 1948.
2. Vasilyev, M. Metals and Man, Moscow, 1967.
ताम्हणकर, रा. वा.